
【题目】请完成下列填空:
(1)当NH3和N2H4所含分子数之比为1∶1时,其所含原子数之比为____,质量之比为____。
(2)现有m g某气体A,其摩尔质量为M g·mol-1。
①气体A在标准状况下的体积为____L
②A溶于水后形成V L溶液(A与水不反应),所得溶液的物质的量浓度为____ mol·L-1。
(3)将a mL 2 mol·L-1的Mg(NO3)2溶液稀释至b mL,稀释后溶液中NO3-的物质的量浓度为____mol/L
(4)一定体积的0.2 mol·L-1的BaCl2溶液,可使相同体积的Na2SO4溶液、KAl(SO4)2溶液、Fe2(SO4)3溶液3种溶液中的SO42-完全沉淀,则上述3种硫酸盐溶液的物质的量浓度比为____。
【答案】2∶3 17∶32 ![]()
![]()
![]() 6∶3∶2
6∶3∶2
【解析】
(1)当NH3和N2H4中分子个数比为1:1 时,原子总数之比为:1×4:1×6=2:3;质量之比为:1×17:1×32=17:32;
(2)①mg该气体的物质的量为:n=![]() =
=![]() mol,在标准状况下的体积为:V=n×22.4L/mol=22.4L/mol×
mol,在标准状况下的体积为:V=n×22.4L/mol=22.4L/mol×![]() mol=
mol=![]() L;
L;
②A溶于水后形成V L溶液(A与水不反应),所得溶液的物质的量浓度c=![]() =
=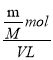 =
=![]() mol·L-1;
mol·L-1;
(3)先由稀释定律计算稀释后c[Mg(NO3)2] =![]() mol/L,再由溶质电离方程式Mg(NO3)2= Mg2++2NO3-可知,c(NO3-) = 2 c[Mg(NO3)2] =
mol/L,再由溶质电离方程式Mg(NO3)2= Mg2++2NO3-可知,c(NO3-) = 2 c[Mg(NO3)2] =![]() mol/L;
mol/L;
(4)要使同体积同浓度的BaCl2溶液中钡离子完全沉淀,则消耗Na2SO4、KAl(SO4)2、Fe2(SO4)3三种溶液中的SO42-的物质的量相等,三种溶液体积相等,则三种溶液中硫酸根离子的浓度相等,Na2SO4、KAl(SO4)2、Fe2(SO4)3中SO42-个数之比为1:2:3,要使硫酸根离子浓度相等,则这三种盐溶液的浓度之比为6:3:2。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 4.6gC2H5OH与6.0gCH3COOH反应,生成的 CH3COOC2H3分子数目为0.1NA
B. 5.6gFe与足量水蒸气完全反应,转移的电子数目为0.2NA
C. 32gO2和O3的混合物中含有的氧原子数目为2NA
D. 25℃时,1L pH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是
A. 纯碱溶液去油污
B. 铁在潮湿的环境下生锈
C. 用氯化铁溶液制氢氧化铁胶体
D. 利用明矾溶液的酸性可清除铜制品表面的铜锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中滴加另一种溶液或通入某种气体时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )
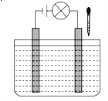
A.盐酸中逐滴加入食盐溶液
B.醋酸中逐滴加入氢氧化钠溶液
C.饱和石灰水中不断通入CO2
D.醋酸中逐滴加入氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各离子浓度关系正确的是
A. pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B. 浓度为0.1 mol·L-1的碳酸氢钠溶液:c(Na+)+ c(H+)=c(HCO3-)+c(OH-)
C. 浓度为0.1 mol·L-1的(NH4)2CO3溶液:c(NH4+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D. 浓度均为0.1 mol·L-1的醋酸溶液与NaOH溶液混合后:c(OH-)=c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰干电池的负极是作为电池壳体的金属锌,正极是被二氧化锰和碳粉包围的石墨电极,电解质是氯化锌和氯化铵的糊状物,该电池放电过程中产生 MnOOH。废旧电池中的Zn、Mn元素的回收,对环境保护有重要的意义。
Ⅰ. 回收锌元素,制备ZnCl2
步骤一:向除去壳体及石墨电极的黑色糊状物中加水,搅拌,充分溶解,经过滤分离得固体和滤液。
步骤二:处理滤液,得到ZnCl2·xH2O晶体。
步骤三:将SOCl2与ZnCl2·xH2O晶体混合制取无水ZnCl2。
制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略) 的装置如下:

(已知: SOCl2是一种常用的脱水剂,熔点-105℃,沸点79℃,140℃以上时易分解,与水剧烈水解生成两种气体。)
(1)写出SOCl2与水反应的化学方程式:______________________。
(2)接口的连接顺序为a→___→___→ h → h →___→___→___→e。______________
Ⅱ. 回收锰元素,制备MnO2
(3)洗涤步骤一得到的固体,判断固体洗涤干净的方法:_________________________。
(4)洗涤后的固体经初步蒸干后进行灼烧,灼烧的目的__________________________。
Ⅲ. 二氧化锰纯度的测定
称取1.40g灼烧后的产品,加入2.68g草酸钠(Na2C2O4)固体,再加入足量的稀硫酸并加热(杂质不参与反应),充分反应后冷却,将所得溶液转移到100mL容量瓶中用蒸馏水稀释至刻线,从中取出20.00mL,用0.0200mol/L高锰酸钾溶液进行滴定,滴定三次,消耗高锰酸钾溶液体积的平均值为17.30mL。
(5)写出MnO2溶解反应的离子方程__________________________________________。
(6)产品的纯度为______________________ 。
(7)若灼烧不充分,滴定时消耗高锰酸钾溶液体积_____(填“偏大”、“ 偏小”、“ 不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积相同的两个容器中,充入等质量CO2和CO气体,下列判断正确的是( )
A.CO2和CO对容器产生的压强之比是7∶11
B.CO2和CO的密度之比是11∶7
C.CO2和CO的分子数相等
D.CO2和CO的氧原子个数比是22∶7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种常见单萜类化合物的结构如下图所示。下列说法正确的是( )
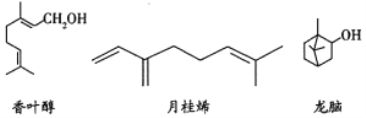
A. 香叶醇和龙脑互为同分异构体,分子式均为![]()
B. 可用金属钠鉴别香叶醇和月桂烯
C. 龙脑分子中所有碳原子在同一个平面上
D. 1mol月桂烯最多能与![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是_____,D是_____,G是_____,H是_____(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:__________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_________。
(3)A中元素的原子结构示意图为________。
(4)F在溶液中的电离方程式为_________。
(5)上述反应中属于氧化还原反应的是_______(填写序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com