
【题目】常温下,下列溶液中各离子浓度关系正确的是
A. pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B. 浓度为0.1 mol·L-1的碳酸氢钠溶液:c(Na+)+ c(H+)=c(HCO3-)+c(OH-)
C. 浓度为0.1 mol·L-1的(NH4)2CO3溶液:c(NH4+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D. 浓度均为0.1 mol·L-1的醋酸溶液与NaOH溶液混合后:c(OH-)=c(H+)+c(CH3COOH)
【答案】A
【解析】
A、因醋酸为弱酸,pH=2的醋酸与pH=12的氢氧化钠溶液等体积混合,反应后为醋酸和醋酸钠的混合溶液,该溶液显酸性,弱电解质的电离大于醋酸根离子的水解,则c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故A正确;
B、浓度为0.1 mol·L-1的碳酸氢钠溶液,由电荷守恒可以知道c(Na+)+ c(H+)=2cCO32-)+c(HCO3-)+c(OH-),故B错误;
C、浓度为0.1 mol·L-1的(NH4)2CO3溶液,由物料守恒可以知道c(NH4+)+c(NH3![]() H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) ,故C错误;
H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) ,故C错误;
D、浓度均为0.1 mol·L-1的醋酸溶液与NaOH溶液若等体积混合,恰好生成醋酸钠,由质子守恒可以知道c(OH-)=c(H+)+c(CH3COOH),但混合时溶液体积未知,故D错误;
所以A选项是正确的。


科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数 K=2×10-5。已知:Ni(CO)4的沸点为 42.2℃,固体杂质不参与反应。第一阶段:将粗镍与 CO 反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是
Ni(CO)4(g)。230℃时,该反应的平衡常数 K=2×10-5。已知:Ni(CO)4的沸点为 42.2℃,固体杂质不参与反应。第一阶段:将粗镍与 CO 反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是
A. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
B. 增大c(CO),平衡正向移动,反应的平衡常数增大
C. 第二阶段,Ni(CO)4分解率较低
D. 增加Ni的含量,CO的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“H2O(l)→H2O(g)→H2和O2”的变化过程中,被破坏的作用力依次是
A. 分子间作用力、离子键B. 分子间作用力、共价键
C. 共价键、离子键D. 共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是( )
A.银、二氧化硫、硫酸、烧碱、食盐
B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙
C.氢气、干冰、硝酸、烧碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、碳酸氢钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员将Cu与Cu2O的混合物ag,用足量的稀H2SO4充分反应后,剩余固体质量为bg。
已知:Cu2O+2H+═Cu+Cu2++H2O
(1)混合物中n(Cu2O)=________mol(用含a、b的最简式表示)
(2)若将ag混合物在空气中加热生成CuO,则m(CuO)=_______g(用含a、b的最简式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成下列填空:
(1)当NH3和N2H4所含分子数之比为1∶1时,其所含原子数之比为____,质量之比为____。
(2)现有m g某气体A,其摩尔质量为M g·mol-1。
①气体A在标准状况下的体积为____L
②A溶于水后形成V L溶液(A与水不反应),所得溶液的物质的量浓度为____ mol·L-1。
(3)将a mL 2 mol·L-1的Mg(NO3)2溶液稀释至b mL,稀释后溶液中NO3-的物质的量浓度为____mol/L
(4)一定体积的0.2 mol·L-1的BaCl2溶液,可使相同体积的Na2SO4溶液、KAl(SO4)2溶液、Fe2(SO4)3溶液3种溶液中的SO42-完全沉淀,则上述3种硫酸盐溶液的物质的量浓度比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20 mL 0.01 mol·L-1HA(aq)中不断滴入0.02 mol·L-1 NaOH(aq),混合溶液pH变化如图所示。此过程溶液下列说法不正确的是(已知:25℃时一元酸HA(aq)电离平衡常数Ka=1.6×10-5)

A. a点溶液的pH大于3
B. b点溶液中离子:c(A-)>c(Na+)>c(H+)>c(OH-)
C. c点表示酸HA(aq)和NaOH(aq)溶液恰好完全反应
D. d点溶液加水稀释后c(H+)/c(HA)的值会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特利原理来解释的是
A. 用排饱和食盐水的方法收集氯气
B. 增大压强,有利于SO2和O2反应生成SO3
C. 在Fe3++3SCN-![]() Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
D. 合成氨工业选择高温(合成氨反应为放热反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 Q、W、X、Y、Z原子序数依次增加,其中Q、W原子核外L 电子层的电子数分别为0、4,X、Y、Z在周期表中的位置如图所示。 下列说法不正确的是
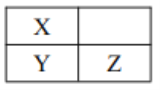
A. W、 X、 Q 的原子半径依次减小 B. Y 的最高价氧化物的水化物一定是强酸
C. W 和 Z 可能形成化合物W3Z8 D. Q、 X、 Z 可能形成离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com