
【题目】中学常见物质A、B、C、D、E、X,存在下图转化关系 ![]() 部分生成物和反应条件略去
部分生成物和反应条件略去![]() 。下列推断不正确的是
。下列推断不正确的是![]()
![]()
A.若D是一种强碱,则A、B、C均可与X反应生成D
B.若D为NaCl,且A可与C反应生成B,则E可能是![]()
C.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、R五种元素均位于周期表的前四周期,且原子序数依次增大。元素X的基态原子中电子占据了三种能量不同的原子轨道,且成对电子数是未成对电子数的2倍;元素Y与W同主族,且Y是地壳中含量最多的元素;Z基态原子有12种不同运动状态的电子;元素R基态原子最外层只有1个电子且内层电子全充满。
请回答下列问题:(答题时,X、Y、Z、W、R用所对应的元素符号表示)
(1)基态Y原子的轨道式表示式为![]() ___。
___。
(2)元素Y、W均可形成含18个电子的氢化物,其中Y的氢化物沸点较高,原因是___;
(3)元素Z与同周期相邻两元素第一电离能由高到低的顺序为___。
(4)元素R在周期表中位于___区,R分别与Y、W形成离子化合物R2Y和R2W,其中熔点较高的为___。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)4]2+,在配离子中与R2+形成配位键的原子是___。
(6)X的一种单质(相邻原子间通过共价键形成空间网状结构)、XY2、WY2、ZW对应的晶体熔沸点由高到低的顺序为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监测测定水中溶解氧的方法是:①量取25.00mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为:2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用0.1000mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗VmL。有关反应式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O、I2+2S2O32-=2I-+S4O62-
滴定次数 | 待测液的体积/mL | 0.1000mol·L-1 Na2S2O3的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
试回答:
(1)消耗Na2S2O3的体积平均值为___mL,水中溶解氧的量是(以g/L为单位,保留3位有效数字)___。
(2)滴定(I2和S2O32-反应)以淀粉溶液为指示剂,终点时现象为___。
(3)判断下列操作引起的误差(填“偏大”、“偏小” “无影响”或“无法判断”)
①读数:滴定前平视,滴定后俯视___。
②未用标准液润洗滴定管___。
③配制Na2S2O3溶液时,其固体中含有对反应体系无影响的杂质___。
④待测液的滴定管之前有气泡,取液后无气泡___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)把SO2通入盛有H2S的溶液中出现淡黄色浑浊,该反应的化学方程式为____________________。
(2)将二氧化硫通入氯化钡溶液无现象,滴入新制的氯水有白色沉淀生成,写出反应的离子方程式:_________________________。
(3)硫酸亚铁铵[(NH4)2Fe(SO4)2]隔绝空气加热至500℃时能完全分解,分解产物中含有氧化铁、二氧化硫、氨气、氮气和水蒸气,反应的化学方程式为__________________。
(4)向氯化铜溶液中通入SO2,加热生成CuCl白色沉淀,离子方程式为___________________。
(5)把氧气通入Cu与浓硫酸反应后剩余的溶液中,铜片继续溶解,反应的化学方程式为________________________________________。
(6)①磷化氢(PH3)通入盛有Fe2(SO4)3溶液的试管中,颜色由棕黄色变成淡绿色,同时还有白色蜡状固体生成,反应的离子方程式是____________________。
②PH3有剧毒,用CuSO4溶液吸收,生成物中有Cu3P、H3PO4,写出反应的化学方程式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.保持容器体积不变,增加H2O(g)的量
B.保持容器体积不变,充入氦气使体系压强增大
C.将容器的体积缩小一半
D.保持容器压强不变,充入氦气使容器体积变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验“操作和现象”与“结论”对应关系正确的是![]()
操作和现象 | 结论 | |
A | 常温下,将Al箔插入浓 | 铝和浓硝酸不反应 |
B | 向饱和 | 析出了 |
C | 用铂丝蘸取溶液进行焰色反应,观察到火焰呈黄色 | 该溶液一定是钠盐溶液 |
D | 向装有 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A. I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B. II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种药物在临床上有许多的应用,具有去热、镇痛等疗效,以下是该药物的合成路线:
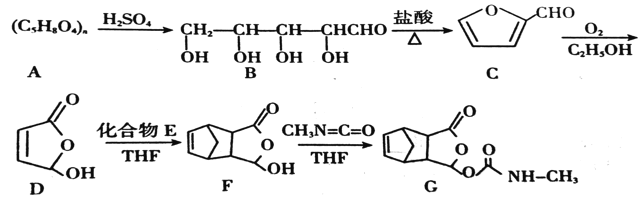
已知:CH2=CH—CH2=CH2+CH2=CH2![]()
(1)化合物C的分子式为__,B中含氧官能团的名称是__。
(2)E的一氯代物有__种,F→G的反应类型为__。
(3)写出D→F的化学方程式__。
(4)F的同分异构体有多种,符合以下条件的同分异构体有__种,写出其中一种的结构简式__。
①属于二取代芳香化合物,苯环上的一氯代物有两种
②能与FeCl3溶液发生显色反应
③能与碳酸氢钠反应产生气体
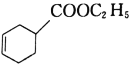
(5)写出由2—溴丁烷、丙烯酸和乙醇为原料合成如图物质的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个体积相同带活塞的容器,分别盛装一定量的颜色相同的NO2(g)和Br2(g),迅速将两容器同时压缩到原来的一半(假设气体不液化),下列说法正确的是( )

A.a→a′过程中,颜色突然加深,然后逐渐变浅,最终颜色比原来的浅
B.a′,b′的颜色一样深
C.a′的压强比a的压强2倍要小,b′的压强为b的压强的2倍
D.a′中的c(NO2)一定比b′中的c(Br2)小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com