
ЎҫМвДҝЎҝөӘј°Жд»ҜәПОпКЗҝЖС§јТГЗТ»ЦұФЪМҪҫҝөДОКМвЈ¬ЛьГЗФЪ№ӨЕ©ТөЙъІъәНЙъГь»о¶ҜЦРЖрЧЕЦШТӘөДЧчУГЎЈ»ШҙрПВБРОКМвЎЈ
ўс.ТСЦӘHЎӘHјьөДјьДЬОӘ436kJЎӨmol-1Ј¬NЎӘHјьөДҪЎДЬОӘ391kJЎӨmol-1Ј¬N![]() NјьөДјьДЬКЗ945.6 kJЎӨmol-1Ј¬Фт·ҙУҰNH3(g)
NјьөДјьДЬКЗ945.6 kJЎӨmol-1Ј¬Фт·ҙУҰNH3(g)![]()
![]() N2(g)+
N2(g)+![]() H2(g)өДҰӨH=______Ј¬ИфФЪДіОВ¶ИПВЖдЖҪәвіЈКэОӘKЈ¬ФтN2(g)+3H2(g)
H2(g)өДҰӨH=______Ј¬ИфФЪДіОВ¶ИПВЖдЖҪәвіЈКэОӘKЈ¬ФтN2(g)+3H2(g) ![]() 2NH3(g)өДЖҪәвіЈКэK1=___________ЈЁУГKұнКҫЈ©
2NH3(g)өДЖҪәвіЈКэK1=___________ЈЁУГKұнКҫЈ©
ўт.ВИ°ұКЗВИЖшУцөҪ°ұЖш·ҙУҰЙъіЙөДТ»Аа»ҜәПОпЈ¬КЗіЈУГөДТыУГЛ®¶юј¶Пы¶ҫјБЈ¬ЦчТӘ°ьАЁТ»ВИ°ұЎў¶юВИ°ұәНИэВИ°ұ(NH2ClЎўNHCl2әНNCl3)Ј¬ёұІъОпЙЩУЪЖдЛьЛ®Пы¶ҫјБЎЈ
ЈЁ1Ј©№ӨТөЙПҝЙАыУГ·ҙУҰ2Cl2(g)+NH3(g)![]() NHCl2 (l)+2HCl(g)ЦЖұё¶юВИ°·ЎЈ
NHCl2 (l)+2HCl(g)ЦЖұё¶юВИ°·ЎЈ
ўЩ¶юВИ°ұФЪЦРРФЎўЛбРФ»·ҫіЦР»б·ўЙъЗҝБТЛ®ҪвЈ¬ЙъіЙҫЯУРЗҝЙұҫъЧчУГөДОпЦКЈ¬РҙіцҫЯУРЗҝЙұҫъЧчУГөДОпЦКөДөзЧУКҪ_______________________ЎЈ
ўЪФЪәгОВМхјюПВЈ¬Ҫ«2molCl2әН1molNH3ідИлДіГЬұХИЭЖчЦР·ўЙъЙПКц·ҙУҰЈ¬ІвөГЖҪәвКұCl2әНHClөДОпЦКөДБҝЕЁ¶ИУлЖҪәвЧЬС№өД№ШПөИзНјЛщКҫЎЈФтAЎўBЎўCИэөгЦРCl2ЧӘ»ҜВКЧоёЯөДКЗ________өгЈЁ МоЎ°AЎұ Ў°BЎұ»тЎ°CЎұЈ©Ј»јЖЛгCөгКұёГ·ҙУҰөДС№ЗҝЖҪәвіЈКэKp(C)=_____________ЈЁKpКЗЖҪәв·ЦС№ҙъМжЖҪәвЕЁ¶ИјЖЛгЈ¬·ЦС№= ЧЬС№ЎБОпЦКөДБҝ·ЦКэЎЈЈ©

ЈЁ2Ј©УГCl2әНNH3·ҙУҰЦЖұёИэВИ°·өД·ҪіМКҪОӘ3Cl2(g)+NH3(g)![]() NCl3(l)+3HCl(g)Ј¬ПтИЭ»эҫщОӘ1LөДјЧЎўТТБҪёцәгОВЈЁ·ҙУҰОВ¶И·ЦұрОӘ400ЎжЎўTЎжЈ©ИЭЖчЦР·ЦұрјУИл2molCl2әН2molNH3Ј¬ІвөГёчИЭЖчЦРn(Cl2)Лж·ҙУҰКұјдtөДұд»ҜЗйҝцИзПВұнЛщКҫЈә
NCl3(l)+3HCl(g)Ј¬ПтИЭ»эҫщОӘ1LөДјЧЎўТТБҪёцәгОВЈЁ·ҙУҰОВ¶И·ЦұрОӘ400ЎжЎўTЎжЈ©ИЭЖчЦР·ЦұрјУИл2molCl2әН2molNH3Ј¬ІвөГёчИЭЖчЦРn(Cl2)Лж·ҙУҰКұјдtөДұд»ҜЗйҝцИзПВұнЛщКҫЈә
t /min | 0 | 40 | 80 | 120 | 160 |
n(Cl2)(јЧИЭЖч)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(Cl2)(ТТИЭЖч)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
ўЩTЎж__________400ЎжЈЁМоЎ°>Ўұ»тЎ°<ЎұЈ©ЎЈ
ўЪёГ·ҙУҰөДҰӨH__________0ЈЁМоЎ°>Ўұ»тЎ°<ЎұЈ©ЎЈ
ўЫёГ·ҙУҰЧФ·ўҪшРРөДМхјюКЗ__________ЈЁМоёЯОВЎўөНОВЎўИОәООВ¶ИЈ©ЎЈ
ўЬ¶ФёГ·ҙУҰЈ¬ПВБРЛө·ЁХэИ·өДКЗ_________ЈЁМоСЎПоЧЦДёЈ©ЎЈ
A.ИфИЭЖчДЪЖшМеГЬ¶ИІ»ұдЈ¬ФтұнГч·ҙУҰҙпөҪЖҪәвЧҙМ¬
B.ИфИЭЖчДЪCl2әНNH3ОпЦКөДБҝЦ®ұИОӘ3ЎГ1Ј¬ФтұнГч·ҙУҰҙпөҪЖҪәвЧҙМ¬
C.·ҙУҰҙпөҪЖҪәвәуЈ¬ЖдЛыМхјюІ»ұдЈ¬ФЪФӯИЭЖчЦР°ҙ![]() =
=![]() јМРшідИлТ»¶ЁБҝ·ҙУҰОпЈ¬ҙпРВЖҪәвәуCl2өДЧӘ»ҜВКФцҙу
јМРшідИлТ»¶ЁБҝ·ҙУҰОпЈ¬ҙпРВЖҪәвәуCl2өДЧӘ»ҜВКФцҙу
D.·ҙУҰҙпөҪЖҪәвәуЈ¬ЖдЛыМхјюІ»ұдЈ¬јУИлТ»¶ЁБҝөДNC13Ј¬ЖҪәвҪ«ПтДж·ҙУҰ·ҪПтТЖ¶Ҝ
Ўҫҙр°ёЎҝ+46.2 kJЎӨmolЈӯ1 ![]()
![]() B 0.5MPa > < өНОВ AC
B 0.5MPa > < өНОВ AC
ЎҫҪвОцЎҝ
ўс.ТСЦӘHЎӘHјьөДјьДЬОӘ436kJЎӨmol-1Ј¬NЎӘHјьөДҪЎДЬОӘ391kJЎӨmol-1Ј¬N![]() NјьөДјьДЬКЗ945.6 kJЎӨmol-1Ј¬Фт·ҙУҰNH3(g)
NјьөДјьДЬКЗ945.6 kJЎӨmol-1Ј¬Фт·ҙУҰNH3(g)![]()
![]() N2(g)+
N2(g)+![]() H2(g)өДҰӨH=3ЎБ391kJ/mol -
H2(g)өДҰӨH=3ЎБ391kJ/mol -![]() 945.6 kJ/mol-
945.6 kJ/mol- ![]() 436kJ/mol=+46.2 kJ/molЈ»NH3(g)
436kJ/mol=+46.2 kJ/molЈ»NH3(g)![]()
![]() N2(g)+
N2(g)+![]() H2(g)өДЖҪәвіЈКэОӘK=
H2(g)өДЖҪәвіЈКэОӘK=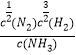 Ј¬N2(g)+3H2(g)
Ј¬N2(g)+3H2(g) ![]() 2NH3(g)өДЖҪәвіЈКэK1=
2NH3(g)өДЖҪәвіЈКэK1=![]() =
=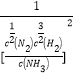 =
=![]() Ј»ўт.ЈЁ1Ј©ўЩ¶юВИ°ұФЪЦРРФЎўЛбРФ»·ҫіЦР»б·ўЙъЗҝБТЛ®ҪвЈ¬ЙъіЙҫЯУРЗҝЙұҫъЧчУГөДОпЦККЗҙОВИЛбЈ¬ЖдөзЧУКҪОӘ
Ј»ўт.ЈЁ1Ј©ўЩ¶юВИ°ұФЪЦРРФЎўЛбРФ»·ҫіЦР»б·ўЙъЗҝБТЛ®ҪвЈ¬ЙъіЙҫЯУРЗҝЙұҫъЧчУГөДОпЦККЗҙОВИЛбЈ¬ЖдөзЧУКҪОӘ![]() Ј»ўЪAЎўBЎўCИэөгЦРҙпөҪЖҪәвЧҙМ¬әуBөгHClЕЁ¶ИЧоҙуЈ¬ЛщТФCl2ЧӘ»ҜВКЧоҙ󣬹КЧӘ»ҜВКЧоёЯөДКЗBөгЈ»ЦЖұё¶юВИ°·өД·ҙУҰОӘ2Cl2(g)+NH3(g)
Ј»ўЪAЎўBЎўCИэөгЦРҙпөҪЖҪәвЧҙМ¬әуBөгHClЕЁ¶ИЧоҙуЈ¬ЛщТФCl2ЧӘ»ҜВКЧоҙ󣬹КЧӘ»ҜВКЧоёЯөДКЗBөгЈ»ЦЖұё¶юВИ°·өД·ҙУҰОӘ2Cl2(g)+NH3(g) ![]() NHCl2 (l)+2HCl(g)Ј¬ФЪәгОВМхјюПВЈ¬1 mol Cl2әНЧгБҝNH3·ўЙъ·ҙУҰФЪCөгКұЈ¬Cl2әНHClөДОпЦКөДБҝЕЁ¶ИПаөИЈ¬ҝЙЦӘҙЛКұ·ҙУҰМеПөЦРc(Cl2)=1molЈ¬c(HCl)=1molЈ¬c(NH3)=0.5molЈ¬ФтИэЦЦОпЦКөД·ЦС№·ЦұрОӘЈәP(Cl2)= P(HCl)=10MPaЎБ
NHCl2 (l)+2HCl(g)Ј¬ФЪәгОВМхјюПВЈ¬1 mol Cl2әНЧгБҝNH3·ўЙъ·ҙУҰФЪCөгКұЈ¬Cl2әНHClөДОпЦКөДБҝЕЁ¶ИПаөИЈ¬ҝЙЦӘҙЛКұ·ҙУҰМеПөЦРc(Cl2)=1molЈ¬c(HCl)=1molЈ¬c(NH3)=0.5molЈ¬ФтИэЦЦОпЦКөД·ЦС№·ЦұрОӘЈәP(Cl2)= P(HCl)=10MPaЎБ![]() =4MPaЈ¬P(NH3)=2MPaЈ¬CөгКұёГ·ҙУҰөДС№ЗҝЖҪәвіЈКэKp(C)=
=4MPaЈ¬P(NH3)=2MPaЈ¬CөгКұёГ·ҙУҰөДС№ЗҝЖҪәвіЈКэKp(C)=![]() =0.5MPaЈ»ЈЁ2Ј©ўЩТАҫЭұнЦРКэҫЭҝЙЦӘЈ¬ёГ·ҙУҰФЪTЎжКұ·ҙУҰЛЩВКҝмЈ¬ҙпөҪЖҪәвЧҙМ¬Кұn(Cl2) ФцҙуЈ¬ФтTЈҫ400Ј»ўЪЛжЧЕОВ¶ИЙэёЯЈ¬ЖҪәвПтДж·ҙУҰ·ҪПтТЖ¶ҜЈ¬ЛөГчёГ·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬span>ҰӨH<0Ј»ўЫёГ·ҙУҰДЬЧФ·ўҪшРРЈ¬ФтұШРлҰӨG=ҰӨH-TҰӨS<0Ј¬Тт·ҙУҰОӘЖшМеМе»эЛхРЎөД·ЕИИ·ҙУҰЈ¬№КОӘмШјхөД·ҙУҰЈ¬ҰӨG=ҰӨH-TҰӨS<0Ј¬ұШРлФЪөНОВМхјюПВЈ»ўЬAЈ®·ҙУҰЗ°әуЖшМеЦКБҝұд»ҜЈ¬ЖшМеМе»эІ»ұдЈ¬ИфИЭЖчДЪЖшМеГЬ¶ИІ»ұдЈ¬ФтұнГч·ҙУҰҙпөҪЖҪәвЧҙМ¬Ј¬СЎПоAХэИ·Ј»BЈ®ПтИЭ»эҫщОӘ1LөДјЧЎўТТБҪёцәгОВЈЁ·ҙУҰОВ¶И·ЦұрОӘ400ЎжЎўTЎжЈ©ИЭЖчЦР·ЦұрјУИл2mol C12әН2mol NH3Ј¬·ҙУҰҪшРРәуЈ¬ИЭЖчДЪОЮ·ЁҙпөҪCl2әНNH3ОпЦКөДБҝЦ®ұИОӘ3ЎГ1Ј¬СЎПоBҙнОуЈ»C.·ҙУҰҙпөҪЖҪәвәуЈ¬ЖдЛыМхјюІ»ұдЈ¬ФЪФӯИЭЖчЦР°ҙ
=0.5MPaЈ»ЈЁ2Ј©ўЩТАҫЭұнЦРКэҫЭҝЙЦӘЈ¬ёГ·ҙУҰФЪTЎжКұ·ҙУҰЛЩВКҝмЈ¬ҙпөҪЖҪәвЧҙМ¬Кұn(Cl2) ФцҙуЈ¬ФтTЈҫ400Ј»ўЪЛжЧЕОВ¶ИЙэёЯЈ¬ЖҪәвПтДж·ҙУҰ·ҪПтТЖ¶ҜЈ¬ЛөГчёГ·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬span>ҰӨH<0Ј»ўЫёГ·ҙУҰДЬЧФ·ўҪшРРЈ¬ФтұШРлҰӨG=ҰӨH-TҰӨS<0Ј¬Тт·ҙУҰОӘЖшМеМе»эЛхРЎөД·ЕИИ·ҙУҰЈ¬№КОӘмШјхөД·ҙУҰЈ¬ҰӨG=ҰӨH-TҰӨS<0Ј¬ұШРлФЪөНОВМхјюПВЈ»ўЬAЈ®·ҙУҰЗ°әуЖшМеЦКБҝұд»ҜЈ¬ЖшМеМе»эІ»ұдЈ¬ИфИЭЖчДЪЖшМеГЬ¶ИІ»ұдЈ¬ФтұнГч·ҙУҰҙпөҪЖҪәвЧҙМ¬Ј¬СЎПоAХэИ·Ј»BЈ®ПтИЭ»эҫщОӘ1LөДјЧЎўТТБҪёцәгОВЈЁ·ҙУҰОВ¶И·ЦұрОӘ400ЎжЎўTЎжЈ©ИЭЖчЦР·ЦұрјУИл2mol C12әН2mol NH3Ј¬·ҙУҰҪшРРәуЈ¬ИЭЖчДЪОЮ·ЁҙпөҪCl2әНNH3ОпЦКөДБҝЦ®ұИОӘ3ЎГ1Ј¬СЎПоBҙнОуЈ»C.·ҙУҰҙпөҪЖҪәвәуЈ¬ЖдЛыМхјюІ»ұдЈ¬ФЪФӯИЭЖчЦР°ҙ![]() =
=![]() јМРшідИлТ»¶ЁБҝ·ҙУҰОпЈ¬әгИЭМхјю°ҙұИАэФцјУ·ҙУҰОпЈ¬ПаөұУЪФцҙуС№ЗҝЈ¬ЖҪәвПтЖшМеМе»эЛхРЎөДХэ·ҙУҰ·ҪПтТЖ¶ҜЈ¬ФтҙпРВЖҪәвәуCl2өДЧӘ»ҜВКФцҙуЈ¬СЎПоCХэИ·Ј»D.·ҙУҰҙпөҪЖҪәвәуЈ¬ЖдЛыМхјюІ»ұдЈ¬јУИлТ»¶ЁБҝөДNC13Ј¬ЕЁ¶ИІ»ұдЈ¬ЖҪәвІ»ТЖ¶ҜЈ¬СЎПоDҙнОуЎЈҙр°ёСЎACЎЈ
јМРшідИлТ»¶ЁБҝ·ҙУҰОпЈ¬әгИЭМхјю°ҙұИАэФцјУ·ҙУҰОпЈ¬ПаөұУЪФцҙуС№ЗҝЈ¬ЖҪәвПтЖшМеМе»эЛхРЎөДХэ·ҙУҰ·ҪПтТЖ¶ҜЈ¬ФтҙпРВЖҪәвәуCl2өДЧӘ»ҜВКФцҙуЈ¬СЎПоCХэИ·Ј»D.·ҙУҰҙпөҪЖҪәвәуЈ¬ЖдЛыМхјюІ»ұдЈ¬јУИлТ»¶ЁБҝөДNC13Ј¬ЕЁ¶ИІ»ұдЈ¬ЖҪәвІ»ТЖ¶ҜЈ¬СЎПоDҙнОуЎЈҙр°ёСЎACЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіС§П°РЎЧйУыҙУ№ӨТө·П·°ҙЯ»ҜјБЦР»ШКХV2O5Ј¬НЁ№э·ЦОцЦӘёГ·П·°ҙЯ»ҜјБөДЦчТӘіЙ·ЦИзПВұн:
ОпЦК | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
ЦКБҝ·ЦКэ/% | 2.2Ў«29 | 2.8Ў«3.1 | 22Ў«28 | 60Ў«65 | 1Ў«2 | <1 |
ЛыГЗНЁ№эІйФДЧКБПХТөҪТ»ЦЦ·П·°ҙЯ»ҜјБөД»ШКХ№ӨТХБчіМВ·ПЯИзПВ:
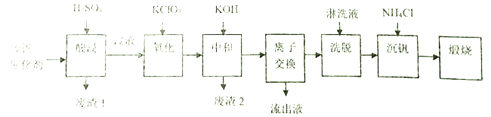
»ШҙрПВБРОКМв:
ЈЁ1Ј©Ў°ЛбҪюЎұКұV2O5ЧӘ»ҜОӘVO2+Ј¬V2O4ЧӘіЙVO2+ЎЈФтЎ°·ПФь1ЎұөДЦчТӘіЙ·ЦКЗ_____________ЎЈ
ЈЁ2Ј©Ў°Сх»ҜЎұөДДҝөДКЗК№VO2+ұдОӘVO2+Ј¬РҙіцёГ·ҙУҰөДАлЧУ·ҪіМКҪ________________________ЎЈ
ЈЁ3Ј©Ў°ЦРәНЎұЧчУГЦ®Т»КЗК№·°ТФV4O124-РОКҪҙжФЪУЪИЬТәЦРЈ¬ФтЎ°·ПФь2ЎұөДіЙ·ЦУР__________(УГ»ҜС§КҪұнКҫ)ЎЈ
ЈЁ4Ј©Ў°АлЧУҪ»»»ЎұәНЎ°ПҙНСЎұҝЙјтөҘұнКҫОӘ:4ROH+ V4O124- ![]() R4V4O12+4OH-(ROHОӘҸҠјоРФТхАлЧУҪ»»»КчЦ¬)ЎЈЎ°БчіцТәЎұЦРСфАлЧУЧо¶аөДКЗ_______________Ј»ОӘБЛМбёЯПҙНСР§ВКЈ¬БЬПҙТәУҰёГіК______РФ(МоЎ°ЛбЎұЎўЎ°јоЎ°»тЎ°ЦРЎұ)ЎЈ
R4V4O12+4OH-(ROHОӘҸҠјоРФТхАлЧУҪ»»»КчЦ¬)ЎЈЎ°БчіцТәЎұЦРСфАлЧУЧо¶аөДКЗ_______________Ј»ОӘБЛМбёЯПҙНСР§ВКЈ¬БЬПҙТәУҰёГіК______РФ(МоЎ°ЛбЎұЎўЎ°јоЎ°»тЎ°ЦРЎұ)ЎЈ
ЈЁ5Ј©Ў°іБ·°ЎұөГөҪЖ«·°Лбп§(NH4VO3)іБөнЈ¬РҙіцөГөҪіБ¶ЁөД»ҜС§·ҪіМКҪ__________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪ«ұкЧјЧҙҝцПВ2.24 L CO2»әВэНЁИл1 L 0.15 molЎӨLЈӯ1өДNaOHИЬТәЦРЈ¬ЖшМеұ»ід·ЦОьКХЈ¬ПВБР№ШПөІ»ХэИ·өДКЗ(ЎЎЎЎ)
A. »мәПИЬТәИЬЦКОӘNaHCO3әНNa2CO3
B. c(NaЈ«)Ј«c(HЈ«)ЈҪc(OHЈӯ)Ј«c(HCO3-)Ј«2c(CO32-)
C. c(NaЈ«)>c(CO32-)>c(HCO3-)>c(OHЈӯ)>c(HЈ«)
D. јУИИХфёЙЛщөГ»мәПИЬТәЈ¬ЧоЦХөГөҪNa2CO3№ММе
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ2017Дк6ФВ5ИХКЗКАҪз»·ҫіИХЈ¬ЦР№ъЦчМвОӘЎ°ВМЛ®ЗаЙҪҫНКЗҪрЙҪТшЙҪЎұөӘөДСх»ҜОпөДОЫИҫИХЗчСПЦШЈ¬ДіЖуТөҙҰАнёГОЫИҫОпөДФӯАнЙијЖОӘИјБПөзіШИзУТНјЛщКҫЎЈФЪҙҰАн№эіМЦРКҜД«ўсөзј«ЙПЙъіЙСх»ҜОпYЈ¬YҝЙСӯ»·К№УГЎЈПВБРЛө·ЁІ»ХэИ·өДКЗ

A. ёГөзіШ·ЕөзКұөзЧУБч¶ҜөД·ҪПтКЗЈәКҜД«ўсөзј«ЎъёәФШЎъКҜД«ўтөзј«ЎъИЫИЪKNO3ЎъКҜД«ўсөзј«
B. КҜД«ўтёҪҪь·ўЙъөД·ҙУҰЈәO2+4e-+2N2O5=4NO3-
C. O2ФЪКҜД«ўтёҪҪь·ўЙъ»№Фӯ·ҙУҰЈ¬YОӘN2O5
D. ПаН¬МхјюПВЈ¬·Еөз№эіМЦРПыәДөДNO2әНO2өДМе»эұИОӘ4ЎГ1
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЎ°ТЎТЎұщЎұКЗТ»ЦЦјҙУГјҙАдөДТыБПЎЈОьКіКұҪ«ТыБП№ЮёфАлІгЦРөД»ҜС§ОпЦКәНЛ®»мәПәуТЎ¶Ҝјҙ»бЦЖАдЎЈёГ»ҜС§ОпЦККЗ
A.ВИ»ҜДЖB.№ММеПхЛбјШC.ЙъКҜ»ТD.№ММеЗвСх»ҜДЖ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР№ШУЪФӯөзіШөДРрКцЦРЈ¬ҙнОуөДКЗ
A.№№іЙФӯөзіШөДХэј«әНёәј«ұШРлКЗБҪЦЦІ»Н¬өДҪрКф
B.ФӯөзіШКЗҪ«»ҜС§ДЬЧӘ»ҜОӘөзДЬөДЧ°ЦГ
C.ФЪФӯөзіШЦРЈ¬өзЧУБчіцөДТ»ј¶КЗёәј«Ј¬·ўЙъСх»Ҝ·ҙУҰ
D.ФӯөзіШ·ЕөзКұЈ¬өзБчөД·ҪПтКЗҙУёәј«өҪХэј«
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝКөСйКТУыҝмЛЩЦЖИЎH2Ј¬УҰСЎУГХэИ·өДҙлК©КЗ
A.ҙҝРҝУлПЎБтЛб·ҙУҰB.ҙЦРҝёъПЎБтЛб·ҙУҰ
C.ҙЦРҝёъПхЛб·ҙУҰD.Ҫ«ҪюЕЭ№эCuSO4ИЬТәөДZnёъПЎБтЛб·ҙУҰ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ№иөҘЦКј°Жд»ҜәПОпУҰУГ·¶О§әЬ№гЈ¬Зл»ШҙрПВБРОКМвЈә
ЦЖұё№и°лөјМеІДБПұШРлПИөГөҪёЯҙҝ№иЈ¬ИэВИјЧ№иНй(SiHCl3)»№Фӯ·ЁКЗөұЗ°ЦЖұёёЯҙҝ№иөДЦчТӘ·Ҫ·ЁЈ¬ЙъІъ№эіМКҫТвНјИзПВЈә
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)РҙіцУЙҙҝSiHCl3ЦЖұёёЯҙҝ№иөД»ҜС§·ҙУҰ·ҪіМКҪ___________Ј»
(2)ХыёцЦЖұё№эіМұШРлСПёсҝШЦЖОЮЛ®ОЮСхЈ¬SiHCl3УцЛ®ҫзБТ·ҙУҰЙъіЙH2SiO3Ј¬HClәНБнТ»ЦЦОпЦКЈ¬РҙіцЕдЖҪөД»ҜС§·ҙУҰ·ҪіМКҪ___________Ј» H2»№ФӯSiHCl3№эіМЦРИф»мИлO2Ј¬ҝЙДЬТэЖрөДәу№ыКЗ_________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝАыУГИзПВКөСйМҪҫҝМъ¶ӨФЪІ»Н¬ИЬТәЦРөДОьСхёҜКҙЎЈ
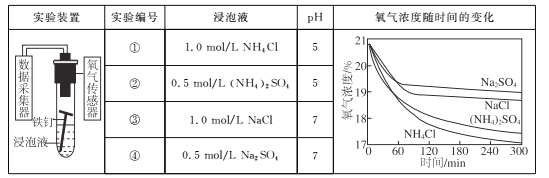
ПВБРЛө·ЁІ»ХэИ·өДКЗ
A. ЙПКцХэј«·ҙУҰҫщОӘO2+4e-+2H2O=4OH-
B. ФЪІ»Н¬ИЬТәЦРЈ¬ClКЗУ°ПмОьСхёҜКҙЛЩВКөДЦчТӘТтЛШ
C. ПтКөСйўЬЦРјУИлЙЩБҝ(NH4)2SO4№ММеЈ¬ОьСхёҜКҙЛЩВКјУҝм
D. ФЪ300 minДЪЈ¬Мъ¶ӨөДЖҪҫщОьСхёҜКҙЛЩВКЛбРФИЬТәҙуУЪЦРРФИЬТә
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com