


科目:高中化学 来源: 题型:
| A、112kJ |
| B、56kJ |
| C、小于56kJ |
| D、-56kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
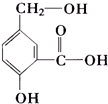 烃及烃的含氧衍生物在有机化学中占有举足轻重的地位.请根据相关知识和信息回答下列有关问题:
烃及烃的含氧衍生物在有机化学中占有举足轻重的地位.请根据相关知识和信息回答下列有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
| 密度/g?cm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |

查看答案和解析>>
科目:高中化学 来源: 题型:
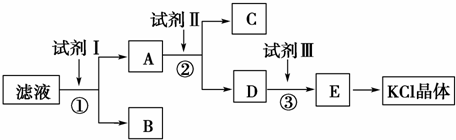
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、SiO2是氧化剂,C为还原剂 |
| B、碳的还原性比硅强 |
| C、氧化剂和还原剂的物质的量之比为2:1 |
| D、1mol SiO2参与反应时,转移电子4mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com