
【题目】根据图填空:

反应物是________;生成物是________。在2 min内A、B、C三者的反应速率值分别是____________、____________、____________,该反应的化学方程式是______________________。
【答案】A、B C 3mol·L-1·min-1 2mol·L-1·min-1 3mol·L-1·min-1 3A+2B![]() 3C
3C
【解析】
分析题给c-t图,根据A、B、C的曲线变化趋势可判断出反应物和生成物。分析图中相同时间内A、B、C的浓度变化值,可计算出三者的反应速率值,进而可推导出反应的化学方程式。
分析题给c-t图,A、B的浓度随着时间的进行逐渐减小,在2min时保持不变,C的起始浓度为0,随着时间的进行逐渐增大,在2min时保持不变,说明A、B为反应物,C为生成物。
由图可知![]() ,
,![]() ,
,![]() ,根据反应速率的定义,
,根据反应速率的定义,![]() ,同理可知:
,同理可知:![]() ,
,![]() 。
。
由同一反应中各物质的反应速率之比等于相应物质的化学计量数之比,可知A、B、C的化学计量数之比=![]() ,则反应方程式为:3A+2B
,则反应方程式为:3A+2B![]() 3C。
3C。
答案为:A、B;C;3mol·L-1·min-1;2mol·L-1·min-1;3mol·L-1·min-1;3A+2B![]() 3C。
3C。


科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A.将混合气体中的氨液化有利于合成氨反应
B.对CO(g)+NO2(g)![]() CO2(g)+NO(g)平衡体系增大压强可使其颜色变深
CO2(g)+NO(g)平衡体系增大压强可使其颜色变深
C.常温下,将1mLpH=3的醋酸溶液加水稀释到100mL,测得其pH<5
D.实验室中常用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成下列问题:
(1)写出由乙醇制取乙二酸的反应方程式_________。
(2)相对分子质量为72且沸点最低的烷烃的习惯名称是__________。
(3)用系统命名法命名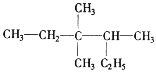 _____。
_____。
(4)某烯烃分子式为C6H12,其同分异构体中主链为4个碳原子的有______种。
(5)合成高聚物![]() 其单体的键线式_______。
其单体的键线式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断
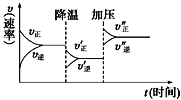
A.正反应是放热反应B.D可能是气体
C.逆反应是放热反应D.A、B、C、D均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和__。
(2)为检验分解产物的成份,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
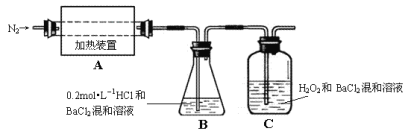
①A中固体充分加热较长时间后,通入氮气,目的是___。
②为验证A中残留物是否含有FeO,需要选用的试剂有___。
A.KSCN溶液 B.浓盐酸 C.KMnO4溶液 D.稀硫酸
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有__气体生成,若含有该气体,观察到的现象为__。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为amol,C中沉淀物质的量为bmol,则b__a(填“大于”、“小于”或“等于”)
⑤现欲将B中溶液准确稀释至100.00mL,应将锥形瓶中的溶液转移入__(填仪器名称)定容。
⑥实验中,观察到C中有白色沉淀生成,则C中发生的反应为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)53克Na2CO3的物质的量是________,所含Na+和CO32-的物质的量各是_____________,
(2)在标准状况下,测得1.32 g某气体的体积为0.672 L。则此气体的摩尔质量_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究 CO2的利用对促进低碳社会的构建具有重要意义。
(1)一定条件下,在 CO2 与足量碳反应所得平衡体系中加入 H2 和适当催化剂,有下列反应发生:CO(g)+3H2(g) ![]() CH4(g)+H2O(g) H1=-206.2kJ/mol ;CO(g)+H2O(g)
CH4(g)+H2O(g) H1=-206.2kJ/mol ;CO(g)+H2O(g)![]() CO2(g)+H2(g)H2若 CO2 和 H2 反应生成 0.1mol CH4(g)和一定量的 H2O(g), 整个过程中放出的热量为 16.5kJ, 则△H2=__________。
CO2(g)+H2(g)H2若 CO2 和 H2 反应生成 0.1mol CH4(g)和一定量的 H2O(g), 整个过程中放出的热量为 16.5kJ, 则△H2=__________。
(2)为研究 CO2 与 CO 之间的转化。让一定量的 CO2 与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)![]() 2CO(g) H。 测得压强、温度对 CO 的体积分数(φ(CO)%)的影响如图所示:
2CO(g) H。 测得压强、温度对 CO 的体积分数(φ(CO)%)的影响如图所示:
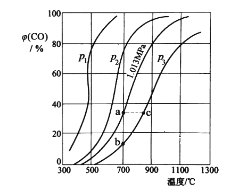
回答下列问题:
① p1、p2、p3 的大小关系是__________,图中 a、b、c 三点对应的平衡常数大小关系是__________(用 Ka、Kb、Kc 表示)。
② 900 ℃、1.013 MPa 时,1 mol CO2 与足量碳反应达平衡后容器的体积为VL,CO2 的转化率为__________,(保留一位小数)该反应的平衡常数 K=__________。
③将②中平衡体系温度降至 640 ℃,压强降至 0.1013 MPa,重新达到平衡后 CO2 的体积分数为 50%。条件改变时,正反应和逆反应速率如何变化?__________,二者之间有何关系?__________。
(3)CO2 可用于工业制备草酸锌,其原理如下图所示(电解液不参加反应),Zn 电极是__________极。已知在 Pb 电极区得到 ZnC2O4,则 Pb 电极上的电极反应式为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向0.1 mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是
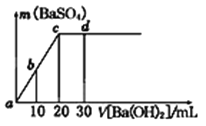
A.溶液的pH:a<b<c<d
B.溶液的导电能力:a>b>d>c
C.c、d溶液呈碱性
D.a、b溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为HOOC![]() CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是
A. 苹果酸中能发生酯化反应的官能团有2种
B. 1mol苹果酸可与3mol NaOH发生中和反应
C. 1mol苹果酸与足量金属Na反应生成生成1mol H2
D. HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com