
【题目】相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g)![]() 2SO3(g);
2SO3(g); ![]() 。实验测得起始、平衡时的有关数据如下表:下列叙述正确的是 ( )
。实验测得起始、平衡时的有关数据如下表:下列叙述正确的是 ( )
容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
SO2 | O2 | SO3 | Ar | ||
甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
A. 若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1<-197 kJ·mol-1
B. Q1=Q2=Q3=197 kJ
C. 甲、乙、丙3个容器中反应的平衡常数不相等
D. 达到平衡时,丙容器中SO2的体积分数最大
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行Fe2+与Fe3+转化实验:向FeCl2溶液中加入少量KSCN溶液,溶液无明显变化,再加入少量双氧水,溶液变红,继续滴加至过量,发现溶液红色褪去,同时有气泡生成.他们针对此异常现象展开探究,请回答有关问题:
(1)该小组对于产生气体的原因有两种猜测:
猜测一:__________________________________________。
猜测二:红色褪去可能是SCN-被H2O2氧化,同时产生的气体中可能含有氮气、二氧化碳、二氧化硫。
(2)化学小组针对猜测二设计下面的实验来验证气体成分:
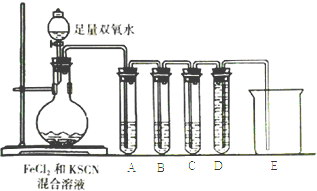
①试管A中盛放品红溶液,若实验中品红溶液褪色,证明气体中含有____________;
②试管B中的溶液是酸性高锰酸钾溶液,其目的是________________,预期试管B中的现象是________________________________。
③试管C中盛有澄清石灰水,目的是___________________;试管D和烧杯的作用是______________。④以上实验证明SCN-能被H2O2氧化.请写出该反应的离子方程式:___________________________________。
(3)根据题目信息及以上实验推断,Fe2+和SCN-中还原性较强的是_______,理由是_________。
(4)有人认为SCN-的氧化产物可能还有硫酸根离子,请设计一个简单实验证明该假设是否正确_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图中,甲烧杯中盛有100 mL 0.50 mol/L AgNO3溶液,乙烧杯中盛有100 mL 0.25 mol/L CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极增重2.7 g,则:

(1)E为电源的__________极,D为电解池的__________极。
(2)A极的电极反应式为__________________,析出物质______ mol。
(3)B极的电极反应式为__________________,析出气体__________ mL(标准状况)。
(4)C极的电极反应式为___________________,析出物质__________ mol。
(5)D极的电极反应式为__________________,析出气体_________ mL(标准状况)。
(6)甲烧杯中滴入石蕊试液,__________(选填“A”、“B”)极附近变红,如果继续电解,在甲烧杯中最终得到__________溶液(写溶质的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用vA、vB、vC表示,且vA、vB、vC之间有如下所示关系:vB=3vA、3vC=2vB.则此反应可表示为( )
A.2A+3B=2C
B.A+3B=2C
C.3A+B=2C
D.3A+B=C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化碘ICl3遇水会产生大量的腐蚀性白色烟雾,有强烈的催泪作用。该反应相当于盐类的水解反应。若生成物之一是HCl,则另一种产物是 ( )
A. HIO3 B. HIO2 C. HIO D. ICl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com