
【题目】氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl、NHCl2和NCl3)。
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质的结构式为________,二氯胺与水反应的化学方程式为_____________。将0.01 mol NCl3通入100 mL 0.5 mol/L Na2SO3溶液中,转移电子的物质的量为_______mol。
(2)已知部分化学键的键能和化学反应的能量变化如下表和下图所示。
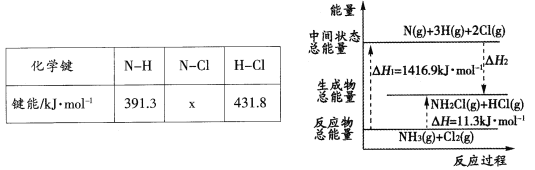
则反应过程中的△H2=____kJ·mol-1,表中的x=_____。
(3)在密闭容器中反应NH3(g)+Cl2(g)![]() NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随![]() 的变化如下图所示。
的变化如下图所示。
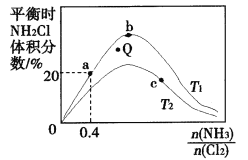
①a、b、c三点对应平衡常数的大小关系是(分别用Ka、Kb、Kc表示)_________。b点时,该反应的平衡常数为________;
②T2℃,Q点对应的速率:![]() __________
__________![]() (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
③在氨氯比一定时,提高NH3的转化率的方法是__________(任写1种);
④若产物都是气体,实验测得NH2C1的体积分数始终比理论值低,原因可能是______________。
【答案】H-O-C1 NHCl2+2H2O=NH3+2HC1O 0.06 -1405.6 191.2 Ka=Kb>Kc ![]() < 升温或及时分离出产物NH2Cl 有副反应,还可能生成NHCl2、NC13、N2等
< 升温或及时分离出产物NH2Cl 有副反应,还可能生成NHCl2、NC13、N2等
【解析】
(1)氯胺与H2O反应产生NH3和HClO;二氯胺与水反应产生NH3和两分子的HClO;NCl3与H2O反应产生NH3和HClO,HClO将Na2SO3氧化为Na2SO4,HClO被还原为HCl,HCl与NH3结合形成NH4Cl,根据反应前后元素化合价的变化分析电子转移情况;
(2)根据反应热与反应物、生成物的活化能大小分析,根据△H=反应物总键能-生成物总键能分析;
(3)①平衡常数只与温度有关,温度不变,平衡常数不变,当n(NH3):n(Cl2)=0.4时结合NH2Cl的体积分数为20%,通过物质平衡转化关系计算出各物质平衡量,代入平衡常数公式计算;
②在T2温度下,过Q点作垂线,此时Q点对应NH2Cl的体积分数偏高,联系平衡移动即可得出正反应速率与逆反应速率的大小;
③提高NH3的转化率,则平衡应该正向移动,联系平衡移动的相关知识解答;
④NH2Cl的体积分数始终比理论值低,可能的原因很多,可从副反应或者有其他杂质产生方面考虑回答即可。
(1)氯胺与H2O反应产生NH3和HClO,反应产生的HClO具有强的氧化性,其结构式为H-O-Cl;二氯胺与水反应产生NH3和两分子的HClO,反应方程式为:NHCl2+2H2O=NH3+2HC1O;NCl3与H2O反应产生NH3和HClO,HClO将Na2SO3氧化为Na2SO4,HClO被还原为HCl,HCl与NH3结合形成NH4Cl,1 mol NCl3反应产生3 mol HClO,氧化Na2SO3产生Na2SO4时转移6 mol电子,则0.01 mol NCl3发生反应转移0.06 mol电子;
(2)由于从能量数值看△H1=△H+△H2,所以△H2=△H1-△H=1416.9 kJ/mol-11.3 kJ/mol=1405.6 kJ/mol,物质由能量高的状态转化为能量低的状态,反应放出热量,则反应过程中的△H2=-1405.6 kJ/mol;由△H=反应物总键能-生成物总键能,得:1416.9 kJ/mol-(2×391.3 kJ/mol+x kJ/mol+431.8 kJ/mol)=+11.3kJ/mol,解得x=191.2 kJ/mol;
(3)①由于a、b两点温度相同,则Ka=Kb,由于该反应的正反应为吸热反应,当![]() 为定值时,T2下NH2Cl的体积分数更小,说明T2下平衡逆向移动,则Kc变小,所以a、b、c三点化学平衡常数的关系是:Ka=Kb>Kc;当
为定值时,T2下NH2Cl的体积分数更小,说明T2下平衡逆向移动,则Kc变小,所以a、b、c三点化学平衡常数的关系是:Ka=Kb>Kc;当![]() =0.4时,假设容器体积为V L,起始量n(NH3)=0.4 mol,n(Cl2)=1 mol,NH3变化量为x mol,则平衡时n(NH3)=(0.4-x) mol,n(Cl2)=(1-x) mol,n(NH2Cl)=n(HCl)=x mol,同温同压下气体的体积比等于气体的物质的量的比,则:
=0.4时,假设容器体积为V L,起始量n(NH3)=0.4 mol,n(Cl2)=1 mol,NH3变化量为x mol,则平衡时n(NH3)=(0.4-x) mol,n(Cl2)=(1-x) mol,n(NH2Cl)=n(HCl)=x mol,同温同压下气体的体积比等于气体的物质的量的比,则:![]() ×100%=20%,解得x=0.28 mol,则该反应的平衡常数Kb=
×100%=20%,解得x=0.28 mol,则该反应的平衡常数Kb=![]() ;
;
②在T2温度下,Q点NH2Cl的体积分数偏高,平衡将向着使NH2Cl的体积分数下降的方向移动,所以Q点平衡逆移,v正<v逆;
③在氨氯比一定时,由(2)知△H>0,升高温度,或及时分离出产物NHCl2,都会使平衡正向移动,NH3的转化率升高;
④NH2Cl的体积分数始终比理论值低,可能是:有副反应,还可能生成NHCl2、NCl3、N2。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】将足量X气体通入Y溶液中,实验结果与预测的现象一致的组合是
X气体 | Y溶液 | 预测的现象 |
| |
① | CO2 | 饱和Na2CO3溶液 | 白色沉淀析出 | |
② | SO2 | Ba(NO3)2溶液 | 白色沉淀析出 | |
③ | Cl2 | AgNO3溶液 | 白色沉淀析出 | |
④ | NH3 | AlCl3溶液 | 白色沉淀析出 |
A. 只有①②③ B. 只有①②④ C. 只有①③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于100mL0.5 mol·L-1Na2CO3溶液,下列有关说法正确的是( )
A.实验室配制该溶液,定容时仰视刻线,所配制溶液浓度偏大
B.该溶液稀释10倍后,c(Na+)=0.05 mol·L-1
C.从该溶液中取出10mL,所取溶液中溶质的物质的量浓度为0.05 mol·L-1
D.该溶液中含有Na2CO3的质量为5.3g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(C1O2)是易溶于水且不与水反应的黄绿色气体,沸点为11℃。某小组在实验室中制备C1O2的装置如下:[已知:SO2+2NaC1O3+H2SO4=2C1O2+2NaHSO4]
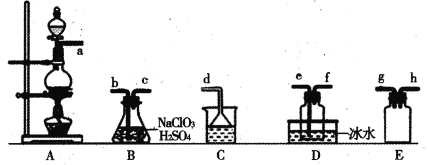
下列说法正确的是
A.连接装置时,导管口a应接h或g,导管口c应接e
B.装置C中装的是饱和食盐水,导管口a通过的气体为SO2
C.装置D放冰水的目的是液化SO2,防止污染环境
D.可选用装置A,用1 mol·L-1盐酸与MnO2反应制取Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学兴趣小组查阅资料得知,反应温度不同,氢气还原氧化铜的产物就不同,可能是Cu或Cu2O,Cu和Cu2O均为不溶于水的红色固体,但Cu2O能与稀硫酸发生反应:Cu2O+H2SO4=CuSO4+Cu+H2O。为探究反应后的红色固体的成分,他们提出了以下假设:
假设一:红色固体只有Cu
假设二:红色固体只有Cu2O
假设三:红色固体中有Cu和Cu2O
下列判断正确的是
A.取少量红色固体,加入足量的稀硫酸,若溶液无明显现象,则假设一和二都成立
B.少量红色固体与足量稀硫酸反应,若溶液呈蓝色且仍有红色固体,则只有假设三成立
C.若将7.2克红色固体通入足量的H2还原,最后得到固体6.4克,则假设二成立
D.实验室可用向新制Cu(OH)2悬浊液(碱性)中加入葡萄糖后加热,来制取Cu2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据如图所示情况,判断下列说法中正确的是____。
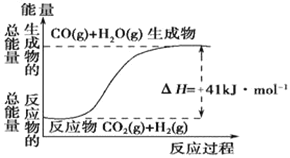
A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) △H=41kJmol﹣1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为△H2,则△H2>△H
(2)25℃、101kPa下,已知1g氢气完全燃烧生成液态水时放出142.9kJ的热量,表示氢气燃烧热的热化学方程式是_____。
(3)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4 的反应焓变为:__(用含△H1、△H2、△H3的式子表示)。
(4)已知反应2HI(g)H2(g)+I2(g)的△H=+11kJmol﹣1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如下:
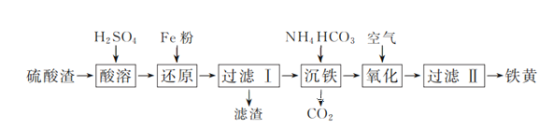
(1)“酸溶”中加快溶解的方法为____(写出一种)。
(2)“还原”过程中的离子方程式为_______。
(3)①“沉铁”过程中生成Fe(OH)2的化学方程式为_______。②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中c(Ca2+)/c(Fe2+)=________。[已知Ksp(CaCO3)=2.8×10-9,Ksp(FeCO3)=2×10-11]
(4)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是_________。
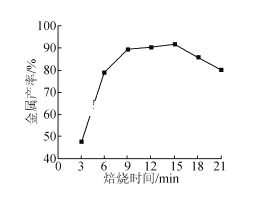
(5)焦炭还原硫酸渣炼铁能充分利用铁资源,在1225℃、n(C)/n(O)=1.2时,焙烧时间与金属产率的关系如图,时间超过15min金属产率下降的原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)。
下列说法正确的是
A. 该固体中一定含有NH4+、CO32-、SO42-、Na+ B. 该固体中一定没有Cu2+、Cl-、Na+
C. 该固体中只含有NH4+、CO32-、SO42-、Cl- D. 根据以上实验,无法确定该固体中有Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中a曲线表示一定条件下的可逆反应:X(g)+Y(g)![]() 2Z(g)+W(g);△H=QkJ/mol的反应过程。若使a曲线变为b曲线,可采取的措施是( )
2Z(g)+W(g);△H=QkJ/mol的反应过程。若使a曲线变为b曲线,可采取的措施是( )
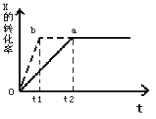
A. 降低温度B. 增大Y的浓度
C. 加入催化剂D. 增大体系压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com