
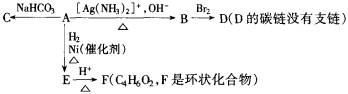
(1)化合物A含有的官能团是_______________.
(2)1 mol A与2 mol H2反应生成1 mol E,其反应方程式是____________________.
(3)与A具有相同官能团的A的同分异构体的结构简式是_______________________.
(4)B在酸性条件下与Br2反应得到D,D的结构简式是________________________.
(5)F的结构简式是_____________由E生成F的反应类型是_______________________.
| (1)碳碳双键、醛基、羧基
(2)OHC—CH==CH—COOH+2H2 (3) (4) (5) 解析:综合A能与NaHCO3溶液反应,能发生银镜反应且生成的B又与Br2反应生成无支链的D及第(2)问所述的1 mol A与2 mol H2反应生成1 mol E等信息,可知A中含—COOH、—CHO、C==C,并且是直链分子,故A的结构简式为OHC—CH==CH—COOH;B是A发生银镜反应的产物,其结构简式为:HOOC—CH==CH—COOH;E是A发生加成反应的产物,其结构简式为HO—CH2—CH2—CH2—COOH.A的同分异构体只可能是双键位置发生变化(—CHO和—COOH必在碳链的端点),E的分子内脱水方式是唯一的,即—OH和—COOH先水成环酯,故F的结构简式为
|


科目:高中化学 来源: 题型:

| ||
| △ |
| ||
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:

| Ni |
| △ |
| Ni |
| △ |
| H2O |
| △ |
| H2O |
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:
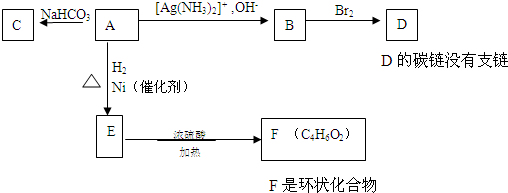
| 催化剂 |
| △ |
| 催化剂 |
| △ |




查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 4 |
| O | 2- 3 |
| O | 2- 3 |
| O | 2- 3 |
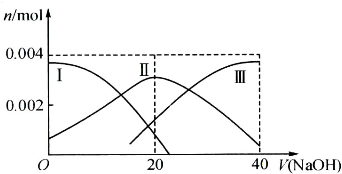
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com