

 +H2O(R、R′为H或烃基)
+H2O(R、R′为H或烃基)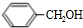 ;C中含有的官能团碳碳双键和醛基(写名称).
;C中含有的官能团碳碳双键和醛基(写名称). .
. .
.


分析 甲基环己烷与氯气在光照条件下发生取代反应生成E,E发生水解反应生成F,F连续两次氧化反应得到G,则F中含有-CH2OH,故E为 ,F为
,F为 ,G为
,G为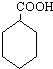 .D与G反应得到芳香酯,则D中含有苯环,A发生催化氧化得到B,B与乙醛发生信息中反应得到C,结合C的分子式可知,A为
.D与G反应得到芳香酯,则D中含有苯环,A发生催化氧化得到B,B与乙醛发生信息中反应得到C,结合C的分子式可知,A为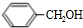 ,B为
,B为 ,则C为
,则C为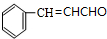 ,D为
,D为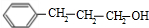 ,故H为
,故H为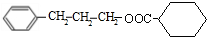 .
.
(5)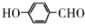 与乙醛在碱性条件下反应得到
与乙醛在碱性条件下反应得到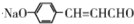 ,然后用银氨溶液氧化,最后酸化得到
,然后用银氨溶液氧化,最后酸化得到 ,
, 再与甲醇发生酯化得产品M.
再与甲醇发生酯化得产品M.
解答 解:甲基环己烷与氯气在光照条件下发生取代反应生成E,E发生水解反应生成F,F连续两次氧化反应得到G,则F中含有-CH2OH,故E为 ,F为
,F为 ,G为
,G为 .D与G反应得到芳香酯,则D中含有苯环,A发生催化氧化得到B,B与乙醛发生信息中反应得到C,结合C的分子式可知,A为
.D与G反应得到芳香酯,则D中含有苯环,A发生催化氧化得到B,B与乙醛发生信息中反应得到C,结合C的分子式可知,A为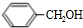 ,B为
,B为 ,则C为
,则C为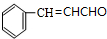 ,D为
,D为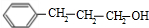 ,故H为
,故H为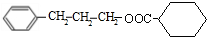 ,
,
(1)根据上面的分析可知,A为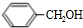 ,C为
,C为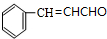 ,C中含有的官能团为碳碳双键和醛基,
,C中含有的官能团为碳碳双键和醛基,
故答案为: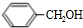 ;碳碳双键和醛基;
;碳碳双键和醛基;
(2)E→F的有机反应类型为取代反应,故答案为:取代反应;
(3)D与G反应生成H的化学方程式为 ,
,
故答案为: ;
;
(4)C为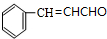 ,根据条件①能发生加聚反应,说明有碳碳双键,②能发生银镜反应,说明有醛基,③属于芳香族化合物,说明有苯环,则符合条件的C的同分异构体为苯环上连有-CH=CHCHO,有顺式和反式两种,或连有两个基团为-CH=CH2、-CHO,有邻间对三种,或为苯环上连有-C(=CH2)CHO,共有6种,其中核磁共振氢谱有五个吸收峰的同分异构体的结构简式为-
,根据条件①能发生加聚反应,说明有碳碳双键,②能发生银镜反应,说明有醛基,③属于芳香族化合物,说明有苯环,则符合条件的C的同分异构体为苯环上连有-CH=CHCHO,有顺式和反式两种,或连有两个基团为-CH=CH2、-CHO,有邻间对三种,或为苯环上连有-C(=CH2)CHO,共有6种,其中核磁共振氢谱有五个吸收峰的同分异构体的结构简式为- ,
,
故答案为:6; ;
;
(5) 与乙醛在碱性条件下反应得到
与乙醛在碱性条件下反应得到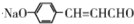 ,然后用银氨溶液氧化,最后酸化得到
,然后用银氨溶液氧化,最后酸化得到 ,
, 再与甲醇发生酯化得产品M,反应的合成路线为
再与甲醇发生酯化得产品M,反应的合成路线为 ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,注意根据反应条件、W的为芳香酯与甲基环己烷的结构条件下推断,熟练掌握官能团的性质与转化,较好地考查学生信息获取与知识迁移运用能力.


科目:高中化学 来源: 题型:选择题
| A. | 钠在常温下很容易被氧化 | B. | 钠在空气中燃烧生成Na2O | ||
| C. | 钠燃烧时发出黄色的火焰 | D. | 钠的密度比水小,熔点低于100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期 | B. | 第一周期 | C. | 第ⅤA族 | D. | 第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.7g | B. | 3.15g | C. | 4.35g | D. | 4.0g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
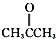 ③CH3CH2Br ④
③CH3CH2Br ④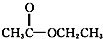 ⑤
⑤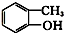
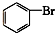 ⑦
⑦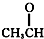 ⑧
⑧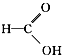 ⑨
⑨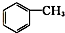 ⑩
⑩
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 相同质量的四块金属片组装成如下的两套装置,其中说法正确的是( )
相同质量的四块金属片组装成如下的两套装置,其中说法正确的是( )| 选项 | 评估项目 | 甲装置 | 乙装置 |
| A | 能量转化的主要形式 | 化学能转化为电能 | 无能量转化 |
| B | 金属片的质量 | 锌片减轻,铜片增重 | 锌片增重,铜片不变 |
| X | SO42-移动方向 | 移向锌片 | 移向锌片 |
| D | 锌片与铜片的质量相差12.9g时,转移电子的物质的量 | 转移0.2mol电子 | 转移25.8mol电子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com