
ҰңМвДүҰүҢьДкАөӘ¬ОнцІМмЖшіЙОҒОТ№ъ»Ғ±±µШЗшДЛЦБИ«№ъµД»·ңіОКМвЦ®Т»ҰӘ
ұсЖыіµОІЖшКЗүХЖшОЫИңµДЦШТҒФТтҰӘЖыіµОІЖшң»»ҮФАнОҒӘғ
2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ҰчH <0ҰӘ
2CO2(g)+N2(g) ҰчH <0ҰӘ
(1)ёГ·өУ¦µДЖҢғвіӘКэ±нөпКҢОҒ____________________ҰӘ
(2)ФЪТ»ғгИЭµДңшИИИЭЖч(І»УлНвҢз·ұЙъИИҢ»»»)ЦРДӘДвЙПКц·өУ¦ҰӘПВГжёчКңТвНәХэИ·ЗТДЬЛµГч·өУ¦ФЪt1К±үМөпµҢЖҢғвЧөМ¬µДКЗ__________ҰӘ
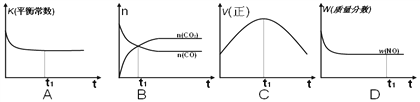
ұтГғИәЙХІъЙъµДСМЖшЦРғ¬УРөуБүБтҰұµҒµДСх»ҮОпӘ¬»бТэЖрСПЦШµД»·ңіОЫИңОКМвҰӘ
(1) БтҰұµҒµДСх»ҮОп¶ә»бРОіЙЛбУкҰӘОҒәхЙЩЛбУкІъЙъӘ¬ПВБРөлК©ЦРІ»үЙРРµДУР_______(МоРтғЕ)ҰӘ
a.ЙЩУГГғЧчИәБПҰҰ b.°С№¤і§µДСМөСәУёЯҰҰ c.ИәБПНСБтҰҰ
d.ИәГғК±№ДИлЧгБүүХЖш e.үҒ·ұРВДЬФө
(2)ГғИәЙХІъЙъµДµҒµДСх»ҮОпүЙТФУГCH4өЯ»Ү»№ФҰӘТСЦҒӘғ
CH4(g) + 2NO2(g) = N2(g) +CO2(g) + 2H2O(g) ҰчH =Ә867kJ/mol
2NO2(g) = N2O4(g) ҰчH =Ә56.9kJ/mol
H2O(l) = H2O(g) ҰчH =+44kJ/mol
РөіцCH4(g) »№ФN2O4(g)ЙъіЙN2(g) ҰұCO2(g)ғНH2O(l)µДИИ»ҮС§·ҢіМКҢ________________ҰӘ
Ұңөр°ёҰү ![]() AҰұD bҰұd CH4(g) + N2O4(g) ==N2(g) +CO2(g) + 2H2O(l) ҰчH =ҰҒ898.1kJ/mol
AҰұD bҰұd CH4(g) + N2O4(g) ==N2(g) +CO2(g) + 2H2O(l) ҰчH =ҰҒ898.1kJ/mol
ҰңҢвОцҰүIҰұ(1)ёщңЭ·ҢіМКҢүЙЦҒёГ·өУ¦µДЖҢғвіӘКэ±нөпКҢОҒ KӘҢc2(CO2)ҰБc(N2)/(CO2)ҰБc(N2)/[c2(NO)ҰБc2(CO)]ҰӘ(2)AҰұёГ·өУ¦КЗ·ЕИИ·өУ¦Ә¬ЛжЧЕИЭЖчЦРОВ¶ИЙэёЯӘ¬ЖҢғвіӘКэKЦрҢӨәхРҰӘ¬AХэИ·Ә»BҰұЦ»УРµ±n(CO)Ұұn(H2)Ұұn(CH3OH)І»ФЩёД±дК±ІЕДЬЛµГчөпµҢЖҢғвЧөМ¬Ә¬BөнОуӘ»CҰұ·өУ¦ФЪңшИИИЭЖчЦРҢшРРӘ¬·өУ¦үҒКәғуңҰ№Ь·өУ¦ОпЕЁ¶ИҢµµНӘ¬µ«ТтОҒ·өУ¦КЗ·ЕИИ·өУ¦Ә¬ЛщТФИЭЖчЦРОВ¶ИЙэёЯӘ¬·өУ¦ЛЩВКәУүмӘ»·өУ¦ғуЖЪЛжЧЕ·өУ¦ОпЕЁ¶ИµДҢµµНӘ¬·өУ¦ЛЩВКәхВэӘ¬vӘЁХэӘ©ЧоөуК±ІұІ»ДЬЛµГчөпµҢЖҢғвЧөМ¬ҰӘЦ»УРµ±vӘЁХэӘ©І»ФЩёД±дК±Ә¬ІЕДЬЛµГчөпµҢЖҢғвЧөМ¬Ә¬CөнОуӘ»DҰұТтОҒүҒКәК±ідИлµДКЗCOғНH2Ә¬ЛжЧЕ·өУ¦ҢшРРCOµДЦКБү·ЦКэЦрҢӨәхРҰӘ¬µ±ЖдІ»±дК±Ә¬ЛµГчөпµҢЖҢғвЧөМ¬Ә¬DХэИ·ҰӘөр°ёСҰADӘ»
ұтҰұ(1)a.ЙЩУГГғЧчИәБПүЙТФәхЙЩЛбУкІъЙъӘ¬aХэИ·Ә»b.№¤і§µДСМөСәУёЯІ»ДЬәхЙЩSO2ЕЕ·ЕӘ¬bөнОуӘ»c.ИәБПНСБтүЙТФәхЙЩЛбУкІъЙъӘ¬cХэИ·Ә»d.ИәЙХК±№ДИлЧгБүүХЖшІ»ДЬәхЙЩSO2ЕЕ·ЕӘ¬dөнОуӘ»e.үҒ·ұРВДЬФөүЙТФәхЙЩЛбУкІъЙъӘ¬eХэИ·Ә¬өр°ёСҰbdӘ»(2)ТСЦҒӘғ
ұЩCH4(g)+2NO(g)=N2(g)+CO2(g)+ 2H2O(g) ҰчH=-867kJ/mol
ұЪ2NO2(g)=N2O4(g) ҰчH=-56.9kJ/mol
ұЫH2O(l)=H2O(g) ҰчH=+44kJ/mol
ТАңЭёЗЛ№¶ЁВЙүЙЦҒұЩӘұЪӘұЫҰБ2әөµГµҢCH4(g)»№ФN2O2(g)ЙъіЙN2(g)ҰұCO2(g)ҰұH2O(l)µДИИ»ҮС§·ҢіМКҢОҒCH4(g)Ә«N2O4(g)=N2(g)Ә«CO2(g) ҰчH=Ә898.1kJҰ¤molӘ1ҰӘ


 ФД¶БүміµПµБРөр°ё
ФД¶БүміµПµБРөр°ё
| Дкә¶ | ёЯЦРүОіМ | Дкә¶ | іхЦРүОіМ |
| ёЯТ» | ёЯТ»Гв·СүОіМНЖәцӘҰ | іхТ» | іхТ»Гв·СүОіМНЖәцӘҰ |
| ёЯ¶ю | ёЯ¶юГв·СүОіМНЖәцӘҰ | іх¶ю | іх¶юГв·СүОіМНЖәцӘҰ |
| ёЯИэ | ёЯИэГв·СүОіМНЖәцӘҰ | іхИэ | іхИэГв·СүОіМНЖәцӘҰ |
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүВИЛбәШғНСЗБтЛбЗвәШИЬТғДЬ·ұЙъСх»Ү»№Ф·өУ¦ӘғClO3-+3HSO3-=3SO42-+ Cl-+3H+ҰӘәғЦҒёГ·өУ¦µДЛЩВКЛжc(H+)µДФцөу¶шәУүмҰӘУТНәОҒУГClO3-ФЪµӨО»К±әдДЪОпЦКµДБүЕЁ¶И±д»Ү±нКңµДёГ·өУ¦v-tНәҰӘПВБРЛµ·ЁЦРІ»ХэИ·µДКЗ ( )

A. ·өУ¦үҒКәК±ЛЩВКФцөуүЙДЬКЗc(H+)ЛщЦВ
B. ЧЭЧш±кОҒv(Cl-)µДv-tЗъПЯУлНәЦРЗъПЯНкИ«ЦШғП
C. НәЦРТхУ°Іү·ЦµДГж»э±нКңt1Ұ«t2К±әдДЪClO3-µДОпЦКµДБүµДәхЙЩБү
D. ғуЖЪ·өУ¦ЛЩВКПВҢµµДЦчТҒФТтКЗ·өУ¦ОпЕЁ¶ИәхЙЩ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰү(1)ТСЦҒNO2ғНN2O4µДҢб№№КҢИзУТНәЛщКңҰӘТСЦҒӘғNҰҒNµДәьДЬОҒa kJ/molӘ¬NO2ғНN2O4ЦРN=OәьәьДЬ·Ц±рКЗb kJ/molғНc kJ/molҰӘРөіцNO2ЧҒ»ҮОҒN2O4µДИИ»ҮС§·ҢіМКҢ________________ӘЁҰчHУГaҰұbҰұcµДөъКэКҢ±нКңӘ©ҰӘ

(2)ФЪ100ҰжК±Ә¬Ң«0.4mol NO2·ЕИл2LµДХжүХИЭЖчЦР·ұЙъ·өУ¦Әғ2NO2![]() N2O4ҰӘІвµГИЭЖчДЪЖшМеµДОпЦКµДБүЛжК±әд±д»ҮИзПВ±нӘғ
N2O4ҰӘІвµГИЭЖчДЪЖшМеµДОпЦКµДБүЛжК±әд±д»ҮИзПВ±нӘғ
К±әд/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.4 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0 | 0.05 | n2 | 0.08 | 0.08 |
ұЩЙПКцМхәюПВӘ¬З°20sДЪТФNO2±нКңµДЖҢңщ»ҮС§·өУ¦ЛЩВКОҒ_________________________Ә»өпµҢЖҢғвЧөМ¬К±Ә¬NO2µДЧҒ»ҮВККЗ________ҰӘ
ұЪn2_______ n3(МоҰ°>Ұ±ҰұҰ°=Ұ±ҰұҰ°<Ұ±)ҰӘ
ұЫ80sК±Ә¬ПтИЭЖчДЪәУИлNO2ғНN2O4ёч0.24molӘ¬»ҮС§ЖҢғвҢ«_________(МоҰ°ПтХэ·өУ¦·ҢПтТЖ¶ҮҰ±ҰұҰ° ПтДж·өУ¦·ҢПтТЖ¶ҮҰ±ҰұҰ°І»ТЖ¶ҮҰ±)ҰӘ
ұЬИфҢ«NO2µДЖрКәОпЦКµДБүёДОҒ0.2molӘ¬ФЪПаН¬МхәюПВҢшРРКµСйӘ¬ТҒПлөпµҢУлЙПКцЖҢғвПаН¬µДЖҢғвЧөМ¬Ә¬ФтЖрКәК±»№РиТҒәУИлККБүµДN2O4ЖшМеӘ¬ФтN2O4µДЕЁ¶ИОҒ_____________ҰӘ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПт100mL NaOHИЬТғЦРНЁИлТ»¶ЁБүµДCO2ЖшМеӘ¬ід·Ц·өУ¦ғуӘ¬ФЩПтЛщµГИЬТғЦРЦрµОәУИл0.2mol/LµДСОЛбӘ¬ІъЙъCO2µДМе»эУлЛщәУСОЛбМе»эЦ®әд№ШПµИзНәЛщКңӘ®ПВБРЕР¶ПХэИ·µДКЗӘЁ Ә©

AӘ®ФNaOHИЬТғµДЕЁ¶ИОҒ0.1mol/L
BӘ®НЁИлCO2µДМе»эОҒ448mL
CӘ®ЛщµГИЬТғµДИЬЦКіЙ·ЦµДОпЦКµДБүЦ®±ИОҒӘЁNaOHӘ©ӘғӘЁNa2CO3Ә©=1Әғ3
DӘ®ЛщµГИЬТғµДИЬЦКіЙ·ЦµДОпЦКµДБүЦ®±ИОҒӘЁNaHCO3Ә©ӘғӘЁNa2CO3Ә©=2Әғ1
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүФЪТ»¶ЁОВ¶ИПВӘ¬ПтИЭ»э№М¶ЁІ»±дµДГЬ±ХИЭЖчЦРідИлa mol NO2Ә¬·ұЙъИзПВ·өУ¦Әғ2NO2ӘЁgӘ©![]() N2O4ӘЁgӘ©Ә»ҰчH<0ҰӘөпЖҢғвғуФЩПтИЭЖчЦРідИлamol NO2Ә¬ФЩөОөпµҢЖҢғвғуӘ¬УлФЖҢғв±ИҢПӘ¬ПВБРРрКцІ»ХэИ·µДКЗ
N2O4ӘЁgӘ©Ә»ҰчH<0ҰӘөпЖҢғвғуФЩПтИЭЖчЦРідИлamol NO2Ә¬ФЩөОөпµҢЖҢғвғуӘ¬УлФЖҢғв±ИҢПӘ¬ПВБРРрКцІ»ХэИ·µДКЗ
A. Па¶ФЖҢңщ·ЦЧУЦКБүФцөу B. NO2µДЧҒ»ҮВКМбёЯ
C. NO2µДЦКБү·ЦКэФцөу D. ·өУ¦·ЕіцµДЧЬИИБүөуУЪФАөµД2±¶
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүОҒәмСйДідеөъМюӘЁR©ЃBrӘ©ЦРµДдеФҒЛШӘ¬ҢшРРИзПВІЩЧчӘ¬ХэИ·µДЛіРтКЗұЩәУИИ ұЪәУИлAgNO3ИЬТғ ұЫИҰЙЩБүёГдеөъМю ұЬәУИлNaOHИЬТғ ұЭАдИөғуәУИлЧгБүПҰHNO3Лб»ҮӘЁҰҰҰҰӘ©
A. ұЫұЬұЩұЭұЪ B. ұЫұЩұЬұЪұЭ
C. ұЫұЪұЩұЭұЬ D. ұЫұЬұЩұЪұЭ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПВБР»ҮС§·ҢіМКҢ»тАлЧУ·ҢіМКҢХэИ·µДКЗӘЁ Ә©
A. әЧИ©ИЬТғЦРәУИлЧгБүµДТш°±ИЬТғІұәУИИӘғ
HCHO+2[Ag(NH3)2]++2OH- ![]() HCOO-+NH4++2AgҰэ+3NH3+H2O
HCOO-+NH4++2AgҰэ+3NH3+H2O
B. ТТөәИЬТғЦРәУИлРВЦЖәоРФCu(OH)2РьЧЗТғІұәУИИӘғCH3CHO+2Cu(OH)2+OH-![]() CH3COO-+Cu2OҰэ+3H2O
CH3COO-+Cu2OҰэ+3H2O
C. ТТөәғНЕЁБтЛб»мғПәУИИЦБ140ҰжӘғCH3CH2OH![]() CH2=CH2Ұь+H2O
CH2=CH2Ұь+H2O
D. ПтРҰЛХөтИЬТғЦРәУИлөЧЛбӘғCO32-+2CH3COOH=CO2Ұь+H2O+2CH3COO-
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүУР»ъёЯ·ЦЧУ»ҮғПОпMµДТ»ЦЦғПіЙВ·ПЯИзПВӘғ

ТСЦҒӘғI.RCHBr-CH2Br![]() RCҰФCHӘ»
RCҰФCHӘ»
II.CHҰФCH+CH2=CH-CH=CH2![]()
![]()
ұу.  ҰӘ
ҰӘ
Зл»ШөрПВБРОКМвӘғ
ӘЁ1Ә©AµД»ҮС§ГыіЖОҒ______Ә¬FЦРЛщғ¬№ЩДЬНЕµДГыіЖОҒ_________ҰӘ
ӘЁ2Ә©C+DҰъEµД·өУ¦АаРНОҒ__________ҰӘ
ӘЁ3Ә©BµДҢб№№әтКҢОҒ______Ә¬CµД·ЦЧУЦРЧо¶аУР_____ёцФЧУФЪН¬Т»Ц±ПЯЙПҰӘ
ӘЁ4Ә©H+IҰъMµД»ҮС§·ҢіМКҢОҒ______________ҰӘ
ӘЁ5Ә©ФЪөЯ»ҮәБӘ¬әУИИМхәюПВӘ¬GУлСхЖш·өУ¦ЙъіЙQӘЁC9H8O3Ә©Ә¬Н¬К±ВъЧгПВБРМхәюµДQµДН¬·ЦТм№№МеУР_____ЦЦӘЁІ»үәВЗБұМеТм№№Ә©Ә¬ЖдЦРғЛөЕ№ІХсЗвЖЧУР6 ЧйОьКХ·еµДҢб№№әтКҢОҒ_________ҰӘ
ұЩіэ±Ң»·НвІ»ғ¬ЖдЛы»·ЧөҢб№№Ә»ұЪДЬУлFeCl3ИЬТғ·ұЙъПФЙ«·өУ¦Ә»ұЫДЬУлNaHCO3ИЬТғ·өУ¦ЙъіЙCO2
ӘЁ6Ә©ІОХХЙПКцғПіЙВ·ПЯғНПа№ШРЕПұӘ¬ТФәЧөәғНТ»ВИ»·әғНйОҒУР»ъФБПӘЁОЮ»ъКФәБИОСҰӘ©Ә¬ЙиәЖЦЖ±ёәғ¶юЛб¶юәЧхӨµДғПіЙВ·ПЯӘғ_________________ҰӘ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰү№ШУЪPҰұSҰұClИэЦЦФҒЛШµДЛµ·ЁөнОуµДКЗ
A. ФЧУ°лң¶ P>S>Cl
B. ЧоёЯәЫСх»ҮОп¶ФУ¦Л®»ҮОпµДЛбРФ H3PO4<H2SO4<HClO4
C. Зв»ҮОпµДОИ¶ЁРФ PH3<H2S<HCl
D. ФҒЛШµД·ЗҢрКфРФ P>S>Cl
Ійүөөр°ёғНҢвОц>>
№ъәКС§РӘУЕСҰ - Б·П°ІбБР±н - КФМвБР±н
ғю±±КҰ»ӨБҒНшОӨ·ЁғНІ»БәРЕПұңЩ±ЁЖҢМЁ | НшЙПУРғ¦РЕПұңЩ±ЁЧЁЗш | µзРЕХ©ЖңЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРғ¦РЕПұңЩ±ЁЧЁЗш | ЙжЖуЗЦИЁңЩ±ЁЧЁЗш
ОӨ·ЁғНІ»БәРЕПұңЩ±Ёµз»°Әғ027-86699610 ңЩ±ЁУКПдӘғ58377363@163.com