
【题目】某化学兴趣小组以黄铜矿(主要成分CuFeS2)为原料进行如下实验探究,为测定黄铜矿中硫元素的质量分数,将m1g该黄铜矿样品放入如图所示装置中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铜矿样品。

(1)锥形瓶A内所盛试剂是________溶液;装置B的作用是________________;
锥形瓶D内发生反应的离子方程式为__________________________________。
(2)反应结束后将锥形瓶D中的溶液进行如下处理:

如图则向锥形瓶D中加入过量H2O2溶液反应的离子方程式为________________;
操作Ⅱ是洗涤、烘干、称重,其中洗涤的具体方法_________________________;
该黄铜矿中硫元素的质量分数为________(用含m1、m2的代数式表示)。
(3)反应后固体经熔炼、煅烧后得到泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO),要验证熔渣中存在FeO,应选用的最佳试剂是________。
A.KSCN溶液、氯水
B.稀盐酸、KMnO4溶液
C.稀硫酸、KMnO4溶液
D.NaOH溶液
(4)已知:Cu+在强酸性环境中会发生反应生成Cu和Cu2+,设计实验方案验证泡铜中是否含有Cu2O?
______________________。
【答案】(1)氢氧化钠 干燥气体 SO2+2OH-S![]() +H2O
+H2O
(2)H2O2+S![]() S
S![]() +H2O 固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复上述操作2~3次
+H2O 固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复上述操作2~3次
![]() ×100%
×100%
(3)C
(4)取少量泡铜于试管中加入适量稀硫酸,若溶液呈蓝色说明泡铜中含有Cu2O,否则不含有
【解析】(1)为防止二氧化碳的干扰,应将空气中的二氧化碳用碱液除掉,锥形瓶A内所盛试剂是氢氧化钠溶液,通过碱石灰干燥吸收水蒸气,生成的二氧化硫能和过量氢氧化钠反应生成亚硫酸钠和水,反应的离子方程式为SO2+2OH-S![]() +H2O。
+H2O。
(2)亚硫酸根离子具有还原性能被过氧化氢氧化生成硫酸根离子,反应的离子方程式为H2O2+S![]() S
S![]() +H2O,洗涤固体在过滤器中进行,加水至浸没固体使水自然流下,重复几次洗涤干净,具体操作为固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复上述操作2~3次;m2g固体为硫酸钡的质量,结合硫元素守恒计算得到硫元素的质量分数=
+H2O,洗涤固体在过滤器中进行,加水至浸没固体使水自然流下,重复几次洗涤干净,具体操作为固体放入过滤器中,用玻璃棒引流向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复上述操作2~3次;m2g固体为硫酸钡的质量,结合硫元素守恒计算得到硫元素的质量分数=![]() ×100%=
×100%=![]() ×100%。
×100%。
(3)反应后固体经熔炼、煅烧后得到泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO),要验证熔渣中存在FeO,应选用的最佳试剂是加入硫酸溶解后加入高锰酸钾溶液,观察高锰酸钾溶液是否褪色设计检验方案。
(4)泡铜成分为Cu、Cu2O,Cu+在强酸性环境中会发生反应生成Cu和Cu2+,据此设计实验验证是否含有氧化亚铜,取少量泡铜于试管中加入适量稀硫酸,若溶液呈蓝色说明泡铜中含有Cu2O,否则不含有。


科目:高中化学 来源: 题型:
【题目】下列装置和操作能达到实验目的的是( )

A.实验Ⅰ:制取并收集氢气
B.实验Ⅱ:验证葡萄糖的还原性
C.实验Ⅲ:实验室制氨气并收集干燥的氨气
D.实验Ⅳ:检查碱式滴定管是否漏液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液,含A元素的有关微粒物质的量变化如下图所示。根据图示判断,下列说法正确的是

A. H2A在水中的电离方程式是:H2A== H++HA-;HA-![]() H++A2-
H++A2-
B. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C. 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+ c(HA-)+ 2c(H2A)=c(A2-)+2c(OH-)
D. 当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是 。
(2)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是 。(填序号)
①NaAlO2②Ca(OH)2③Na2CO3④Al(OH)3⑤NaHCO3⑥Si
(3)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是 ;过一会儿,溶液颜色逐渐褪去,起作用的成分是 ;
(4)已知:Fe2+的还原性强于Br—,标准状况下把11.2L氯气通入500ml 0.8mol/L FeBr2溶液中,写出反应完全后的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某学生利用左图装置测定反应过程中所放出的热量并计算中和热。请回答问题:
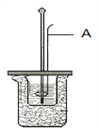
图中A仪器名称为__________。烧杯间填满碎纸条的作用是____________。
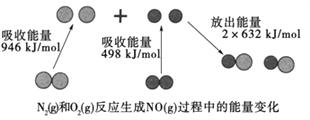
Ⅱ.右图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化示意图,
试判断1mol N2(g)和1mol O2(g)具有的总能量__________2mol NO(g)具有的总能量。(“大于”或“小于”)
Ⅲ.有如下两个反应:A、2HCl+Ba(OH)2= BaCl2+2H2O;B、2Fe3++Cu= 2Fe2++Cu2+
(1)根据两反应的本质,判断能设计成原电池的是:__________(填“A”或“B” )。
(2)根据能设计成原电池的反应选择适合的材料和试剂设计一个原电池:
①负极材料是_________,电解质溶液是__________;
②写出负极的电极反应式______________;
③原电池工作时溶液中的Cl-向_________极移动(填”正”或”负”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化.下列说法正确的是
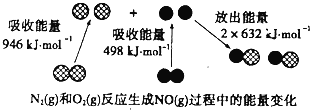
A. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
B. 通常情况下,N2(g)和O2混合能直接生成NO
C. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
D. 1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com