
【题目】由乙醇合成部分有机物的路线如下:
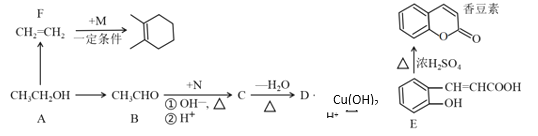
已知:CH3CHO+CH3CHO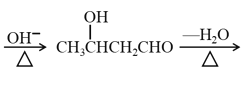 CH3CH=CHCHO
CH3CH=CHCHO
(1)香豆素所含官能团名称_____________。
(2)M的名称_________。
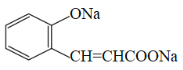
(3)N的结构简式____________。
(4)B与银氨溶液反应方程式___________________。
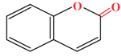
(5)香豆素在NaOH溶液中发生水解反应的化学方程式为_____________。
(6)由A到F反应的化学方程式___________。
(7)以乙醇为起始原料,无机试剂任选,合成CH3CH=CHCOOC2H5写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)______________。
【答案】碳碳双键、酯键 2,3-二甲基-1,3-丁二稀 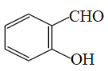
![]()
 +2NaOH
+2NaOH![]()
 +H2O
+H2O ![]()
![]()
![]()
【解析】
由图可知乙醇通过消去反应得到F乙烯,由已知条件2和生成物推断M的结构式,乙醇通过铜的催化氧化得到乙醛,由条件1可知N为 ,C为
,C为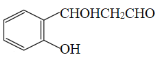 ,D为:
,D为: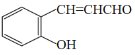 ,D和新制氢氧化铜反应制得E,E通过自身的酯化反应得到香豆素。据此分析。
,D和新制氢氧化铜反应制得E,E通过自身的酯化反应得到香豆素。据此分析。
(1)由香豆素 结构式可知香豆素所含官能团名称碳碳双键、酯键,故答案为:碳碳双键、酯键;
结构式可知香豆素所含官能团名称碳碳双键、酯键,故答案为:碳碳双键、酯键;
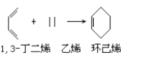
(2)由已知条件2和生成物![]() 可知M为2,3-二甲基-1,3-丁二稀,故答案为:2,3-二甲基-1,3-丁二稀;
可知M为2,3-二甲基-1,3-丁二稀,故答案为:2,3-二甲基-1,3-丁二稀;
(3)由E得结构简式可推出D的结构简式为: ,由D的结构简式和条件可以推出C的结构简式为:
,由D的结构简式和条件可以推出C的结构简式为: ,由C和已知条件1可以推出N的结构简式
,由C和已知条件1可以推出N的结构简式 ;
;
(4)B与银氨溶液反应方程式![]() ,故答案为:
,故答案为:![]() ;
;
(5)香豆素在NaOH溶液中发生水解反应的化学方程式为 +2NaOH
+2NaOH![]()
 +H2O;
+H2O;
(6)由A到F反应的化学方程式![]() ;
;
(7)由已知条件可以用乙醇催化氧化制取乙醛,再由乙醛由已知条件1制得![]() 再发生消去反应得到
再发生消去反应得到![]() ,再发生氧化反应得到
,再发生氧化反应得到![]() ,再通过和乙醇的酯化反应得到
,再通过和乙醇的酯化反应得到![]() ,合成路线如下所示:
,合成路线如下所示:![]()
![]() 。
。


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】纳米Fe3O4在生物医学和催化剂载体等领域应用前景光明。其制备流程如下:
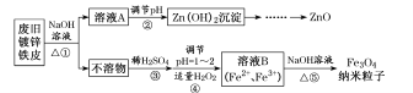
已知:锌单质溶于强碱生成ZnO22-;Zn(OH)2既能溶于强酸又能溶于强碱。
请回答下列问题:
(l)用NaOH溶液处理废旧锌铁皮的作用有___。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)步骤②生成Zn(OH)2沉淀的离子方程式为____,用离子方程式结合文字说明该步骤pH不能过小的原因____。调节pH的最佳方法是向溶液中通入____(填化学式)。
(3)步骤④反应的离子方程式为_____;为确保纳米Fe3O4粒子的纯度,应调整原溶液中Fe2+与所加H2O2的物质的量之比为_______。
(4)步骤⑤制得Fe3O4纳米粒子的过程,需要在无氧环境下进行,说明理由__________;T业生产中可采取___________措施提供无氧环境。
(5)步骤⑤ _______(填“能”或“不能”)用减压过滤(抽滤)得到纳米Fe3O4粒子?理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.28g乙烯和环烷的混合气体中含有的碳原子数为2NA
B.2.0gD2O中含有的质子数、电子数均为NA
C.常温下,5.6gFe与含0.2molHNO3的溶液充分作用,最少失去的电子数为0.15NA
D.含1molCl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH4+数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是药物合成的种中间体,可通过以下方法合成:

(1)B中官能团名称为__。
(2)G→H的反应类型为__。
(3)已知C的一种同分异构体为: ,下列说法正确的是__。
,下列说法正确的是__。
a.能发生酯化反应
b.能发生银镜反应
c.1mol该物质完全水解能消耗3molNaOH
d.该分子的核磁共振氢谱中峰面积之比为1:2:6:2
e.其在酸性条件下的水解产物之一能与FeCl3溶液发生显色反应
(4) 中手性碳原子个数为__。
中手性碳原子个数为__。
(5)E的分子是为C14H17O3N,E经还原得到F,写出E→F的反应方程式:__。
(6)已知:①
②苯胺(![]() 易被氧化
易被氧化
请以甲苯和(CH3CO)2O为原料制备 ,写出制备的合成路线流程图(无机试剂任选)。__。
,写出制备的合成路线流程图(无机试剂任选)。__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是不同温度下水的离子积的数据:
温度 | 25 |
|
|
水的离子积 |
| a |
|
试回答以下问题
(1)若![]() ,则a______1×10-14填“<”“>”或“=”)。
,则a______1×10-14填“<”“>”或“=”)。
(2)250C时,某Na2SO4溶液中c(SO42-)=5×10-4mol/L,取该溶液1mL加水稀释至10mL,则稀释后溶液中![]() :
:![]() ______。
______。
(3)在![]() 温度下测得某溶液
温度下测得某溶液![]() ,该溶液显______
,该溶液显______![]() 填“酸”、“碱”或“中”
填“酸”、“碱”或“中”![]() 性
性![]() 将此温度下
将此温度下![]() 的NaOH溶液aL与
的NaOH溶液aL与![]() 的
的![]() 溶液bL混合,若所得混合液
溶液bL混合,若所得混合液![]() ,则a:b______。
,则a:b______。
(4)某同学用0.1 mol·L-1的NaOH溶液分别滴定20.00 mL0.1 mol·L-1的HCl溶液和0.1 mol·L-1的CH3COOH溶液,得到如图所示的两条滴定曲线,请回答有关问题:
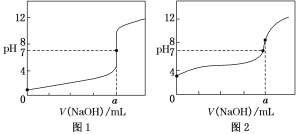
①0.1 mol·L-1的NaOH溶液滴定0.1 mol·L-1的CH3COOH溶液的曲线是______(填“图1”或“图2”)曲线。
②a=________。
(5)某同学用0.1 mol·L-1的NaOH溶液分别滴定20.00 mL未知浓度的HCl溶液选用_______作指示剂,若装标准液的滴定管未润洗则会导致测定结果________(填“偏高”或“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明许多疾病,包括基因突变(癌变、动脉硬化等)和生物机体中毒等,可能是一氧化氮的释放或调节不正常引起的。用间接电化学法可对NO进行无害化处理,其原理如图所示(质子膜允许H+和H2O通过),下列相关判断不正确的是 ( )
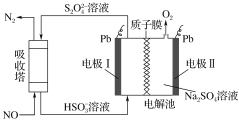
A.电极Ⅰ接电源负极,电极反应式为2HSO3-+2H++2e-==S2O42-+2H2O
B.质子从电极Ⅱ通过质子膜向电极Ⅰ作定向移动
C.吸收塔中的反应为2NO+2S2O42-+2H2O==N2+4HSO3-
D.每处理2 mol NO,电解池质量减少32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸是唯一具有脂溶性的果酸,在医药工业可用于头孢羟唑、血管扩张药环扁桃酸酯、滴眼药羟苄唑、匹莫林等的中间体,也可作防腐剂。实验室用如下原理制备:

合成扁桃酸的实验步骤、装置示意图及相关数据如下:
物质 | 状态 | 熔点/℃ | 沸点/℃ | 溶解性 |
扁桃酸 | 无色透明晶体 | 119 | 300 | 易溶于热水、乙醚和异丙醇 |
乙醚 | 无色透明液体 | -116.3 | 34.6 | 溶于低碳醇、苯、氯仿,微溶于水 |
苯甲醛 | 无色液体 | -26 | 179 | 微溶于水,能与乙醇、乙醚、苯、氯仿等混溶 |
氯仿 | 无色液体 | -63.5 | 61.3 | 易溶于醇、醚、苯、不溶于水 |
实验步骤:

步骤一:向如图所示的实验装置中加入0.1mol(约l0.1mL)苯甲醛、0.2mol(约16mL)氯仿,慢慢滴入含19g氢氧化钠的溶液,维持温度在55~60℃,搅拌并继续反应1h,当反应液的pH接近中性时可停止反应。
步骤二:将反应液用200mL水稀释,每次用20mL乙醚萃取两次,合并醚层,待回收。
步骤三:水相用50%的硫酸酸化至pH为2~3后,再每次用40mL乙醚分两次萃取,合并萃取液并加入适量无水硫酸钠,蒸出乙醚,得粗产品约11.5g。请回答下列问题:
(1)图中仪器C的名称是_________________,装置B的作用是_____________
(2)步骤一中合适的加热方式是_____________________。
(3)步骤二中用乙醚的目的是_____________________。
(4)步骤三中加入适量无水硫酸钠的目的是_____________________。
(5)该实验的产率为____________(保留三位有效数字)。
(6)扁桃酸在高端化学中也有很重要的作用,如以扁桃酸与正丁醇为原料,在催化剂的催化下可合成手性拆分剂扁桃酸正丁酯,试写出该反应的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol/L NaHS溶液:c(H+)+c(Na+)=c(S2-)+c(HS-)+c(OH-)
B.0.1mol/L Na2CO3溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.2 mol/L
C.浓度均为0.1 mol/L的 ① NH4Cl ②NH4Al(SO4)2 ③ NH4HCO3三种溶液,其中c(NH4+):②>①>③
D.pH=11的NaOH溶液与pH =3的CH3COOH溶液等体积混合:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯喹是合成一种抑制病毒药物的中间体,其合成路线如图:
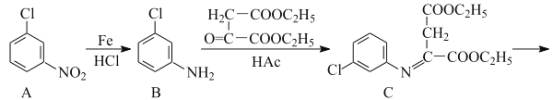
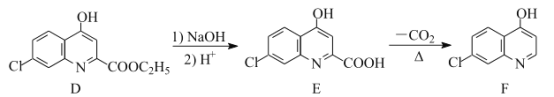
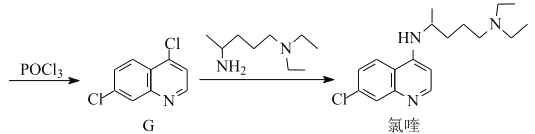
(1)D中含氧官能团的名称为___和___。
(2)A→B的反应类型为___。
(3)C→D的反应中有副产物X(X与D互为同分异构体)生成,写出X的结构简式:
___。
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
①酸性条件下水解得到的两种有机产物,都能发生银镜反应,其中一种与FeCl3溶液发生显色反应;
②分子中有氰基(-CN),有一个手性碳原子,有4种不同化学环境的氢。
(5)已知:①![]() NH2易被氧化;
NH2易被氧化;
②酰氯(![]() Cl)的氯原子比氯代烃的更易被取代
Cl)的氯原子比氯代烃的更易被取代
③![]() RHC=N-CH2R’
RHC=N-CH2R’
写出以![]() 和
和![]() 为原料制备
为原料制备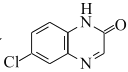 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)___。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com