
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
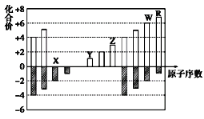
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R<W
C. WX3和水反应形成的化合物是离子化合物
D. Y和Z两者最高价氧化物对应的水化物能相互反应
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.碳酸钙与盐酸反应:CO32﹣+H+═H2O+CO2
B.铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2
C.硝酸与氢氧化钡反应:OH﹣+H+═H2O
D.铜片插入硝酸银溶液中: Cu+Ag+=Cu2++Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在透明溶液中能大量共存的是( )
A.K+、Cu2+、Na+、Cl-
B.H+、Na+、NO3-、HCO3-
C.Ba2+、H+、NO3-、SO42-
D.Mg2+、Na+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.钠的摩尔质量等于它的相对原子质量
B.CH4的摩尔质量为16 g/mol
C.22.4 L任何气体的物质的量均为1 mol
D.1 mol 任何物质均含有NA个分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造如图(a)所示。回答下列问题:

(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2===Zn(NH3)2Cl2+2MnOOH,该电池中,负极材料主要是______________,电解质的主要成分是________,正极发生的主要反应是________________________
(2)与普通锌锰电池相比,碱性锌锰电池的优点及其理由是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤的烟气中含有SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。
(1)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是______(填字母序号)。
a.石灰乳b.CaCl2溶液
(2)某工厂利用含SO2的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:

①用SO2处理含铬废水时,利用了SO2的______性。
②吸收塔中发生反应的离子方程式为____________________________________。
(3)该废水经处理后,测得有关数据如下(其他离子忽略不计):
离子 | Cr2O72- | Cr3+ | H + | Na + | SO42- |
浓度(mol/L) | a | 0.2×10-6 | 1.2×10-6 | 6.8×10-6 | 3.0×10-6 |
则a= ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是( )
A. 原子半径:Y>Z>R>T B. 气态氢化物的稳定性:W<R<T
C. 最高价氧化物对应的水化物的碱性:X>Z D. XR2、WR2两种化合物中R的化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述正确的是( )
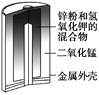
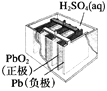
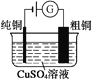
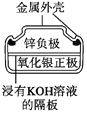
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计计如下图所示装罝(部分夹持装置己略去)进行实验探究:
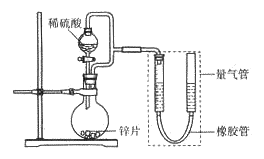
(1)用上述装置探究影响化学反应速率的因素。以生成9.0 mL气体为计时终点,结果为t1>t2。
序号 | V(H2SO4)/mL | C(H2SO4)/mol·L-1 | t/s |
I | 40 | 1 | t1 |
II | 40 | 4 | t2 |
①比较实验I和Ⅱ可以得出的实验结论是_______________。
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据。粗锌片中所含杂质可能是_________(填序号)。
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀。
①圆底烧瓶中的试剂可选用________(填序号)。
A.稀HCl B .NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com