
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A.32 g S8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
B.1L、0.1mol/L的Na2CO3溶液中含阴离子总数为0.1NA个
C.标准状况下,22.4LHF含NA个分子
D.标准状况下,11.2 L Cl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA
科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别充有等物质的量的N2和H2,在相同温度下发生合成氨反应,并达到平衡。在这过程中,甲容器为恒容容器,乙容器为恒压容器,若甲容器中H2的转化率为a%,则乙容器中H2的转化率为:
A.等于a%B.大于a%C.小于a%D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.强酸、强碱、重金属盐等可使蛋白质变性
B.用新制氢氧化铜悬浊液(必要时可加热)能鉴别甲酸、乙醇、乙醛
C.乙酸乙酯中混有的乙酸,可加入足量的饱和![]() 溶液,经分液除去
溶液,经分液除去
D.向苯和苯酚的混合液中加入浓溴水,充分反应后过滤,可除去苯中少量的苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
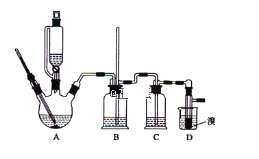
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)写出由乙醇制备乙烯的化学方程式______________________________,乙烯制备1,2-二溴乙烷的化学方程式_______________________________。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___________;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置A中除了浓硫酸和乙醇外,还应加入_____,其目的是_______装置A中生成副产物乙醚的化学反应方程式 ___________________。
(4)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放 ________________,
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液d.品红和酸性KMnO4
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______的方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种元素的基态原子的电子排布式:
① ![]() ;②
;② ![]() ;③
;③ ![]() ;④
;④ ![]() 。
。
则下列有关比较中正确的是( )
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>③>②>①
D.最高正化合价:④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是同周期主族元素,Y的最外层电子数是X次外层电子数的3倍,四种元素与锂组成的盐是一种新型的锂离子电池的电解质(结构如图,箭头指向表示共同电子对由W提供)。下列说法不正确的是( )
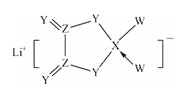
A.W的非金属性比Y的强 B.在该物质中Ⅹ原子满足8电子稳定结构
C.该物质中含离子键和共价键 D.Z的氧化物都易溶于水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置制取少量溴苯![]() 已知该反应为放热反应
已知该反应为放热反应![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
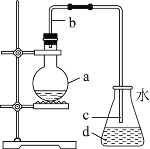
A.加入烧瓶a中试剂是苯、液溴和铁屑
B.导管b的作用是导气和冷凝回流
C.锥形瓶内可以观察到白雾,这是因为生成的HBr结合空气中的水蒸气
D.实验结束后,向d中滴入AgNO3溶液若有淡黄色沉淀生成,则可以证明苯和液溴发生了取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的化工产品。
(1)工业中用氯气和氢气在一定条件下合成氨气,有关方程式如下: 3H2 (g)+N2(g)2NH3 (g) + 92.4 kJ
①对于该反应:要使反应物尽可能快的转化为氨气,可采用的反应条件是__________,要使反应物尽可能多的转化为氨气,可采用的反应条件是__________:(均选填字母)
A.较高温度B.较低温度C.较高压强 D.较低压强 E.使用合适的催化剂
工业上对合成氨适宜反应条件选择,是综合考虑了化学反应速率、化学平衡和设备材料等的影响。
②该反应达到平衡后,只改变其中一个因素,以下分析中不正确的是_______:(选填字母)
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小生成物浓度,对逆反应的反应速率影响更大
③某化工厂为了综合利用生产过程中副产品CaSO4,和相邻的合成氨厂联合设计了制备(NH4)2SO4的工艺流程(如图),该流程中:
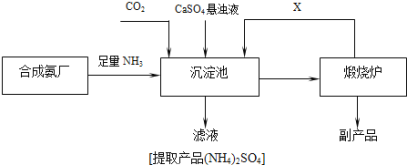
向沉淀池中通入足量的氨气的目的是______________________________,可以循环使用的X是_______________。(填化学式)
(2)实验室中可以用铵盐与强碱共热得到氨气。有关的离子方程式为_____________________。
①0.01 mol/L硝酸铵溶液0.5L,与足量的氢氧化钠溶液共热,可产生氨气_____L(标准状态)。
②若有硝酸铵和硫酸铵的混合溶液0.5L,与足量的氢氧化钠溶液共热,可产生氨气0.025mol;在反应后的溶液中加入足量的氯化钡溶液,产生0.01 mol 白色沉淀,则原混合液中,硝酸铵的浓度为_______mol/L。
③现有硝酸铵、氯化铵和硫酸铵的混合溶液V L,将混合溶液分成两等分:一份溶液与足量的氢氧化钠溶液共热,共产生氨气A mol;另一份溶液中慢慢滴入C mol/L的氯化钡溶液B L,溶液中SO42-恰好全部沉淀;将沉淀过滤后,在滤液中继续滴入硝酸银溶液至过量,又产生D mol沉淀。则原混合溶液中,氯化铵的浓度为________mol/L,硝酸铵的浓度为_______mol/L。(用含有字母的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com