
分析 该反应的焓变大于0,为吸热反应,反应物总能量大于生成物;△H-T△S<0的反应能够自发进行,该反应为气体体积增大的反应,其熵变大于0,据此进行解答.
解答 解:反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ•mol-1的△H>0,说明该反应为吸热反应,则生成物的总能量比反应物的总能量高;
该反应为气体体积增大的反应,则反应后物质的混乱度增加,其熵变△S>0,即熵值增加,
故答案为:高;增加.
点评 本题考查了反应热与焓变的关系及应用,题目难度不大,明确反应自发进行的条件为解答关键,注意掌握熵变的含义及判断方法,试题培养了学生的分析能力及灵活应用基础知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
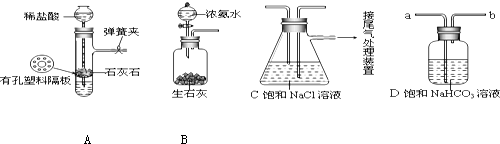
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内每减少1mol A2,同时生成2mol AB3 | |
| B. | 容器内每减少1mol A2,同时消耗3mol B2 | |
| C. | 容器内每减少1mol A2,同时消耗1mol B2 | |
| D. | 容器内每减少1mol A2,同时生成3mol B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜和稀盐酸 | B. | Ba(OH)2溶液滴入稀硫酸中 | ||
| C. | 澄清的石灰水和稀硝酸反应 | D. | 醋酸和氢氧化钠反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为94 | B. | 中子数为144 | C. | 质子数为238 | D. | 电子数为144 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱、氧气、碘酒 | B. | 小苏打、石灰水、二氧化硫 | ||
| C. | 干冰、铁、氯化氢 | D. | 空气、氮气、胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素编号 | 元素性质或原子结构 |
| T | 最高正价与最低负价的代数和为4 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 最高正价是+7价 |
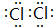 ;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).
;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com