
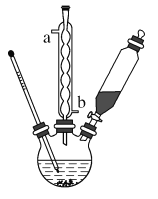
【题目】苯甲酸钠是一种常见食品防腐剂。实验室制备苯甲酸的装置图和有关数据如下:
相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
甲苯 | 92 | -94.9 | 110.6 | 难溶于水 |
苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
苯甲酸钠 | 144 | ---- | 249.3 | 易溶于水 |
(1)制备苯甲酸:在三颈烧瓶中加入4mL甲苯和20mL稀硫酸,放入碎瓷片后,加热至沸腾,加入12.8g高锰酸钾,加热到甲苯层消失。将三颈烧瓶在冰水浴中冷却,分离出苯甲酸。
①球形冷凝管的作用是_________,其进水口是________(填“a”或“b”)。
②已知三颈烧瓶中反应的离子方程式为![]() +6MnO4-+18H+→
+6MnO4-+18H+→![]() +6Mn2++14H2O,在该反应中体现了甲苯____性。
+6Mn2++14H2O,在该反应中体现了甲苯____性。
③分离苯甲酸选用的玻璃仪器除玻璃棒、烧杯外还有________(填字母)。
A.分液漏斗 B.漏斗 C.蒸馏烧瓶 D.直形冷凝管
④分离出粗品苯甲酸晶体中可能含有的杂质是MnSO4和___,为进一步提纯,应采用的操作方法是______。
(2)制备苯甲酸钠:控制温度为70℃,向三颈烧瓶中加入61.0g苯甲酸和适量的32%碳酸钠溶液,充分反应后停止加热。在深色的溶液中加入活性炭,并将混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体。
⑤控制温度为70℃的方法是_______。
⑥加入活性炭的作用是___________。
⑦若提纯得到46.8g苯甲酸钠,则苯甲酸钠的产率________。(保留三位有效数字)
【答案】冷凝回流 b 还原 B K2SO4 重结晶 水浴加热 吸附脱色 65.0%
【解析】
(1)①甲苯易挥发,冷凝管冷凝回流挥发的甲苯;采取逆流原理通入冷凝水,充分冷凝;
②甲苯被酸性高锰酸钾溶液氧化生成苯甲酸;
③苯甲酸微溶于水,常温下为晶体,采取过滤方法分离;
④反应得到溶液中含有硫酸锰、硫酸钾,分离出的苯甲酸晶体中可能含有该杂质,苯甲酸微溶于水,可利用重结晶进行提纯;
(2)⑤低于水的沸点可采取水浴加热,受热均匀,便于控制温度;
⑥在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,说明活性炭吸附色素;
⑦苯甲酸钠的产率=![]() ×100%。
×100%。
(1)①甲苯易挥发,冷凝管冷凝回流挥发的甲苯,减少损失;采取逆流原理通入冷凝水,充分冷凝,即从b口通入冷凝水;
②甲苯被酸性高锰酸钾溶液氧化生成苯甲酸,体现了甲苯还原性;
③苯甲酸微溶于水,常温下为晶体,采取过滤方法分离,需要的仪器有:烧杯、玻璃棒、漏斗;
④反应得到溶液中含有硫酸锰、硫酸钾,分离出的苯甲酸晶体中可能含有的杂质是K2SO4、MnSO4,硫酸锰、硫酸钾易溶于水,苯甲酸微溶于水,可以利用重结晶进行提纯;
(2)⑤控制温度为70℃,低于水的沸点,可以采取水浴加热,受热均匀,便于控制温度;
⑥在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,说明活性炭吸附色素;
⑦61.0g苯甲酸完全转化可以生成苯甲酸钠质量为:61g×![]() =72g,苯甲酸钠的产率=
=72g,苯甲酸钠的产率=![]() ×100%=65.0%。
×100%=65.0%。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】某研究性学习小组讨论甲、乙、丙、丁四种实验装置的有关用法,其中正确的是
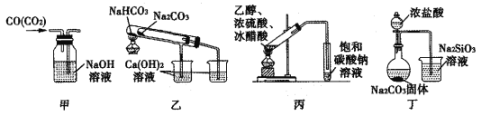
A.甲装置:可用来除去CO气体中的CO2气体
B.乙装置:可用来验证NaHCO3和Na2CO3的热稳定性
C.丙装置:可用来实验室制备乙酸乙酯
D.丁装置:可用来比较HC1、H2CO3和H2SiO3的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,可逆反应mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数时,一定达到平衡的标志是( )
pC(g)+qD(g),当m、n、p、q为任意整数时,一定达到平衡的标志是( )
①体系的温度不再改变 ②体系的压强不再改变
③各组分的浓度不再改变 ④各组分的质量分数不再改变
⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
⑥单位时间内m mol A发生断键反应,同时p mol C也发生断键反应
A. ③④⑤⑥B. ①③④⑥C. ②③④⑥D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:2NH3(g)+NO(g)+NO2(g)== 2N2(g)+3H2O(g) △H<0
①该反应中,反应物总能量_____(填“>”、“<”或“=”)生成物总能量。
②当该反应有2mol N2(g)生成时,转移电子的物质的量为____________mol。
③该反应中,还原剂为_____________(填化学式),氧化产物与还原产物的质量比为______________。
(2)也可以利用甲烷催化还原氮氧化物.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是_________________________________。
(3)还可利用ClO2消除氮氧化物的污染,反应过程如下(部分反应物或生成物略去):
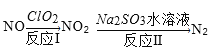
反应I的产物中还有两种强酸生成,且其中一种强酸为硝酸,且硝酸与NO2物质的量相等,则化学反应方程式为______,反应中若生成22.4L N2(标准状况),则消耗ClO2______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
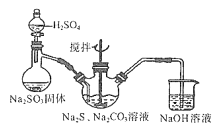
【题目】硫代硫酸钠俗称保险粉,可用于照相业作定影剂、纸浆漂白作脱氯剂等。实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。本实验对Na2S纯度要求较高,利用项图所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按下图所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S9H2O晶体。
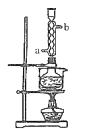
(1)下列说法不正确的是______。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用冷水淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
E.在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析岀而损失、去除杂质
(2)用下图所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是______,三颈烧瓶中发生反应的化学方程式______。
(3)保险粉样品中Na2S2O35H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6,准确称取Wg样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000mol/L碘的标准溶液进行滴定。请回答:
①到达滴定终点的标志______;
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为______,产品的纯度为______(设Na2S2O35H2O相对分子质量为M)。

③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O35H2O的纯度的测量结果______(“偏高”、“偏低”或“不变”)。
(4)某研究小组以硫代硫酸钠与硫酸反应来探究外界条件对反应速率的影响,设计实验如下:
实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
体积/mL | 浓度/mol/L | 体积/mL | 浓度/mol/L | |||
① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
下列有关说法不正确的是______。
A.该同学在实验中采用的研究方法是实验比较法
B.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
C. 实验①和③溶液变浑浊的时间相同
D.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和实验⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐类水解程度的大小可用“水解度”来表示,NaA型盐的水解度为已水解的离子的物质的量占该离子原来总物质的量的百分数。常温下10.0 mL 0.040 mol·L-1 NaOH溶液与20.0 mL 0.020 mol·L-1的某一元弱酸HA恰好完全中和,所得溶液pH为10(假设溶液的体积变化忽略不计),则所得NaA溶液的水解度为
A.1.0%B.0.75%C.0.50%D.0.25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热稳定系数和总氯量是漂白粉行业标准里的两个指标。
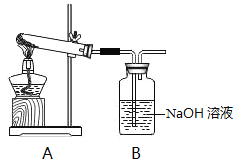
Ⅰ.利用如图装置,探究漂白粉的热分解产物。资料显示:久置于潮湿环境中的漂白粉受热生成的气体产物有O2和少量Cl2。
(1)加热干燥的漂白粉样品,观察到B中只有大量无色气泡产生,则次氯酸钙分解的固体产物中一定有_______________(填化学式)。
(2)加热久置于潮湿环境中的漂白粉样品,观察到B中也有气泡产生。B中发生反应的离子方程式为________________。
Ⅱ.测定漂白粉总氯的百分含量(即样品中氯元素总质量与样品总质量的比值),实验步骤如下:
①准确称取5.000 g漂白粉样品,研细,加蒸馏水溶解并冷却后,配制成500 mL溶液。
②移取25.00 mL该试样溶液至锥形瓶中,调节溶液pH,缓慢加入适量3% H2O2水溶液,搅拌至不再产生气泡。加入适量K2CrO4溶液作为指示剂,以0.1000 mol·L-1AgNO3标准溶液滴定至终点。多次实验,测得消耗AgNO3标准溶液的平均体积为25.00 mL。〔已知:Ksp (AgCl,白色)=1.56×10-10,Ksp (Ag2CrO4,砖红色)=9.0×10-12〕
(3)步骤①溶液配制中,所用的玻璃仪器有烧杯、玻璃棒、________、________。
(4)加入H2O2溶液,搅拌至不再产生气泡,目的是__________(用离子方程式表示)。
(5)滴定终点的现象是___________________________。
(6)该漂白粉总氯的百分含量为______________。
(7)下列操作会导致总氯百分含量测定结果偏高的是__________(填序号)。
A.指示剂K2CrO4的用量过多
B.在达到滴定终点读数时,俯视标准液液面
C.滴定前滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应的平衡常数表达式为![]() ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:
t/°C | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述不正确的是
A.该反应的化学方程式是CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.若平衡浓度符合下列关系式:![]() ,则此时的温度为1 000 °C
,则此时的温度为1 000 °C
D.在1L的密闭容器中通入CO2和H2各1mol,5 min后温度升高到830°C,此时测得CO为0.4 mol,则该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 分子式为C4H8有机物最多存在4个C﹣C单键
B. ![]() 和
和![]() 均是芳香烃,
均是芳香烃,![]() 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
C. ![]() 和
和![]() 分子组成相差一个﹣CH2﹣,因此是同系物关系
分子组成相差一个﹣CH2﹣,因此是同系物关系
D. 分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由此可以初步推测有机物结构简式为C2H5﹣OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com