
【题目】热稳定系数和总氯量是漂白粉行业标准里的两个指标。
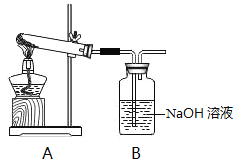
Ⅰ.利用如图装置,探究漂白粉的热分解产物。资料显示:久置于潮湿环境中的漂白粉受热生成的气体产物有O2和少量Cl2。
(1)加热干燥的漂白粉样品,观察到B中只有大量无色气泡产生,则次氯酸钙分解的固体产物中一定有_______________(填化学式)。
(2)加热久置于潮湿环境中的漂白粉样品,观察到B中也有气泡产生。B中发生反应的离子方程式为________________。
Ⅱ.测定漂白粉总氯的百分含量(即样品中氯元素总质量与样品总质量的比值),实验步骤如下:
①准确称取5.000 g漂白粉样品,研细,加蒸馏水溶解并冷却后,配制成500 mL溶液。
②移取25.00 mL该试样溶液至锥形瓶中,调节溶液pH,缓慢加入适量3% H2O2水溶液,搅拌至不再产生气泡。加入适量K2CrO4溶液作为指示剂,以0.1000 mol·L-1AgNO3标准溶液滴定至终点。多次实验,测得消耗AgNO3标准溶液的平均体积为25.00 mL。〔已知:Ksp (AgCl,白色)=1.56×10-10,Ksp (Ag2CrO4,砖红色)=9.0×10-12〕
(3)步骤①溶液配制中,所用的玻璃仪器有烧杯、玻璃棒、________、________。
(4)加入H2O2溶液,搅拌至不再产生气泡,目的是__________(用离子方程式表示)。
(5)滴定终点的现象是___________________________。
(6)该漂白粉总氯的百分含量为______________。
(7)下列操作会导致总氯百分含量测定结果偏高的是__________(填序号)。
A.指示剂K2CrO4的用量过多
B.在达到滴定终点读数时,俯视标准液液面
C.滴定前滴定管尖嘴部分有气泡,滴定后消失
【答案】CaCl2 2OH-+Cl2=Cl-+ ClO-+ H2O 500mL容量瓶 胶头滴管 ClO-+ H2O2=Cl-+O2↑+ H2O 当滴入最后一滴标准液,溶液中出现砖红色沉淀,且半分钟内不消失 35.5% C
【解析】
Ⅰ.(1)加热干燥的漂白粉样品,观察到B中有大量无色气泡,为产生的氧气,结合氧化还原反应中元素化合价的变化分析判断;
(2)久置于潮湿环境中的漂白粉受热生成的气体产物有O2和少量Cl2,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
Ⅱ.(3)根据配制溶液的一般步骤分析判断需要的仪器;
(4)加入H2O2水溶液,搅拌至不再产生气泡,是利用过氧化氢的还原性还原次氯酸根离子生成氯离子,过氧化氢被氧化为氧气;
(5)加入适量K2CrO4溶液作为指示剂,以0.1000molL-1AgNO3标准溶液滴定至终点,溶液中出现砖红色沉淀Ag2CrO4;
(6)结合元素守恒,生成氯化银沉淀的氯离子来源于过氧化氢还原次氯酸根离子,Ag++Cl-=AgCl↓,据此计算漂白粉中总氯的百分含量;
(7)滴定过程中消耗标准溶液体积越多,测定结果越高,反之越低,据此分析判断。
Ⅰ.(1)久置于潮湿环境中的漂白粉受热生成的气体产物有O2和少量Cl2,加热干燥漂白粉样品,观察到B中有大量无色气泡,为产生的氧气,氧化还原反应中存在元素化合价的升高和降低,氧元素化合价升高,氯元素化合价降低,则氯元素化合价变化为-1价,生成固体产物为氯化钙,化学式为CaCl2,故答案为CaCl2;
(2)①久置于潮湿环境中的漂白粉受热生成的气体产物有O2和少量Cl2,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,B中发生反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故答案为2OH-+Cl2=Cl-+ClO-+H2O;
Ⅱ.(3)准确称取5.000g漂白粉样品,研细,加蒸馏水溶解并冷却后,稀释至500mL需要在容量瓶中进行,配制过程需要经过溶解、转移、洗涤、定容摇匀等步骤,所用的玻璃仪器有烧杯、玻璃棒、500mL容量瓶、胶头滴管,故答案为500mL容量瓶;胶头滴管;
(4)加入H2O2水溶液,搅拌至不再产生气泡,是利用过氧化氢的还原性还原次氯酸根离子生成氯离子,过氧化氢被氧化为氧气,反应的离子方程式为:ClO-+H2O2=Cl-+O2↑+H2O,故答案为ClO-+H2O2=Cl-+O2↑+H2O;
(5)加入适量K2CrO4溶液作为指示剂,以0.1000molL-1AgNO3标准溶液滴定至终点,滴定终点的现象是:当滴入最后一滴标准液,溶液中出现砖红色Ag2CrO4沉淀,且半分钟内不消失,故答案为当滴入最后一滴标准液,溶液中出现砖红色沉淀,且半分钟内不消失;
(6)准确称取5.000g漂白粉样品,研细,加蒸馏水溶解并冷却后,稀释至500mL,移取25.00mL该试样溶液至锥形瓶中,调节pH,缓慢加入适量3% H2O2水溶液,搅拌至不再产生气泡。加入适量K2CrO4溶液作为指示剂,以0.1000molL-1AgNO3标准溶液滴定至终点,多次实验,测得消耗AgNO3标准溶液平均体积为25.00mL,氯元素守恒,得到该漂白粉总氯的百分含量=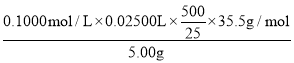 ×100%=35.5%,故答案为35.5%;
×100%=35.5%,故答案为35.5%;
(7)A.指示剂K2CrO4的用量过多,根据Ksp 可知,可能会导致消耗标准溶液的体积偏小,滴定结果可能偏低,故A错误;B.在滴定终点读取滴定管刻度时,俯视标准液液面,导致消耗标准溶液的体积偏小,测定结果偏低,故B错误;C.滴定前滴定管尖嘴部分有气泡,滴定后消失,导致消耗标准溶液的体积偏大,测定结果偏高,故C正确;故答案为C。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
【题目】呋喃酚是生产呋喃丹、好安威等农药的主要中间体,是高附加值的精细化工产品.一种以邻氯苯酚(A)为主要原料合成呋喃酚(F)的流程如下:
![]()

回答下列问题:
(1)A 物质核磁共振氢谱共有 个峰,④的反应类型是 ,C和D中含有的相同官能团的名称是 .
(2)下列试剂中,能和D反应的有 (填标号).
A.溴水 B.酸性K2Cr2O7溶液 C.FeC12溶液 D.纯碱溶液
(3)写出反应①的化学方程式是 (有机物用结构简式表示,下同).
(4)有机物B可由异丁烷经三步反应合成:异丁烷![]() X
X![]() Y
Y![]()
![]() 有机物B条件a为 ,Y生成B的化学方程式为 .
有机物B条件a为 ,Y生成B的化学方程式为 .
(5)呋喃酚的同分异构体很多,写出符合下列条件的所有同分异构体的结构简式
①苯环上的一氯代物只有一种
②能发生银镜反应的芳香酯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下的化学反应CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度的关系如下表,根据以上信息推断以下说法正确的是( )
CO(g)+H2O(g),其化学平衡常数K和温度的关系如下表,根据以上信息推断以下说法正确的是( )

A.此反应为放热反应
B.此反应只有达到平衡时,密闭容器中的压强才不会变化
C.此反应达到1 000 ℃时的反应速率比700 ℃时大
D.该反应的化学平衡常数越大,反应物的转化率越低
查看答案和解析>>
科目:高中化学 来源: 题型:
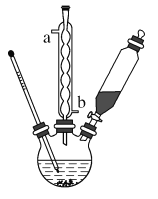
【题目】苯甲酸钠是一种常见食品防腐剂。实验室制备苯甲酸的装置图和有关数据如下:
相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
甲苯 | 92 | -94.9 | 110.6 | 难溶于水 |
苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
苯甲酸钠 | 144 | ---- | 249.3 | 易溶于水 |
(1)制备苯甲酸:在三颈烧瓶中加入4mL甲苯和20mL稀硫酸,放入碎瓷片后,加热至沸腾,加入12.8g高锰酸钾,加热到甲苯层消失。将三颈烧瓶在冰水浴中冷却,分离出苯甲酸。
①球形冷凝管的作用是_________,其进水口是________(填“a”或“b”)。
②已知三颈烧瓶中反应的离子方程式为![]() +6MnO4-+18H+→
+6MnO4-+18H+→![]() +6Mn2++14H2O,在该反应中体现了甲苯____性。
+6Mn2++14H2O,在该反应中体现了甲苯____性。
③分离苯甲酸选用的玻璃仪器除玻璃棒、烧杯外还有________(填字母)。
A.分液漏斗 B.漏斗 C.蒸馏烧瓶 D.直形冷凝管
④分离出粗品苯甲酸晶体中可能含有的杂质是MnSO4和___,为进一步提纯,应采用的操作方法是______。
(2)制备苯甲酸钠:控制温度为70℃,向三颈烧瓶中加入61.0g苯甲酸和适量的32%碳酸钠溶液,充分反应后停止加热。在深色的溶液中加入活性炭,并将混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体。
⑤控制温度为70℃的方法是_______。
⑥加入活性炭的作用是___________。
⑦若提纯得到46.8g苯甲酸钠,则苯甲酸钠的产率________。(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表:
化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 溶解度g/l00g水 |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
操作如下:
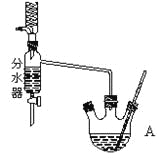
①在50mL三颈烧瓶中投入几粒沸石,将18.5 mL正丁醇和13.4 mL冰醋酸(过量),3~4滴浓硫酸按一定顺序均匀混合,安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管。
②将分水器分出的酯层和反应液一起倒入分液漏斗中依次用水洗,10% Na2CO3洗,再水洗,最后转移至锥形瓶并干燥。
③将干燥后的乙酸正丁酯加入烧瓶中,常压蒸馏,收集馏分,得15.1 g乙酸正丁酯。
请回答有关问题:
(1)写出任意一种正丁醇同类的同分异构体的结构简式___________。
(2)仪器A中发生反应的化学方程式为___________________。
(3)步骤①向三颈烧瓶中依次加入的药品是:__________________。
(4)步骤②中,用 10%Na2CO3溶液洗涤有机层,该步操作的目的是____________。
(5)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏___,(填“高”或“低”)原因是__。
(6)该实验生成的乙酸正丁酯的产率是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭被人们誉为黑色的“金子”,它是人类使用的主要能源之一。为了提高煤的利用率,减少有害气体的排放,人们采取了各式各样的方法。
(1)煤的气化和液化可能提高煤的利用率。煤的气化技术的主要产物是___________。煤的液化技术又分为直接液化和间接氧化.将煤隔绝空气加强热得到焦炉气、煤焦油及焦炭等产品的技术称为___________。
(2)煤在燃烧前、后及燃烧过程中均可采取措施减少有害气体的排放.
①在燃烧前,可以采用微生物脱硫技术.原理如下:
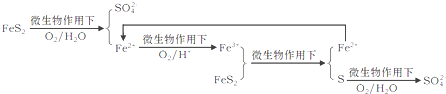
上述过程中Fe2+的作用为________________。写出Fe2+![]() Fe3+的离子方程式________________。
Fe3+的离子方程式________________。
②煤在燃烧时,进行脱硫处理,常采用________燃烧技术,在把煤和脱硫剂加入锅炉燃烧室,使煤与空气在流化过程中充分混合、燃烧,起到固硫作用.常用脱硫剂的主要化学成分为_______(填化学式)。
③煤在燃烧后,烟气净化常采用除尘技术和脱硫、脱硝技术.湿法脱硫、脱硝技术中将烟气通入_________设备,用石灰水淋洗。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。
(1)自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷锂铝石等。为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈________,可以认为存在锂元素。
A.紫红色 B.紫色 C.黄色
(2)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如下:

已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。

回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为________。
②为提高“酸化焙烧”效率,常采取的措施是________。
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为_______ 。(已知:完全沉淀后离子浓度低于1×l0-5) mol/L)
④“滤渣2”的主要化学成分为 _______。
⑤“沉锂”过程中加入的沉淀剂为饱和的 __________(化学式)溶液;该过程所获得的“母液”中仍含有大量的Li+,可将其加入到“ ___________”步骤中。
⑥Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为__________。
(3)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6![]() LixC6+Li1-xCoO2其工作原理如图2。
LixC6+Li1-xCoO2其工作原理如图2。
下列关于该电池的说法正确的是___________(填字母)。
A.过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流储能电池是一种新型的绿色环保储能系统(工作原理如图,电解液含硫酸)。该电池负载工作时,左罐颜色由黄色变为蓝色。

 4
4
下列说法错误的是
A.该电池工作原理为VO2++VO2++2H+![]() VO2++V3++H2O
VO2++V3++H2O
B.a和b接用电器时,左罐电动势小于右罐,电解液中的H+通过离子交换膜向左罐移动
C.电池储能时,电池负极溶液颜色变为紫色
D.电池无论是负载还是储能,每转移1 mol电子,均消耗1 mol氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+I2(g)![]() 2HI(g)△H=-14.9kJ·mol-1。某温度下,在体积均为2.0L的甲、乙两个恒容密闭容器中充入反应物,其起始物质的量如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的是( )
2HI(g)△H=-14.9kJ·mol-1。某温度下,在体积均为2.0L的甲、乙两个恒容密闭容器中充入反应物,其起始物质的量如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的是( )
起始物质的量 | n(H2)/mol | n(I2)/mol | n(HI)/mol |
甲 | 0.02 | 0.02 | 0 |
乙 | 0.04 | 0.04 | 0 |
A. 平衡时,乙中H2的转化率是甲中的2倍
B. 平衡时,甲中混合物的颜色比乙中深
C. 平衡时,甲、乙中热量的变化值相等
D. 该温度下,反应的平衡常数K=0.25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com