
【题目】25°C时有三瓶溶液:pH=3的盐酸、pH=3的醋酸溶液和pH=11的氢氧化钠溶液,下列说法不正确的是
A. 分别用pH=11的氢氧化钠溶液中和等体积pH=3盐酸和pH=3醋酸溶液至pH=7,所需氢氧化钠溶液的体积前者小于后者
B. 等体积pH=3的盐酸和pH=3醋酸的溶液中分别加入少量相同的锌粒,醋酸中锌粒先反应完
C. 三瓶溶液加水稀释100倍,pH变化最大的是醋酸溶液
D. 三瓶溶液中水电离出的c(H+)均为1.0×10-11mol·L-1
【答案】C
【解析】A项,pH都等于3的HCl和CH3COOH,CH3COOH的浓度大于HCl,pH=11的NaOH溶液与pH=3的盐酸等体积混合后溶液呈中性pH=7,pH=11的NaOH溶液和pH=3的醋酸溶液等体积混合后溶液呈酸性pH![]() ,则分别用pH=11的氢氧化钠溶液中和等体积pH=3的盐酸和pH=3的醋酸溶液至pH=7,所需氢氧化钠溶液的体积前者小于后者,正确;B项,等体积pH=3的盐酸和pH=3的醋酸溶液中分别加入少量相同的锌粒,开始反应速率相等,在醋酸溶液中存在电离平衡:CH3COOH
,则分别用pH=11的氢氧化钠溶液中和等体积pH=3的盐酸和pH=3的醋酸溶液至pH=7,所需氢氧化钠溶液的体积前者小于后者,正确;B项,等体积pH=3的盐酸和pH=3的醋酸溶液中分别加入少量相同的锌粒,开始反应速率相等,在醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,H+被消耗,电离平衡正向移动,在反应过程中醋酸溶液中H+浓度大于盐酸溶液中H+浓度,则反应过程中Zn与醋酸反应比与盐酸反应快,醋酸中锌粒先反应完,正确;C项,三瓶溶液加水稀释100倍,盐酸的pH变为5,NaOH溶液的pH变为9,加水稀释促进CH3COOH的电离,稀释后醋酸溶液的pH:3
CH3COO-+H+,H+被消耗,电离平衡正向移动,在反应过程中醋酸溶液中H+浓度大于盐酸溶液中H+浓度,则反应过程中Zn与醋酸反应比与盐酸反应快,醋酸中锌粒先反应完,正确;C项,三瓶溶液加水稀释100倍,盐酸的pH变为5,NaOH溶液的pH变为9,加水稀释促进CH3COOH的电离,稀释后醋酸溶液的pH:3![]() pH
pH![]() 5,pH变化最小的是醋酸溶液,错误;D项,酸溶液中OH-全部来自水电离,pH=3的盐酸和pH=3的醋酸溶液中水电离的c(H+)水=c(OH-)水=c(OH-)溶液=1
5,pH变化最小的是醋酸溶液,错误;D项,酸溶液中OH-全部来自水电离,pH=3的盐酸和pH=3的醋酸溶液中水电离的c(H+)水=c(OH-)水=c(OH-)溶液=1![]() 10-11mol/L,碱溶液中H+全部来自水电离,pH=11的NaOH溶液中水电离的c(H+)水=c(H+)溶液=1
10-11mol/L,碱溶液中H+全部来自水电离,pH=11的NaOH溶液中水电离的c(H+)水=c(H+)溶液=1![]() 10-11mol/L,正确;答案选C。
10-11mol/L,正确;答案选C。
c(H+) | c(酸) | 中和碱的能力 | 与足量活泼金属产生H2量 | 与活泼金属反应速率 | ||
开始 | 过程中 | |||||
盐酸 | 相同 | 小 | 小 | 小 | 相同 | 小 |
醋酸 | 大 | 大 | 大 | 大 | ||


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列变化不能通过一步反应直接完成的是( )
A.Al→Al3+B.Na2SO3→NaOHC.Al2O3→Al(OH)3D.Fe(OH)2→Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中将2molNaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(n)的取值范围是( )
A. n≥1 B. 1<n<2 C. 2≤n<4 D. n≥4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,下列说法错误的是( )
A.乙酸乙酯中含有18O
B.18O存在于水中
C.此反应属于取代反应
D.生成的乙酸乙酯的相对分子质量为90
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)![]() 2C(g) △H<0。t1 时刻达到平衡后,在t2 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2C(g) △H<0。t1 时刻达到平衡后,在t2 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
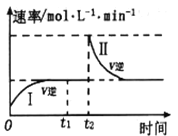
A. 0~t2时间段内,υ正> υ逆
B. I、Ⅱ两过程达到平衡时,A的体积分数I﹥II
C. t2时刻改变的条件可能是向密闭容器中加C
D. I、II两过程达到平衡时,平衡常数I﹤II
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应的反应物和产物如下:KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
(1)该反应的氧化剂是
(2)如果该反应方程式中I2和KIO3的系数都是5 ①KMnO4的系数是
②在下面的化学式上标出电子转移的方向和数目KMnO4+KI+H2SO4→
(3)如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组.原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. (1)下列条件的改变能增大活化分子百分数的是_____________。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=__________kJ·mol-1。
Ⅱ.2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。

已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示___________,E表示______________;该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,理由是____________ ;
(2)图中△H=_________kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com