
����Ŀ��������أ�K2FeO4����һ�����͡���Ч�������ɫˮ����������ҵ�������Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����ͣ�ʹ�������������
��1���ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ��2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2�����÷�Ӧ��Na2O2 ��___________��������������ԭ����
��2��ʪ���Ʊ�������صķ�Ӧ��ϵ������������Fe(OH)3��ClO����OH����FeO42-��Cl����H2O��
�ټ��������£��������ͻ�ԭ�������ʵ����ı�Ϊ3:2������Ӧ��д������ƽʪ���Ƹ�����ص����ӷ�Ӧ����ʽ��__________________��
������Ӧ������ת����0.3mol���ӣ���ԭ��������ʵ���Ϊ__________mol��
����֪��2Fe3����2I��=2Fe2����I2��2Fe2����Br2=2Fe3����2Br����
��1������1 mol FeI2��2 mol FeBr2����Һ��ͨ��2 mol Cl2����ʱ��������������______��
��2������a mol FeI2��b mol FeBr2����Һ��ͨ��c mol Cl2����I����Fe2����Br����ȫ������ʱ��c=__________���ú�a��b�Ĵ���ʽ��ʾ����
���𰸡�����������ԭ�� 2Fe��OH��3 + 3ClO- + 4OH-��2FeO42- + 3Cl- + 5H2O 0.15 I-��Fe2+ c=3(a+b)/2
��������
��1����Ӧ��FeԪ�ػ��ϼ���+2������Ϊ+6�ۣ���������FeSO4Ϊ��ԭ��������������OԪ�صĻ��ϼ��ɣ�1�۽���Ϊ��2�ۣ��ɣ�1������Ϊ0���������Ƽ���������Ҳ�ǻ�ԭ����
��2����ʪ���Ʊ��������(K2FeO4)����FeO42��Ϊ���Fe(OH)3Ϊ��Ӧ����ϼ������ܹ�3�ۣ��ɵ���ת���غ��֪��ClOΪ��Ӧ�ClΪ��������ϼ۽���2�ۣ����ϼ�������С������Ϊ6����Fe(OH)3��ϵ��Ϊ2��FeO42����ϵ��Ϊ2��ClO��ϵ��Ϊ3��Cl��ϵ��Ϊ3�����ݵ���غ��֪��OHΪ��Ӧ�ϵ��Ϊ4����Ԫ���غ��֪H2OΪ�������ϵ��Ϊ5�����ӷ���ʽΪ��2Fe��OH��3 + 3ClO- + 4OH-��2FeO42- + 3Cl- + 5H2O��
������Ӧ������ת����0.3mol���ӣ���ԭ��������ʵ���Ϊ![]() =0.15mol��
=0.15mol��
��1������1molFeI2��2molFeBr2����Һ��ͨ��2molCl2���ȷ�����Ӧ2I+Cl2=I2+2Cl��2mol��������ȫ��Ӧ��Ҫ����1mol��Ȼ������ӦCl2+2Fe2+=2Cl+2Fe3+��1mol������Ӧ��Ҫ�������ӵ����ʵ�����2mol����Һ�к���3mol�������ӣ��μӷ�Ӧ���������ӵ����ʵ�����2mol��������Һ�л�ʣ����������1mol�����Ա�������������2molI��2molFe2+��
��2��amolFeI2��ȫ������ת��3amol���ӣ�bmolFeBr2��ȫ������ת��3bmol���ӣ��ɵ�ʧ�����غ��֪����I��Fe2+��Br��ȫ������ʱ����������Ϊ0.5��(3a+3b)mol����c=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B����������Ԫ����ɵĻ����A��ij��Ԫ�ص���������Ϊ75% ��B��һ�ֵ���ɫ���壬C��J��ͬ����Ԫ�ص���̬�⻯�����C�Ǻ�������ߵ�����XΪ��ɫҺ�塣��Ӧ���ɵ�ˮ������ȥ������������ͼ��ʾ�Ĺ�ϵ��

��1��д����ѧʽ��A___________B____________J_____________��
��2����Ӧ����ÿ����1molF��ת�Ƶ��ӵ���ĿΪ��___________��
��3����Ӧ�ܵĻ�ѧ����ʽΪ��________________________________________________��
��4�����ӷ���ʽ�ֱ�Ϊ����Ӧ��__________________________________________��
��__________________________________________________________��
��5����Ӧ���У�ÿ1.00gC��������F���ã��ָ���25��ų�55.6kJ������д����Ӧ�ٵ��Ȼ�ѧ����ʽ__________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ�Һ�°����NaHCO3�ܽ�ȱ�NaCl��Na2CO3��NH4HCO3��NH4Cl��С�����ʣ�����CO2 + NH3 + H2O + NaCl = NaHCO3��+ NH4Cl�ķ�Ӧԭ���Ʊ������������ʵ���ҽ���ģ��ʵ�����������ʾ��ͼ��

�����������������( )
A.A������NH3��B������CO2
B.�ڢõ��ľ����Ƿ��ͷ۵���Ҫ�ɷ�
C.�ڢ����õ�����Ҫ�����������ձ���©����������
D.�ڢ�����������Ҫ�������ܽ⡢�������ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС������ȡCuO��֤��CuO�ܼӿ�KClO3�ķֽ����ʣ���Ʋ���������ʵ�飺
��һ����ȡCuO
�ٳ�ȡ2 g������ϸ������ձ�������������ˮ�ܽ⣻
�������������Һ����μ���NaOH��Һ��ͭ���ӳ�����ȫ��
�۽���������ó������ˡ�ϴ�ӣ����������أ���ϸ���á�
�ش��������⣺
��1������ʵ�鲽�����ܽ⡢����ʱ������������������_____________��
��2�������������ǰ������ɫ�ı仯Ϊ_______��
��3�����û�ѧ����֤��ͭ�����Ѿ�������ȫ�IJ�����____________��
������֤��CuO�ܼӿ�KClO3�ķֽ����ʣ�����MnO2�Ĵ�Ч�ʽ��бȽ�
����ͼװ�ý���ʵ�飬�Ҿ���������ͬ״����20 mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԣ�������ݼ��±���

ʵ����� | KClO3���� | ������������ | �������� |
�� | 1.5 g | ���������� | |
�� | 1.5 g | CuO 0.5 g | |
�� | 1.5 g | MnO2 0.5 g |
��4������ʵ���еĴ�������ָ_____________����ʵ�������˼·�⣬������ͨ���ⶨ______________���Ƚ�CuO��MnO2�Ĵ�Ч�ʡ�
��5����ʵ��װ��ͼ������װ�����齺�ܺ�����A_______________�������ƣ���50 mL___________��������ʽ��������ʽ�����ζ��ܸ������װ���ɣ�
��6��Ϊ̽��CuO��ʵ������Ƿ�������ã��貹������ʵ�飺
a��CuO��������û�иı䣻
b��CuO�Ļ�ѧ������û�иı䡣
������֤CuO�����Ƿ�ı�IJ�������_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʼ䷢����Ӧ�����ĵ����ʵ������ᣬ��������������
A. ľ̿��Ũ����B. ͭ��ϡ����C. п��ϡ����D. ľ̿��Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeSO4��һ�־�ϸ������Ʒ������������ȱ����ƶѪ���Ƹľ�ķ����ȡ��Ʊ����裺����3mol��L-1�������������ȣ�����ʹ���ַ�Ӧ�������ȹ��ˣ�����50�������������ᾧ���õ����塪���̷���FeSO4��7H2O�����ش��������⣺
��1���Ʊ�FeSO4��Һʱһ�㲻�ý�Ũ�������3mol��L-1�����ԭ����___________����ӦʱҪ�����۹�����������__________��
��2�����鲽����������Һ�н��������ӵķ�����_________��
��3�����������ȹ��˵�ԭ����__________��
��4���ڿ����м����̷��������������¶ȱ仯��������ͼ��
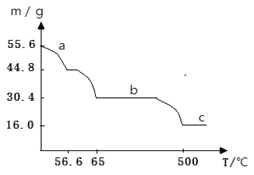
a���߶�Ӧ�ķ�Ӧ��ѧ����ʽΪ____________��
c���߶�Ӧ�����ʻ�ѧʽΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���Ƿ���ȷ
��1�� | ��2�� | ��3�� | ��4�� |
___ | ___ | ___ | ___ |
��1��22.4LO2��һ������6.02��1023��������
��2����80gNaOH����1Lˮ�У�������Һ��NaOH�����ʵ���Ũ��Ϊ2mol/L
��3��18gH2O�ڱ�״���µ������22.4L
��4���ڱ�״��ʱ��20mLNH3��60mLO2�����ķ��Ӹ�����Ϊ1��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���Ľṹ��ʽ��ͼ��ʾ�����й��ڸ��л��������˵��������ǣ� ��
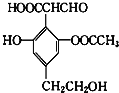
A. 1mol�����ʿ���4mol����������Һ��Ӧ
B. ��NaHCO3��Һ��Ӧ���Բ���CO2����
C. ��������H2��Ӧ��1mol�������������3mol H2
D. �����ʿ���ʹ����KMnO4��Һ��ɫ��Ҳ�ɷ�����ȥ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.2 mol NaOH��0.1 mol Ba(OH)2����Һ�г����ȶ���ͨ��CO2���壬��ͨ����������Ϊ6.72 L����״���£�ʱ����ֹͣ��������һ�����У���Һ�����ӵ����ʵ�����ͨ��CO2����������ϵ��ȷ��ͼ���ǣ�������ܽ���Բ��ƣ��� ��
A.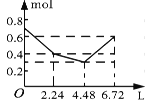 B.
B. C.
C.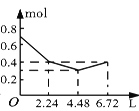 D.
D.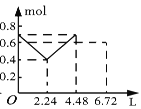
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com