
【题目】肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。
(1)已知在101 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气和水,放出热量624 kJ(25 ℃时),N2H4完全燃烧的热化学方程式是__________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时,正极的反应式是___________________________;负极的反应式是____________________________。
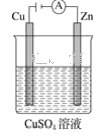
(3)下图是一个电化学过程示意图。
①锌片上发生的电极反应式是_________________________________________________。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气______L(假设空气中氧气体积分数为20%)。
(4)有同学想把Ba(OH)2·8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”)
【答案】 N2H4(l)+O2(g)===N2(g)+2H2O(l) ΔH=-624 kJ·mol-1 O2+4e-+2H2O===4OH- N2H4+4OH--4e-===N2↑+4H2O Cu2++2e-===Cu 112 否
【解析】(1)32.0 g N2H4即1molN2H4在氧气中完全燃烧生成氮气和水,放出热量624 kJ(25 ℃时), N2H4(l)+O2(g)===N2(g)+2H2O(l) ΔH=-624 kJ·mol-1 ;(2)燃料电池中,正极上是氧气发生得电子的还原反应,在碱性环境下,电极反应式为:2H2O+O2+4e-=4OH-;负极上投放的是燃料,负极上燃料失电子发生氧化反应,在碱性环境下的反应式为:N2H4+4OH--4e-=4H2O+N2↑。(3)①与电源负极相连的是电解池的阴极,在阴极上阳离子铜离子发生得电子的还原反应,即Cu2++2e-=Cu;②铜片上的电极反应为:Cu-2e-=Cu,Cu的质量变化128g,根据电极反应,转移电子为4mol,根据反应N2H4+O2=N2+2H2O,当转移电子4mol时,消耗氧气的物质的量是1mol,氧气的体积是空气体积的五分之一,所以消耗空气的体积是5mol,即112L;(4)Ba(OH)2·8H2O晶体与NH4Cl晶体的反应不是自发的氧化还原反应,不能设计成原电池。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化学与生活、生产和社会发展密切相关。下列说法正确的是
A. 《天工开物》中“凡石灰,经火焚炼而用”里的石灰,指的是Ca(OH)2
B. 某品牌的八宝粥不含任何糖类物质,糖尿病人可以放心食用
C. 未成熟的苹果肉遇碘酒变蓝,成熟苹果的汁液不能与银氨溶液反应
D. 用氯化铁溶液洗涤银镜反应后的试管比用硫酸铁溶液效果好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是( )
A.作还原剂
B.作氧化剂
C.既作氧化剂又作还原剂
D.既不作氧化剂又不作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氢吡喃(DHP)常用作有机合成中的保护基。
(1)按照如下路线可以制得DHP。

①单糖A的分子式为_____, DHP分子的核磁共振氢谱有_____组峰。
②1mol糠醛与3mol H2反应转化为B,则B的结构简式为_____。
③ DHP的同分异构体中,属于链状有机物且能发生银镜反应的有_____种。
(2)已知:i. DHP的保护和脱保护机理为
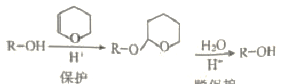
ii. R-C≡CNa + R1OH → R-C≡CH + R1ONa
iii. R-C≡CNa + R1Br → R-C≡C-R1+ NaBr
应用DHP作保护基合成梨小食心虫性外激素的路线如下:
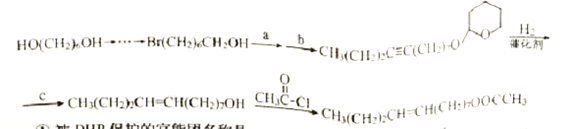
①被DHP保护的官能团名称是_______,保护反应的类型是 ______。
②上述路线中最后一步反应的方程式为 ______。
③上述路线中步骤a、b、c分别为_______、 ______、_______。(例:  )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是( )
A. 0.1mol·L-1Na2S溶液中:2[Na+]=[S2-]+[HS-]+[H2S]
B. 0.1mol·L-1NaHSO4溶液中:[Na+]>[SO42-]>[H+]>[OH-]
C. Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4)+2c(H2C2O4)
D. CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、选择下列实验方法分离物质,将分离方法的字母填在横线上。
A.萃取分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法 F.升华法
(1)______________分离饱和食盐水与沙子的混合物。
(2)______________分离水和汽油的混合物。
(3)______________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
(4)_____________从碘的水溶液里提取碘。
Ⅱ、蒸馏是实验室制备蒸馏水的常用方法。
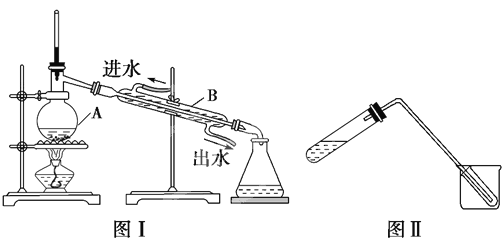
(1)图Ⅰ是实验室制取蒸馏水的常用装置,图中明显的错误是_____________________。
(2)仪器A的名称是______________,仪器B的名称是______________。
(3)实验时A中除加入少量自来水外,还需加入少量________________,其作用是________________________________________。
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图Ⅰ完全相同。该装置中使用的玻璃导管较长,其作用是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,溶液体积均为200 ml ,开始时,电解质溶液的浓度均为0.1 mol·L-1 ,工作一段时间后,测得导线上通过了0.02 mol 电子,若不考虑溶液体积的变化,下列叙述中正确的是( )
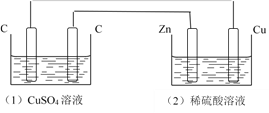
A. (1)、(2)两装置均为电解池
B. (1)、(2)溶液的PH均减小
C. (1)中阳极电极反应式为:4OH--4e-===2H2O+O2↑
D. (1)中阴极上析出0.32 g Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com