
| A. | 实验室制取氧气 | B. | 萃取碘水中的碘 | ||
| C. | 粗盐提纯 | D. | 用海水制取蒸馏水 |
科目:高中化学 来源: 题型:解答题
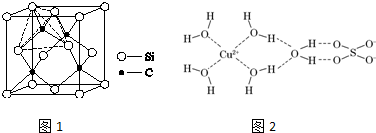
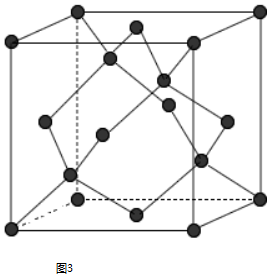
 ;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.
;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
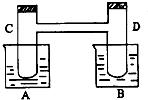 如图所示,在烧杯A中盛有20℃,50毫升水,B中盛有1摩/升盐酸50毫升,试管C、D相通,其中盛有红棕色气体,它处于下列平衡状态,2NO2?N2O4(△H<0,放热).当向A中加入50克硝酸铵使其溶解,往B中加入2克苛性钠,也使其溶解时,问:(注:硝酸铵溶于水吸热)
如图所示,在烧杯A中盛有20℃,50毫升水,B中盛有1摩/升盐酸50毫升,试管C、D相通,其中盛有红棕色气体,它处于下列平衡状态,2NO2?N2O4(△H<0,放热).当向A中加入50克硝酸铵使其溶解,往B中加入2克苛性钠,也使其溶解时,问:(注:硝酸铵溶于水吸热)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
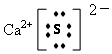 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.7mol/L | B. | 12.7mol/L | C. | 13.7mol/L | D. | 14.7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 用小苏打治疗胃酸(盐酸)过多:HCO3-+H+═CO2↑+H2O | |
| D. | CaCO3溶于稀硝酸中:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com