
【题目】甲醇(CH3OH)热值高、无污染,既可做燃料,又是重要的化工原料。科学家正研究利用CO2生产甲醇以发展低碳经济。
(1)已知CO(g)和CH3OH(l)的燃烧热分别为283kJmol-1和726kJmol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为______。
(2)根据甲醇在酸性电解质溶液中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池,则其负极反应式为______。若该燃料电池消耗1mol甲醇所能产生的最大电能为689.7kJ,与其燃烧所能释放的全部能量相比,该燃料电池的理论效率为______。
(3)探究不同条件下对合成甲醇反应的影响:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。
①其他条件不变,T1、T2两种温度下CH3OH的物质的量随时间的变化如图,则该反应在T1时的平衡常数比T2时的______(填“大”、“小”),处于A点的反应体系从T1变到T2,达到平衡时 ______(填“增大”、“减小”或“不变”)。
______(填“增大”、“减小”或“不变”)。
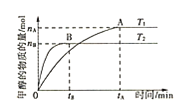
②某温度下,在体积为1L的密闭容器中加入4molCO2、8molH2,测得H2的物质的量随时间变化如图曲线(甲)所示:

则a→b时间段内v(CH3OH)=______molL-1min-1;若仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线(乙)所示。曲线(乙)对应改变的实验条件可以是______(填序号)。
A.加催化剂 B.增大压强 C.升高温度 D.增大CO2浓度
若图中曲线甲平衡后保持恒温恒容,按如表各组的物质的量再次增加投入反应混合物,其中平衡向正反应方向进行的是______。
物质 | n(CO2) | n(H2) | n(CH3OH) | n(H2O) |
A | 0 | 0 | 1 | 1 |
B | 1 | 0 | 1 | 0 |
C | 0 | 1 | 1 | 0 |
【答案】CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-443kJmol-1 CH3OH-6e-+H2O=CO2+6H+ 95% 大 增大 0.5 BD C
【解析】
(1)根据CO(g)和CH3OH(l)的燃烧热,写出热化学方程式,再根据盖斯定律分析解答;
(2)燃料电池中,通入燃料的电极做负极,则负极为甲醇放电生成CO2,据此书写电极反应式;燃料电池的理论效率=![]() ×100%;
×100%;
(3)①根据图象,结合平衡移动原理进行分析;②由图可知:a→b时间段内,△n(H2)=3mol,△t=2min,据此计算v(H2)=,v(CH3OH)=![]() v(H2);根据影响化学平衡的因素分析判断;先根据三段式求出平衡常数K,再根据Qc与K比较判断平衡移动的方向。
v(H2);根据影响化学平衡的因素分析判断;先根据三段式求出平衡常数K,再根据Qc与K比较判断平衡移动的方向。
(1)CO(g)的燃烧热的热化学方程式为:①CO(g)+![]() O2(g)=CO2(g) △H=-283kJmol-1;CH3OH(l)的燃烧热的热化学方程式为:②CH3OH(l)+
O2(g)=CO2(g) △H=-283kJmol-1;CH3OH(l)的燃烧热的热化学方程式为:②CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) △H=-726kJmol-1,根据盖斯定律:反应②-反应①即可得甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-726kJmol-1+283kJmol-1 = -443kJmol-1,故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-443kJmol-1;
O2(g)=CO2(g)+2H2O(l) △H=-726kJmol-1,根据盖斯定律:反应②-反应①即可得甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-726kJmol-1+283kJmol-1 = -443kJmol-1,故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-443kJmol-1;
(2)对于燃料电池,燃料做负极,则负极为甲醇放电生成CO2,根据电子转移、电荷守恒,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;该燃料电池的理论效率=![]() ×100%=95%,故答案为:CH3OH-6e-+H2O=CO2+6H+;95%;
×100%=95%,故答案为:CH3OH-6e-+H2O=CO2+6H+;95%;
(3)①由图可知,T1温度下,平衡时甲醇的物质的量更多,所以T1时的平衡常数比T2时的大;T2温度下反应先达平衡,则T2>T1,且甲醇的物质的量减少,说明平衡逆移,正反应为放热反应,处于A点的反应体系从T1变到T2,相当于升高温度,平衡逆移,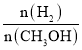 增大,故答案为:大;增大;
增大,故答案为:大;增大;
②由图可知:a→b时间段内,△n(H2)=3mol,△t=2min,则v(H2)=![]() =
=![]() =
=![]() =1.5mol/(Lmin),v(CH3OH)=
=1.5mol/(Lmin),v(CH3OH)=![]() v(H2)=0.5mol/(Lmin);A、加入催化剂,平衡不移动, H2平衡的物质的量不变,故A错误;B、增大压强,反应速率加快,平衡正移,H2的物质的量减小,符合图象变化,故B正确;C、升高温度,反应速率加快,平衡逆移,H2的物质的量增大,不符合图象变化,故C错误;D、增大CO2浓度,反应速率加快,平衡正移,H2的物质的量减小,符合图象变化,故D正确;故选BD;
v(H2)=0.5mol/(Lmin);A、加入催化剂,平衡不移动, H2平衡的物质的量不变,故A错误;B、增大压强,反应速率加快,平衡正移,H2的物质的量减小,符合图象变化,故B正确;C、升高温度,反应速率加快,平衡逆移,H2的物质的量增大,不符合图象变化,故C错误;D、增大CO2浓度,反应速率加快,平衡正移,H2的物质的量减小,符合图象变化,故D正确;故选BD;
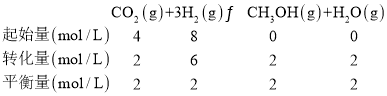
平衡常数K=![]() =
=![]() =0.25(mol/L)-2,A、只加生成物,则平衡逆移,故A错误;B、Qc=
=0.25(mol/L)-2,A、只加生成物,则平衡逆移,故A错误;B、Qc=![]() =0.25=K,平衡不移动,故B错误;C、Qc=
=0.25=K,平衡不移动,故B错误;C、Qc=![]() =0.11<K,平衡正移,故C正确;故选C,故答案为:0.5;BD;C。
=0.11<K,平衡正移,故C正确;故选C,故答案为:0.5;BD;C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某同学欲利用如图装置制取能较长时间存在的Fe(OH)2,其中实验所用溶液现配现用且蒸馏水先加热煮沸。下列分析正确的是
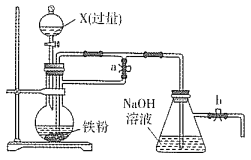
A. X可以是稀硫酸或稀硝酸或稀盐酸
B. 实验开始时应先关闭止水夹a、打开b,再向烧瓶中加入X
C. 反应一段时间后可在烧瓶中观察到白色沉淀
D. 反应结束后若关闭b及分液漏斗活塞,则Fe(OH)2可较长时间存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在电解冶炼铝的过程中加入冰晶石(Na3AlF6)可起到降低Al2O3熔点的作用。
(1)基态氟原子中,电子占据的最高能层的符号为______,电子占据最高能级上的电子数为______。
(2)向NaAlO2及氟化钠溶液中通入CO2,可制得冰晶石。
①该反应中涉及的非金属元素的电负性由大到小的顺序为______________。
②1molCO2中含有的σ键数目为________,其中C原子的杂化方式为_________;CO2与SCNˉ互为等电子体,SCNˉ的电子式为_________。
③Na2O的熔点比NaF的高,其理由是:_________。
(3)冰晶石由两种微粒构成,冰晶石的晶胞结构如图所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处△所代表的微粒是________(填微粒符号)。
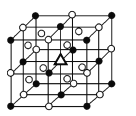
(4)冰晶石稀溶液中存在的化学键有________(填标号)。
A 离子键 B 共价键 C 配位键 D 氢键
(5)金属铝晶体中的原子堆积方式为面心立方最密堆积,其晶胞参数为apm,则铝原子的半径为______pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学模拟工业制碘的方法,探究ClO3-和I-的反应规律。实验操作及现象如下:
实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
| 1 | 0.05mL | 浅黄色 | 无色 |
2 | 0.20mL | 深黄色 | 无色 | |
3 | 0.25mL | 浅黄色 | 蓝色 | |
4 | 0.30mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如下实验:
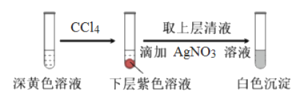
经检验,上述白色沉淀是AgCl。写出加入0.20mLNaClO3后,溶液中ClO3-和I-发生反应的离子方程式____________。
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2,反应的离子方程式是______________________。
进行实验:取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有IO3-。其中试剂X可以是_________(填字母序号)。
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
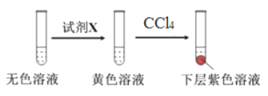
获得结论:NaClO3溶液用量增加导致溶液褪色。
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如下实验结果:
编号 | 6.0mol·L-1H2SO4溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
5 | 0.25mL | 浅黄色 | 无色 |
6 | 0.85mL | 无色 | 蓝色 |
①对比实验4和5,可以获得的结论是______________________。
②实验6中ClO3-和I-反应的离子方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种淡黄色粉末,易溶于水,不溶于乙醇。在实验室制备连二亚硫酸钠流程如下:
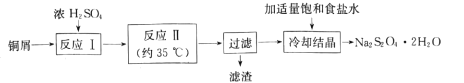
(1)反应Ⅰ是制备SO2,下图装置可制取纯净干燥的SO2:
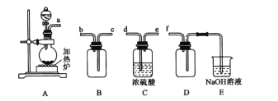
①按气流方向连接各仪器接口,顺序为a→ ___→f,装置D的作用是______。
②装置A中反应的化学方程式为___。
(2)反应Ⅱ所用实验装置如图所示(部分装置省略)。
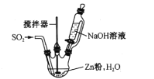
①通SO2之前先强力搅拌,将锌粉和水制成悬浊液,其目的是_________;控制反应温度的方法是____
②反应Ⅱ的离子方程式为 ___。
(3)“滤渣”经洗涤、灼烧,可得到一种工业产品是____(填化学式);加入适量饱和食盐水的目的是 ___。
(4)产品Na2S2O42H2O久置空气中易被氧化,其氧化产物可能是_______(写2种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“宏观——微观——符号”之间建立联系是化学学科特有的思维方式。如图是科研人员提出的HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程示意图(图中只画出了HAP的部分结构)。下列说法不正确的是
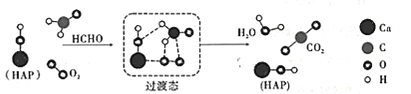
A.HAP能降低HCHO与O2反应的活化能
B.该反应的化学方程式为HCHO+O2![]() CO2+H2O
CO2+H2O
C.反应过程中断裂或生成的的化学键类型均为极性共价键
D.产物CO2分子中的氧原子不仅仅来源于O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的表达式正确的是
A. 乙炔分子的比例模型示意图:![]()
B. 2-甲基-2-戊烯的键线式:![]()
C. ![]() 的名称:3-甲基-1-丁烯
的名称:3-甲基-1-丁烯
D. 1,3-丁二烯的分子式:C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上将石灰石和硫煤混合使用,称之为“固硫”,其反应原理为:2CaCO3(s)+2SO2(g)+O2(g)![]() 2CaSO4(s)+2CO2(g) △H1=akJ·mol-1。
2CaSO4(s)+2CO2(g) △H1=akJ·mol-1。
已知:CaO(s)+CO2(g)![]() CaCO3(s) △H2=bkJ·mol-1;
CaCO3(s) △H2=bkJ·mol-1;
2SO2(g)+O2(g)![]() 2SO3(g) △H3=ckJ·mol-1。
2SO3(g) △H3=ckJ·mol-1。
请回答下列问题:
(1)CaSO4(s)![]() CaO(s)+SO3(g)△H=___kJ·mol-1(用a、b、c表示)。
CaO(s)+SO3(g)△H=___kJ·mol-1(用a、b、c表示)。
(2)T1℃时,向某恒容密闭容器中通入一定量的CO2和足量CaO发生反应:CaO(s)+CO2(g)![]() CaCO3(s),CO2的浓度随时间变化如图所示:
CaCO3(s),CO2的浓度随时间变化如图所示:
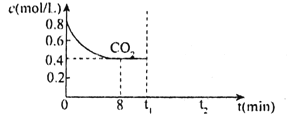
①0~8min,v(CO2)=___。
②t1min时,若保持其他条件不变,压缩容器体积至原来的![]() ,t2min重新达到平衡,请在图中画出CO2的浓度自条件改变至新平衡的变化曲线___。
,t2min重新达到平衡,请在图中画出CO2的浓度自条件改变至新平衡的变化曲线___。
(3)T2℃时,向某密闭容器中通入2molSO2和1molO2发生反应:2SO2(g)+O2(g)![]() 2SO3(g) △H3=ckJ·mol-1。
2SO3(g) △H3=ckJ·mol-1。
①若该容器为恒压密闭容器,下列选项可判断反应已达平衡状态的是___。
A.混合气体的密度不再改变
B混合气体的压强不再改变
C.相同时间内,每断裂0.1molO=O键,同时生成0.2molSO3
D.混合气体的平均相对分子质量不再改变
②若该容器为2L的恒容密闭容器,达平衡时SO3的体积分数为40%,则O2的转化率为___,T2℃时该反应的平衡常数K=___。
③反应达到②中的平衡状态后,保持反应温度和O2的浓度不变,增大容器体积,则平衡将___(填“正向”、“逆向”或“不“)移动,原因为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com