
【题目】向2L的密闭容器中充入7.6mol NO和3.8mol O2 , 发生如下反应: ①2NO(g)+O2(g)2NO2(g)
②2NO2(g)N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )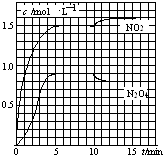
A.前5min反应的平均速率v(N2O4)=0.36mol(Lmin)﹣1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , T1℃达到平衡时,N2O4的转化率为10%
【答案】D
【解析】解:A、前5min反应的平均速率v(N2O4)= ![]() =
= ![]() =0.18mol(Lmin)﹣1 , 故A错误; B、T1℃时反应②的化学平衡常数K=
=0.18mol(Lmin)﹣1 , 故A错误; B、T1℃时反应②的化学平衡常数K= ![]() =
= ![]() =0.4L/mol,故B错误;
=0.4L/mol,故B错误;
C、在该题中,升高温度后,二氧化氮的浓度增加,四氧化二氮的浓度减小,所以平衡②逆向移动,该反应是放热的,故C错误;
D、若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , 则Qc=0.31<K,所以反应正向进行,T1℃达到平衡时,
2NO2(g) | N2O4(g) | |
初始: | 1.8 | 1.0 |
变化: | 2x | X |
平衡: | 1.8-2x | 1.0+x |
则 ![]() =0.4,解得x=0.1,即N2O4的转化率为10%,故D正确.
=0.4,解得x=0.1,即N2O4的转化率为10%,故D正确.
故选D.
A、根据化学反应速率v= ![]() 来计算化学反应速率;
来计算化学反应速率;
B、化学平衡常数K= ![]() ,代入相关数据来计算即可;
,代入相关数据来计算即可;
C、根据温度对化学平衡移动的影响:升高温度,化学平衡向着吸热方向进行,反之向着放热方向进行,据此来判断反应的吸放热;
D、根据转化率= ![]() 来计算即可.
来计算即可.


科目:高中化学 来源: 题型:
【题目】下列实验方法中不正确的是( )
A.用水萃取溴乙烷中的乙醇
B.通过常压分馏分离煤油和柴油
C.用目视比色法粗测Na2CO3溶液的浓度
D.利用烧碱溶液鉴别MgCl2和AlCl3两种溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,将X溶液逐滴加入固体Y中,装置B的试管中的现象不正确的是( )
选项 | X溶液 | 固体Y | Z溶液 | 现象 |
|
A | 稀硫酸 | 亚硫酸氢钠 | 品红试剂 | 品红褪色 | |
B | 浓氨水 | CaO | 紫色石蕊试液 | 溶液变红 | |
C | 盐酸 | 石灰石 | 硅酸钠溶液 | 出现白色沉淀 | |
D | 双氧水 | MnO2 | 氢硫酸溶液 | 产生浑浊 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
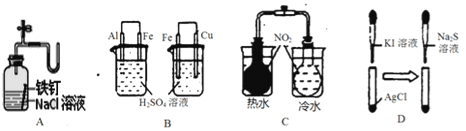
【题目】下列实验过程中的现象及结论均正确且存在因果关系的是
实验 | 实验现象 | 结论 |
A | 广口瓶中光亮的铁钉放置一段时间后生锈 | 铁钉发生析氢腐蚀 |
B | 左烧杯铁表面冒气泡,右烧杯铜表面冒气泡 | 金属活动性:Al>Fe>Cu |
C | 左烧杯气体颜色加深,右烧杯气体颜色变浅 | 2NO2(g) |
D | 白色固体先变为黄色,后变为黑色 | Ksp:AgCl<AgI<Ag2S |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】准确量取25.00 mL高锰酸钾溶液,可选用的仪器是( )
A.50 mL量筒
B.10 mL量筒
C.50 mL酸式滴定管
D.50 mL碱式滴定管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列几种情况,对中和滴定结果无影响的是 ( )
A.滴定管用蒸馏水洗后注入标准液
B.滴定管尖端未充满液体
C.滴定管中标准液在零刻度以上
D.盛未知浓度溶液的锥形瓶中有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的化合物是优良的催化剂,可用于干电池原料生产等.
(1)锌锰干电池的反应为2MnO2+Zn+2NH4Cl=2MnO(OH)+Zn(NH3)2Cl2 , MnO(OH)中锰元素的化合价为 .
(2)向废电池还原后的废液(含有Mn2+、Fe2+、Zn2+等)中逐滴滴加Na2S溶液,最先生成的沉淀为(填化学式).[已知Ksp(MnS)=1.4×10﹣15 , Ksp(ZnS)=2.9×10﹣25 , Ksp(FeS)=6.0×10﹣18]
(3)Mn2+催化H2O2分解:2H2O2(l)=2H2O(l)+O2(g)△H1 , 其反应机理如图:
①已知反应Ⅱ为MnO2(s)+H2O2(1)+2H+ ( aq)=Mn2+ (aq)+O2(g)+2H2O(1)△H2 . 写出反应 I的热化学方程式(焓变用△H1和△H2表示): .
②某温度时,向10mL0.4mol/L H2O2液中滴入1滴MnSO4发生分解:2H2O2=2H2O+O2 , 测得不同时刻生成O2的体积(已折算为标准状况下的体积)如表:
t/min | 0 | 2 | 4 | 6 |
V(O2)mL | 0 | 9.9 | 17.2 | 22.4 |
0~2min时反应速率比2~4min时的快,其原因是 , 0~6min的平均反应速率v(H2O2)=(忽略溶液体积的变化).
(4)锰基催化剂是合成甲醇、二甲醚的催化剂.已知:
反应 | 平衡常数KP | |
773K | 873K | |
Ⅰ.CO2(g)+4H2(g)CH4(g)+2H2(g) | 19.4 | 0.803 |
Ⅱ.CO2(g)+3H2(g)CH3OH(g)+H2O(g) | 6.07×10-9 | 3.65×10-9 |
①反应I的正反应是(填“放热”或“吸热”)反应.
②反应Ⅱ的平衡常数表达式为 . 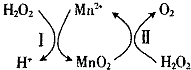
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化物的叙述正确的是( )
A. 金属氧化物都是碱性氧化物
B. 酸性氧化物均可与碱反应
C. 酸性氧化物都是非金属氧化物
D. 氧化铜是碱性氧化物,可与水反应生成Cu(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:在酸性条件下发生的反应为AsO43﹣+2I﹣+2H+═AsO33﹣+I2+H2O,在碱性条件下发 生的反应为AsO33﹣+I2+2OH﹣═AsO43﹣+H2O+2I﹣ . 设计如图装置(C1、C2均为石墨电极),分别进行下述操作: Ⅰ.向B烧杯中逐滴加入浓盐酸,发现电流表指针发生偏转
Ⅱ.若改向B烧杯中逐滴加入40% NaOH溶液 发现电流表指针偏转方向与Ⅰ相反. 试回答下列问题:
(1)两次操作过程中指针偏转方向为什么相反?试用化学平衡移动原理解释 .
(2)操作Ⅰ过程中C1棒为极,发生的电极反应为 .
(3)操作Ⅱ过程中C2棒为极,发生的电极反应为 . 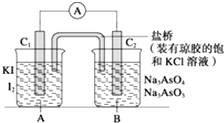
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com