
【题目】锰的化合物是优良的催化剂,可用于干电池原料生产等.
(1)锌锰干电池的反应为2MnO2+Zn+2NH4Cl=2MnO(OH)+Zn(NH3)2Cl2 , MnO(OH)中锰元素的化合价为 .
(2)向废电池还原后的废液(含有Mn2+、Fe2+、Zn2+等)中逐滴滴加Na2S溶液,最先生成的沉淀为(填化学式).[已知Ksp(MnS)=1.4×10﹣15 , Ksp(ZnS)=2.9×10﹣25 , Ksp(FeS)=6.0×10﹣18]
(3)Mn2+催化H2O2分解:2H2O2(l)=2H2O(l)+O2(g)△H1 , 其反应机理如图:
①已知反应Ⅱ为MnO2(s)+H2O2(1)+2H+ ( aq)=Mn2+ (aq)+O2(g)+2H2O(1)△H2 . 写出反应 I的热化学方程式(焓变用△H1和△H2表示): .
②某温度时,向10mL0.4mol/L H2O2液中滴入1滴MnSO4发生分解:2H2O2=2H2O+O2 , 测得不同时刻生成O2的体积(已折算为标准状况下的体积)如表:
t/min | 0 | 2 | 4 | 6 |
V(O2)mL | 0 | 9.9 | 17.2 | 22.4 |
0~2min时反应速率比2~4min时的快,其原因是 , 0~6min的平均反应速率v(H2O2)=(忽略溶液体积的变化).
(4)锰基催化剂是合成甲醇、二甲醚的催化剂.已知:
反应 | 平衡常数KP | |
773K | 873K | |
Ⅰ.CO2(g)+4H2(g)CH4(g)+2H2(g) | 19.4 | 0.803 |
Ⅱ.CO2(g)+3H2(g)CH3OH(g)+H2O(g) | 6.07×10-9 | 3.65×10-9 |
①反应I的正反应是(填“放热”或“吸热”)反应.
②反应Ⅱ的平衡常数表达式为 . 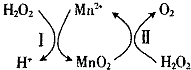
【答案】
(1)+3
(2)ZnS
(3)H2O2(1)+Mn2+(aq)=2H+(aq)+MnO2(s)△H=△H1﹣△H2;随着反应的进行,H2O2浓度不断减小,反应速率不断减慢;3.3×10﹣2mol/(L?min)
(4)放热;K= ![]()
【解析】解:(1)MnO(OH)中O元素的化合价为﹣2价,H元素的化合价为+1价,根据正负化合价的代数和为0,锰元素的化合价为+3价,所以答案是:+3;(2)因为Ksp(MnS)=1.4×10﹣15>Ksp(FeS)=6.0×10﹣18>Ksp(ZnS)=2.9×10﹣25 , 向废电池还原后的废液(含有Mn2+、Fe2+、Zn2+等)中逐滴滴加Na2S溶液,最先生成溶解度最小的物质,最先生成的沉淀为ZnS,所以答案是:ZnS;(3)①转化关系可知,过氧化氢和锰离子反应得到二氧化锰和氢离子,2H2O2(l)═2H2O(l)+O2(g)△H1①,MnO2(s)+H2O2(l)+2H+═Mn2+(aq)+O2(g)+2H2O(l)△H2 , ②依据盖斯定律①﹣②得到H2O2(l)+Mn2+(aq)═MnO2(s)+2H+(aq)△H=△H1﹣△H2所以答案是:H2O2(l)+Mn2+(aq)═MnO2(s)+2H+(aq)△H=△H1﹣△H2②0~2min产生的氧气的物质的量n(O2)= ![]() =0.00044mol,n(H202)=2n(O2)=0.00088mol,v(H2O2)=
=0.00044mol,n(H202)=2n(O2)=0.00088mol,v(H2O2)= ![]() ≈4.4×10﹣2mol/(Lmin),4~6min产生的氧气的物质的量n(O2)=
≈4.4×10﹣2mol/(Lmin),4~6min产生的氧气的物质的量n(O2)= ![]() =2.3×10﹣4mol,n(H202)=2n(O2)=4.6×10﹣4mol,v(H202)=
=2.3×10﹣4mol,n(H202)=2n(O2)=4.6×10﹣4mol,v(H202)= ![]() =2.3×10﹣2mol/Lmin,0~2min H2O2平均反应速率比4~6min快,原因为随着反应的进行,H2O2浓度不断减小,反应速率不断减慢;0~6min产生的氧气的物质的量n(O2)=
=2.3×10﹣2mol/Lmin,0~2min H2O2平均反应速率比4~6min快,原因为随着反应的进行,H2O2浓度不断减小,反应速率不断减慢;0~6min产生的氧气的物质的量n(O2)= ![]() =0.001mol,n(H202)=2n(O2)=0.002mol,v(H202)=
=0.001mol,n(H202)=2n(O2)=0.002mol,v(H202)= ![]() ≈3.3×10﹣2mol/(Lmin),所以答案是:②随着反应的进行,H2O2浓度不断减小,反应速率不断减慢;3.3×10﹣2mol/(Lmin);(4)①温度有773K升高到873K,平衡常数减小,表明升高温度,平衡向逆反应方向移动,说明正反应是放热反应,所以答案是:放热;②反应Ⅱ为CO2(g)+3H2(g)CH3OH(g)+H2O(g),其平衡常数表达式为K=
≈3.3×10﹣2mol/(Lmin),所以答案是:②随着反应的进行,H2O2浓度不断减小,反应速率不断减慢;3.3×10﹣2mol/(Lmin);(4)①温度有773K升高到873K,平衡常数减小,表明升高温度,平衡向逆反应方向移动,说明正反应是放热反应,所以答案是:放热;②反应Ⅱ为CO2(g)+3H2(g)CH3OH(g)+H2O(g),其平衡常数表达式为K= ![]() ,所以答案是:K=
,所以答案是:K= ![]() .
.
【考点精析】通过灵活运用化学平衡的计算,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%即可以解答此题.


科目:高中化学 来源: 题型:
【题目】关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是( )
A. ①②③④B. ②③C. ①②④D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2L的密闭容器中充入7.6mol NO和3.8mol O2 , 发生如下反应: ①2NO(g)+O2(g)2NO2(g)
②2NO2(g)N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )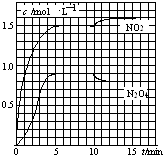
A.前5min反应的平均速率v(N2O4)=0.36mol(Lmin)﹣1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A~E都是由NH4+、H+、Na+、OH﹣、CH3COO﹣、Cl﹣中离子两两组成(离子可重复,如NaCl、HCl).常温下将各物质的溶液从1mL稀释到1000mL,pH的变化如甲图所示.请回答: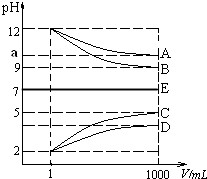
(1)已知常温下CH3COOH和NH3H2O 的电离常数相等都等于2×10﹣5 molL﹣1 , E可能为(填化学式).
(2)根据甲图显示的pH的变化关系,写出物质的化学式:C .
(3)25℃时,将amol B溶于水,向其中逐滴滴加D溶液至二者恰好完全反应,溶液显性,在滴加D溶液的过程中的水的电离平衡将(填”正向”“不”或“逆向”)移动;若向该溶液中又滴加b升 D溶液后溶液呈中性,所滴加D溶液的浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 树状分类法是唯一能表示物质分类的方法
B. 由一种元素组成的物质是单质
C. 在水溶液或熔融状态下能够导电的物质是电解质
D. 金刚石、石墨和C60三者互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成下面题目:
(1)硫酸是一种重要的含氧酸.实验室用浓硫酸与乙二酸(H2C2O4)晶体花热,可获得CO与CO2的混合气体,再将混合气体进一步通过(填一种试剂的名称)即可得纯净干燥的CO.
(2)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层.外层的优氯净 Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去;优氯净中氯元素的化合价为;无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另一固体.请写出无水亚硫酸钠受热分解的反应方程式;
(3)某无机盐M是一种优良的氧化剂,为确定其化学式,某小组设计并完成了如下实验: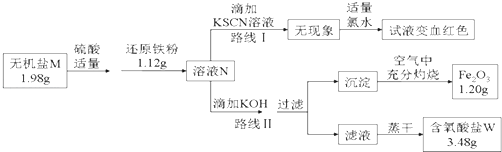
已知:
①无机盐M仅由钾离子和一种含氧酸根组成,其分子中的原子个数比为2:1:4;
②如图中,将1.98g该无机盐溶于水,滴加适量稀硫酸后,再加入1.12g还原铁粉,恰好完全反应得混合溶液N.
③该小组同学将溶液N分为二等份,分别按路线Ⅰ、路线Ⅱ进行实验.
④在路线Ⅱ中,首先向溶液N中滴加适量KOH至元素X刚好沉淀完全,过滤后将沉淀在空气中充分灼烧得纯净的Fe2O3粉末1.20g;再将滤液在一定条件下蒸干,只得到3.48g纯净的不含结晶水的正盐W.
请按要求回答下列问题:
①由路线Ⅰ的现象可知,溶液N中含有的阳离子是;
②由实验流程图可推得,含氧酸盐W的化学式是;由路线Ⅱ可知,1.98g无机盐M中所含钾元素的质量为g;
③无机盐M与1.12g还原铁粉恰好完全反应生成溶液N的化学反应方程为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
C. 25℃,101KPa,64gSO2中含有的原子数为3NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com