
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2 mol A和1 mo B,发生反应:2A(g)+B(g)![]() 2D(g) △H=Q kJ/mol,相关条件和数据见下表:下列说法正确的是( )
2D(g) △H=Q kJ/mol,相关条件和数据见下表:下列说法正确的是( )
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
A.Q<0,K3>K2>K1
B.实验I和Ⅱ探究的是催化剂对于化学反应的影响
C.实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,平衡向正向移动
D.A的转化率:Ⅲ![]() Ⅱ
Ⅱ![]()
【答案】B
【解析】
A.反应为2A(g)+B(g)![]() 2D(g),比较实验I和III,温度升高,平衡时D的量减少,化学平衡向逆反应方向移动,温度相同,平衡常数相同,据此分析;
2D(g),比较实验I和III,温度升高,平衡时D的量减少,化学平衡向逆反应方向移动,温度相同,平衡常数相同,据此分析;
B.实验II达到平衡的时间很短,与实验I温度相同,平衡时各组分的量也相同,据此判断;
C.温度不变,平衡常数不发生改变,根据浓度商与平衡常数K的关系判断化学反应的方向;
D.图表数据分析,实验I和Ⅱ探究的是催化剂对于化学反应的影响,A转化率不变,实验III中温度升高平衡逆向进行。
A.反应为2A(g)+B(g)![]() 2D(g),比较实验I和III,温度升高,平衡时D的量减少,说明化学平衡向逆反应方向移动,由于该反应的正反应为放热反应,Q<0,则K3<K1,温度相同,平衡常数相同,则K1=K2,综上,则平衡常数的关系为:K3<K2=K1,A错误;
2D(g),比较实验I和III,温度升高,平衡时D的量减少,说明化学平衡向逆反应方向移动,由于该反应的正反应为放热反应,Q<0,则K3<K1,温度相同,平衡常数相同,则K1=K2,综上,则平衡常数的关系为:K3<K2=K1,A错误;
B.实验II达到平衡的时间很短,与实验I温度相同,平衡时各组分的量也相同,可判断实验II使用了催化剂,催化剂加快反应速率,但不改变化学平衡状态,实验I和Ⅱ探究的是催化剂对于化学反应的影响,B正确;
C.实验III中,原平衡的化学平衡常数为K=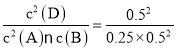 =4,温度不变,则平衡常数不变,实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,则此时容器中c(A)=1 mol/L,c(B)=0.25 mol/L,c(D)= 1mol/L,此时浓度商Q=
=4,温度不变,则平衡常数不变,实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,则此时容器中c(A)=1 mol/L,c(B)=0.25 mol/L,c(D)= 1mol/L,此时浓度商Q=![]() =4,则平衡不发生移动,C错误;
=4,则平衡不发生移动,C错误;
D.图表数据分析,实验I和Ⅱ探究的是催化剂对于化学反应的影响,A转化率不变,实验III中温度升高平衡逆向进行,A的转化率减小,A的转化率:Ⅲ<Ⅱ=I,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中正确的是( )
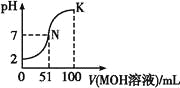
A.HA可能为一元弱酸
B.MOH为一元强碱
C.N点水的电离程度小于K点水的电离程度
D.若K点对应的溶液的pH=10,则有c(MOH)+c(M+)=0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验
实验一 | 实验二 | |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为![]() 的恒容密闭容器中充入
的恒容密闭容器中充入![]() 和
和![]() ,发生反应
,发生反应![]()
![]()
![]()
![]() ,测得
,测得![]() 随时间的变化如图曲线Ⅰ所示。下列说法正确的是
随时间的变化如图曲线Ⅰ所示。下列说法正确的是![]()
![]()
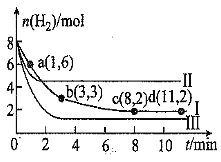
A.![]() 内,用
内,用![]() 表示的平均反应速率为
表示的平均反应速率为![]()
B.保持温度不变,若起始时向上述容器中充入![]() 和
和![]() ,则平衡时
,则平衡时![]() 的体积分数为
的体积分数为![]()
C.保持温度不变,若起始时向上述容器中充入![]() 、
、![]() 、
、![]() 和
和![]() ,则此时反应正向进行
,则此时反应正向进行
D.改变条件得到曲线Ⅱ、Ⅲ,则曲线Ⅱ、Ⅲ改变的条件分别是升高温度、充入氦气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料。
(1)标准状况下,22.4L Cl2的物质的量为________mol。
(2)实验室制取Cl2的化学方程式为 ________________________。
(3)收集Cl2应使用 _________ 法,要得到干燥的Cl2可选用 _______ 做干燥剂。
(4)写出实验室制取漂白液的反应的离子方程式 ______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验:①将0.1mol·L-1MgCl2溶液和0.5mol·L-1NaOH溶液等体积混合得到浊液;②取少量①中浊液,滴加0.1mol·L-1FeCl3溶液,出现红褐色沉淀;③将①中浊液过滤,取少量白色沉淀,滴加0.1mol·L-1FeCl3溶液,白色沉淀变为红褐色;④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解。下列说法中,不正确的是( )
A. 将①中所得浊液过滤,所得滤液中含少量Mg2+
B. 浊液中存在溶解平衡:Mg(OH)2(s)Mg2+(aq)+2OH-(aq)
C. 实验②和③均能说明Fe(OH)3比Mg(OH)2难溶
D. NH4Cl溶液中的NH4+可能是④中沉淀溶解的原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各种微粒浓度大小关系或结论正确的是( )
A.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性: ![]()
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(H+)=2c(OH-)+c(CH3COOH)
D.0.1 mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下0.1 mol/L的NaHB(强电解质)溶液中c(H+)>c(OH-),则下列关系一定正确的是( )
A. c(Na+)=c(HB-)+2c(B2-)+c(OH-)
B. c(Na+)=0.1 mol/L≥c(B2-)
C. HB-的水解方程式为HB-+H2O![]() B2-+H3O+
B2-+H3O+
D. 在该盐的溶液中,离子浓度大小顺序为c(Na+)>c(HB-)>c(B2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 为二元弱酸,
为二元弱酸,![]() ,
,![]() ,设
,设![]() 溶液中
溶液中![]() 。室温下用NaOH溶液滴定
。室温下用NaOH溶液滴定![]() 溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是( )
溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是( )
A.![]() 溶液:
溶液:![]()
B.![]() 的溶液:
的溶液:![]()
C.![]() 的溶液:
的溶液:![]()
D.![]() 的溶液:
的溶液:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com