
【题目】下列有关物质的性质与用途具有对应关系的是
A.明矾易溶于水,可用作净水剂
B.Al2O3熔点高,可用于制作耐火材料
C.HClO具有弱酸性,可用于漂白、消毒
D.Al(OH)3高温会分解,可用于治疗胃酸过多
科目:高中化学 来源: 题型:
【题目】某元素原子价电子构型3d54s2,其在周期表中的位置是( )
A. 第四周期ⅦA族 B. 第四周期ⅡB族
C. 第四周期ⅤB族 D. 第四周期ⅦB族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将溶液 的c(H+)、c(OH﹣)之比取为AG[AG=lg ![]() ].25℃时,用0.01mol.L﹣1的氢氧化钠溶液滴定20mL相同物质的量浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( )
].25℃时,用0.01mol.L﹣1的氢氧化钠溶液滴定20mL相同物质的量浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( ) 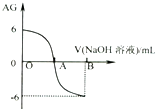
A.A点时c(CH3COO﹣)>c(Na+)
B.室温时0.01mol.L﹣1的醋酸溶液pH=6
C.OA段溶液中均有:c(CH3COO﹣)>c(CH3COOH)
D.若B点时加入NaOH溶液40mL,所得溶液中:c(CH3COO﹣)+2c(CH3COOH)=c(OH﹣)﹣c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯  (g)+CO2(g)
(g)+CO2(g) 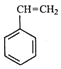 (g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行 A.
(g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行 A.  (g)
(g)  (g)+H2(g)△H1=﹣125KJ/mol
(g)+H2(g)△H1=﹣125KJ/mol
B.H2(g)+CO2(g)CO(g)+H2O(g)△H2=﹣41KJ/mol
(1)上述乙苯与CO2反应的反应热△H为
(2)苯乙烯与HCl加成的产物中具有手性异构体的分子的结构简式为 .
(3)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为1.0mol/L和3.0mol/L,其中实验I在T1℃,0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图I所示. 
①实验I乙苯在0﹣50min时的反应速率为
②实验Ⅱ可能改变条件的是
③图II是实验I中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体积分数V%随时间t的变化曲线.
(4)25℃时,将体积为Va PH=a的某一元强碱与体积为Vb PH=b的某二元强酸混合.若所得混合溶液的pH=11,且a=13,b=2,则Va:Vb= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语或模型正确的是
A. HF的电子式:![]() B. 用核素符号表示中子:
B. 用核素符号表示中子:![]()
C. HClO的结构式:H-Cl-O D. 用电子式表示CO2的形成过程: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5.X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物.请回答:
(1)X元素的名称是;Y元素的名称是;Z元素的名称是 .
(2)XZ3化合物的电子式是 .
(3)分别写出X、Y的含氧酸的分子式、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H 是一种免疫调节剂,其合成流程如下:

问答下列问题:
(1)H所含官能团有氨基、羟基和______________。
(2)X的化学式为_______________,③的反应类型是_____________。
(3)设计反应①和⑤的目的是__________________。
(4)反应①为取代反应,其化学方程式为________________。
(5)R的同分异构体M同时满足下列条件:
①M 能与氯化铁溶液发生显色反应
②1molM 最多能和4molNaOH 发生反应
③在核磁共振氢谱上有四组峰且峰的面积之为3:3:2:2
M 的结构简式可能为________________。
(6)已知: ,结合上述相关信息,以
,结合上述相关信息,以 为原料设计合成路线合成
为原料设计合成路线合成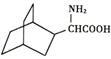 _________(其他试剂自选)。
_________(其他试剂自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L的密闭容器中发生反应xA(g)+yB(g) ![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。
A.200 ℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B.200℃时,该反应的平衡常数为25 L2/mol2
C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D.由图乙可知,反应xA(g)+yB(g) ![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com