
室温下,在下列实验过程中,有关溶液的温度、浓度和质量始终不变的是( )
A.向浓氨水中持续通入干燥洁净的空气(不含CO2)
B.向KNO3饱和溶液中加ng KNO3晶体
C.向98.3%浓硫酸中加入ng SO3
D.向硫酸铜饱和溶液中加入ng无水硫酸铜粉末
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:阅读理解
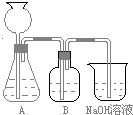
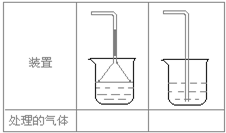
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
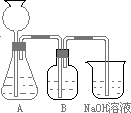
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 4.8c(v2-v1) |
| m |
| 4.8c(v2-v1) |
| m |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
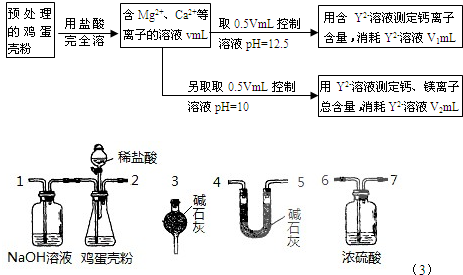
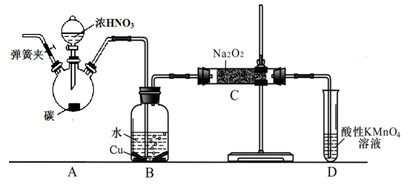
.鸡蛋壳中含有大量钙、少量镁和钾等元素。实验室可用图示流程测定鸡蛋壳中钙、镁元素含量。依据的反应可以表示为:Ca2++Y2-=CaY、Mg2++Y2-=MgY。回答下列问题。
⑴测定Ca2+、Mg2+总含量时,控制溶液pH=10。若pH过大,测定结果将 (填“偏大”、“偏小”或“无影响”);
⑵测定Ca2+含量的关键是控制溶液的pH,使溶液中Mg2+形成沉淀,若要使溶液中c(Mg2+)不大于1.2×10-7mol/L,则溶液pH应不小于 (已知:Ksp[Mg(OH)2]=1.2×10-11,上述实验均在室温下进行)。
⑶如果鸡蛋壳粉质量为m g,溶液中Y2-浓度为cmol/L,则鸡蛋壳样品中镁元素质量分数是 。
⑷有同学提出可采用如下装置、通过测定鸡蛋壳与盐酸反应产生的二氧化碳的量就能测定鸡蛋壳中的钙的总含量。
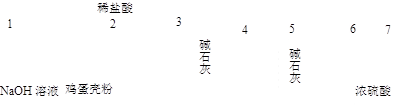
①采用该方法进行实验,各装置从左到右的连接顺序依次:
1—2—________________ __(填各装置对应接口的数字序号)。
②若排除实验仪器和操作的影响因素,此实验方法测得的结果是否准确?
![]() 答:________(填“准确”、“不一定准确”或“无法判断”)。
答:________(填“准确”、“不一定准确”或“无法判断”)。
原因是___________________ __
![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com