
某有机物的结构为下图所示,这种有机物不可能具有的性质是( )
①可以燃烧; ②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应; ⑥能发生水解反应
A.①④ B.只有⑥ C.只有⑤ D.④⑥
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
碳、硫的含量影响钢铁性能.碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定.
(1)采用图1装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2.
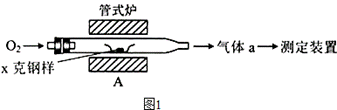
①气体a的成分是
②若钢样中硫以FeS形式存在,A中反应::

3FeS+5O2 1_________+3___________。
(2)将气体a通入测硫酸装置中(如图2),采用滴定法测定硫的含量.
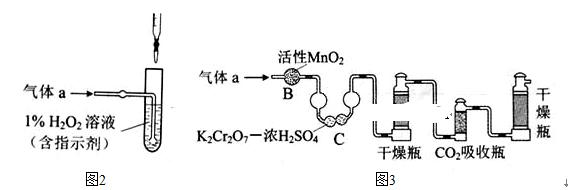
①H2O2氧化SO2的化学方程式:
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液.若消耗1mL NaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:
(3)将气体a通入测碳装置中(如图3),采用重量法测定碳的含量.
①气体a通过B和C的目的是
②计算钢样中碳的质量分数,应测量的数据是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知R2-的核内有x个中子,R的质量数为M,则m克R2-含有的电子的物质的量为( )
A.(M-x+2 )mol B.m(M+x-2
)mol B.m(M+x-2 )/M mol
)/M mol
C.m(M-x-2 )/M mol D. m(M-x+2
)/M mol D. m(M-x+2 )/M mol
)/M mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应现象中,叙述正确的是( )
A.灼热的铁丝在氯气中燃烧,集气瓶内产生棕黄色烟雾
B.氢气在氯气中燃烧,集气瓶口有白雾
C.钠在氯气中燃烧,集气瓶内产生大量的白色烟雾
D.灼热的铜丝在氯气中燃烧,集气瓶内产生棕红色烟
查看答案和解析>>
科目:高中化学 来源: 题型:
现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL0.2 mol/L的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平 。请回答下列问题:
(1) 上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2) 将计算、取得的浓H2SO4加适量蒸馏水稀释,冷却片刻,随后全部转移到 mL的容量瓶中,转移时应用玻璃棒 。转移完毕,用少量蒸馏水 ,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度 处。改用 加蒸馏水到瓶颈刻度的地方,振荡、摇匀后,装瓶、贴签。
(3) 在配制过程中,其他操作都准确,下列操作中,能引起误差偏高的有 (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示方法正确的是
A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由“C(石墨)=C(金刚石)ΔH = +1.9kJ/mol”可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH = - 57.3kJ/mol,若将含
1molCH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3kJ
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧
的热化学方程式表示为2H2(g)+O2(g)=2H2O(l)ΔH = —285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
反应N2O4(g) 2NO2(g)ΔH =+57 kJ·mol-1,在温度为T1、T2时,
2NO2(g)ΔH =+57 kJ·mol-1,在温度为T1、T2时,
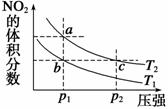 平衡体系中NO2的体积分数随压强(缩小体积)的
平衡体系中NO2的体积分数随压强(缩小体积)的
变化曲线如图所示。下列说法正确的是 ( )
A.a、c两点的反应速率:a>c
B.a、c两点气体的颜色:a深,c浅
C.由状态b到状态a,可以用加热的方法
D.a、c两点气体的平均相对分子质量:a>c
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对实验现象的描述中错误的是
A.向FeCl3和KSCN混合溶液中加入少量KCl固体,溶液血红色变浅
B.向5mL0.1mol/LK2Cr2O7溶液中加入少量NaOH固体,溶液由橙色变为黄色
C.等体积等浓度Na2S2O3和H2SO4混合,温度升高出现浑浊和生成气体速度加快
D.酸性KMnO4溶液中滴加H2C2O4,H2C2O4浓度越大褪色和生成气体速度越快
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A、标准状况下,33.6 L SO3中含有的氧原子数是4.5NA
B、1 mol OH-和1 mol—OH(羟基)中含有的电子数均为9NA
C、在加热条件下,100 mL18.4 mol/L的浓硫酸与足量金属铜反应得到的SO2的分子数为0.92 NA
D、当0.2 mol Na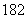 O2与足量CO2完全反应后,生成碳酸钠的质量为21.6 g
O2与足量CO2完全反应后,生成碳酸钠的质量为21.6 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com