
����Ŀ����֪��Ӧ![]() ��Ϊ�о�Ӱ��÷�Ӧ���ʵ����أ��ڲ�ͬ�����½���4��ʵ�飬Y��Z����ʼŨ��Ϊ0����Ӧ��X��Ũ���淴Ӧʱ��ı仯�����ͼ��ʾ������˵������ȷ����( )
��Ϊ�о�Ӱ��÷�Ӧ���ʵ����أ��ڲ�ͬ�����½���4��ʵ�飬Y��Z����ʼŨ��Ϊ0����Ӧ��X��Ũ���淴Ӧʱ��ı仯�����ͼ��ʾ������˵������ȷ����( )

A.��ʵ��ڡ���ֻ�ı�һ������������ʵ��ڡ��ܵó����ۣ������¶ȣ���ѧ��Ӧ���ʼӿ�
B.��ʵ��١���ֻ�ı�һ������������ʵ��١��ڵó����ۣ�����Ӧ��Ũ�ȣ���ѧ��Ӧ���ʼӿ�
C.��ʵ��ڡ���ֻ�ı�һ����������ʵ���ʹ���˴���
D.0��10min�ڣ�ʵ��۵�ƽ������v(Y)=0.04 mol/(L��min)
���𰸡�D
��������
A����ʵ��ڡ���ֻ�ı�һ��������ʵ��ڡ�������ʵ�飬X����ʼŨ����ͬ���¶��ɵڢ���ʵ���800�����ߵ�820�棬��Ӧ�������Լӿ죬˵���¶����ߣ���ѧ��Ӧ���ʼӿ죬Aѡ����ȷ��
B����ͼ���п��Կ�����ʵ��١�������ʵ�飬�¶���ͬ�����ŷ�ӦΪX��Ũ������ѧ��Ӧ���ʼӿ죬Bѡ����ȷ��
C��ʵ��ڡ�������ʵ�飬X����ʼŨ����ȣ��¶���ͬ��ƽ��״̬Ҳ��ͬ����ʵ��۴ﵽƽ���ʱ��̣���Ӧ���ʿ죬˵��ʵ���ʹ���˴�����Cѡ����ȷ��
D����0��10min�ڣ�ʵ��۵�ƽ������v(X)=��1.0mol/L��0.6mol/L����10min��0.04mol/(L��min)����Ϊ��ѧ��Ӧ����֮�ȵ��뻯ѧ������֮�ȣ�����v(Y)=0.02mol/(L��min)����D�����
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ɷֱ�ͨ������������Ӧ��ȡ����: �� ��
a.CH3CH2OH(g)+H2O(g) ![]() 4H2(g)+2CO(g)����H=+256.6 kJ��mol-1
4H2(g)+2CO(g)����H=+256.6 kJ��mol-1
b.2CH3CH2OH(g)+O2(g) ![]() 6H2(g)+4CO(g)����H=+27.6 kJ��mol-1
6H2(g)+4CO(g)����H=+27.6 kJ��mol-1
������˵����ȷ���ǣ� ��
A.�Ҵ���ȼ������H=-13.8 kJ��mol-1
B.���߷�Ӧa�ķ�Ӧ�¶ȣ��Ҵ���ת���ʼ�С
C.2H2(g)+O2(g)=2H2O(g)����H=-229 kJ��mol-1
D.��ȡ��������������Ӧb���յ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼú�����������к��н϶��CO2��CO��SO2��Ӱ�컷�������塣����ۺ�������Щ����һֱ�ǿ��е�λ�о����ȵ㡣
(1)��֪��
��Ӧ | �Ȼ�ѧ����ʽ | ƽ�ⳣ�� |
�� | 2CO2(g)��6H2(g) | K1 |
�� | CO(g)��H2O(g) | K2 |
�� | 2CO(g)��4H2(g) | K3 |
����H1��___________(����H2����H3��ʾ)��K3��____________(��K1��K2��ʾ)��
(2)��Է�Ӧ���о����֣��÷�Ӧ��CO2��ƽ��ת�����淴Ӧ�¶ȡ�Ͷ�ϱ�[n(H2)/n(CO2)]�ı仯������ͼ��
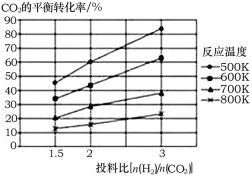
����H1______(���>������<��)0��
���������������䣬��������ѹǿ�� ���淴Ӧ����____________(����������������С����������������ͬ)��ƽ�ⳣ��K____________��
(3)�о����֣��������Դ�ʹ����CO��SO2ת��ΪCO2��S����Ӧԭ��Ϊ��2CO(g)��SO2(g) ![]() 2CO2(g)��S(l)����H��-270 kJ��mol-1
2CO2(g)��S(l)����H��-270 kJ��mol-1
������������ͬ���о����֣��ֱ�ѡȡFe2O3��NiO��Cr2O3��������Ӧ�Ĵ���ʱ��SO2��ת�����淴Ӧ�¶ȵı仯��ͼ���о��ó���Ӧ��ѡ��Fe2O3����������Ҫԭ�������______________��

������2 L�����ܱ������У���3 mol CO��1 molSO2��ϣ���һ��������������Ӧ����SO2��ƽ��ת����Ϊ40%ʱ����ʱK��________��
����Ӧ�������ٷֱ�ͨ���������壬����ʹSO2ת�����������____(�����)��
A��CO������B��SO2������C��N2������D��H2S������E��CO2
(4)һ���¶��£���ij���������ܱ�������ͨ��һ������CO(g)��H2O(g)������ӦCO(g)��H2O(g) ![]() CO2(g)��H2(g)������ͼ��ֱ�����ʱ䣨��H�����������ƽ����Է���������
CO2(g)��H2(g)������ͼ��ֱ�����ʱ䣨��H�����������ƽ����Է���������![]() ���������ܶȣ�������CO2���������(CO2)�뷴Ӧʱ��Ĺ�ϵ��������ȷ���ܱ����ÿ��淴Ӧ�ﵽƽ��״̬����________(�����)��
���������ܶȣ�������CO2���������(CO2)�뷴Ӧʱ��Ĺ�ϵ��������ȷ���ܱ����ÿ��淴Ӧ�ﵽƽ��״̬����________(�����)��
A. 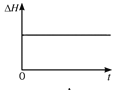 B.
B. 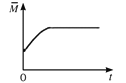 C.
C. 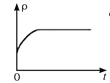 D.
D. 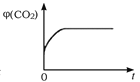
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��DΪԭ�������������������Ԫ�أ�A������������������Ӳ���2����B�������Ӻ�C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ����Ԫ�صĵ��ʷ�Ӧ������һ�ֵ���ɫ�Ĺ���E��D��L������������������Ӳ��ϵĵ�����֮�͡�
(1)AԪ������Ϊ______��D�����ڱ��е�λ��________�����Ӱ뾶��СB___C(����>����<������=��)��
(2)B�����ֵ����ڳ����¶������壬���ǻ�Ϊ____________���Ƚ�B���⻯���D���⻯��е㣺B___D��������������������=������ԭ����_________________��
(3)E�к��л�ѧ�����ͣ�_________������___________������������ӻ��������������ۻ�����������
(4)�õ���ʽ��ʾC��D�Ķ�Ԫ��������γɹ��̣�_____________________��
(5)��ԭ����B�ֱ��γ�10���Ӻ�18���ӷ��ӣ�д��18���ӷ���ת����10���ӷ��ӵĻ�ѧ����ʽ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(AlN)��һ�ֻҰ�ɫ���壬����ˮ������Ӧ������NH3��Al��800�����Ϸ�Ӧ���Ʊ�AlN��ʵ��װ�����£�

�ش��������⣺
(1)װ�â���ʢ�ŵ�ҩƷΪ__________��װ�âܵ����������հ�����__________��
(2)ʵ��ʱ�ȵ�ȼ�ٴ��ƾ��ƣ���Ŀ����______________________________________��
(3)Ϊʹʵ�鰲ȫ��װ�âܵ�β������������_____________________��
(4)װ�â��з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��װ�â��з�����Ӧ�Ļ�ѧ����ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����ڹ�ҵ��������������;��ij�����Ի�ͭ��(��Ҫ�ɷ�Ϊ Cu2S�������� Fe2O3��SiO2 ������)Ϊԭ���Ʊ�������ˮ�ļ�ʽ̼��ͭ���������£�
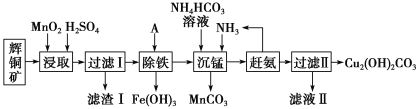
��֪��
�ٳ����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±�
�������� | Fe2�� | Fe3�� | Cu2�� | Mn2�� |
��ʼ���� | 7.5 | 2.7 | 5.6 | 8.3 |
��ȫ���� | 9.0 | 3.7 | 6.7 | 9.8 |
�� Ksp[Fe(OH)3]��4.0��10��38
(1)�ӿ�����ȡ�����ʣ����ʵ���������Ũ���⣬���ɲ�ȡ�Ĵ�ʩ��__________����дһ�֣���
(2)����I�е���Ҫ�ɷ���MnO2��S��SiO2����д������ȡ����Ӧ������S�Ļ�ѧ����ʽ��______________��
(3)��������������ʱ������Լ�A����CuO�ȣ�����pH���ķ�ΧΪ_________������ A ����Һ�� pH��Ϊ4.0������Һ�� Fe3����Ũ��Ϊ_________mol/L��
(4)д����������(�� Mn2��)�����з�Ӧ�����ӷ���ʽ��_________________________��
(5)���ϰ���ʱ�������˵IJ���������________________��
(6)���ˢ�õ��ij�������ϴ�ӡ�������Եõ���ʽ̼��ͭ���жϳ����Ƿ�ϴ���IJ�����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)������ͼװ�ã�����NH3�����������MxOy��Ӧ����M��N2��H2O��ͨ����������ˮ���������ⶨM�����ԭ��������a���Լ���Ũ��ˮ��

������a������Ϊ_________������b��װ����Լ�������___________��
�ڰ�����������ȷ��װ������˳��Ϊ_________(����ĸ��װ�ÿ��ظ�ʹ��)��
(2)����������һ�ֹ�ҵ�Σ���������������Ӧ�ù㷺��������ͼ��ʾװ��(�г�װ����ʡ��)��ҩƷ��̽���������������ᷴӦ���������ɷ֡�
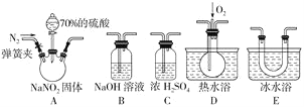
��֪����.NO+NO2+2OH-=2NO2-+H2O
��.����Һ�����¶ȣ�NO2(21��)��NO(-152��)
�ٷ�ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪����Ŀ����________________��
��Ϊ�˼���װ��A�����ɵ�����������������˳��(������������)��A��_________����װ���������������еIJ�����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ����(����)
A.̼�������Һ����������������Һ��![]()
B.������þ�����ᷴӦ��![]()
C.��ˮ�����ᷴӦ��![]()
D.̼�������ϡ�����У�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100 mL NaOH��Һ��ͨ��һ������CO2���壬��ַ�Ӧ������������Һ����μ���0.2 mol��L��1�����ᣬ����CO2������������������֮���ϵ��ͼ��ʾ�������ж���ȷ����(����)
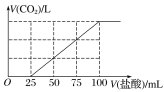
A. ԭNaOH��Һ��Ũ��Ϊ0.2 mol��L��1
B. ͨ��CO2�ڱ�״���µ����Ϊ448 mL
C. ������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaOH)��n(Na2CO3)��1��3
D. ������Һ�����ʳɷֵ����ʵ���֮��Ϊn(NaHCO3)��n(Na2CO3)��1��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com