
【题目】同温同压下,同体积的氨气(![]() )和硫化氢气体(
)和硫化氢气体(![]() )的质量比为_________;同质量的氨和硫化氢气体的体积比为___________;若二者氢原子数相等,则它们的体积比为___________。(均为前者比后者)
)的质量比为_________;同质量的氨和硫化氢气体的体积比为___________;若二者氢原子数相等,则它们的体积比为___________。(均为前者比后者)
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述,正确的是
A. 新制氯水中只含Cl2和H2O分子
B. 新制氯水可使蓝色石蕊试纸先变红后褪色
C. 光照氯水有气泡逸出,该气体是Cl2
D. 氯水放置数天后酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,1-二环丙基乙烯(![]() )是重要医药中间体,下列关于该化合物的说法错误的是
)是重要医药中间体,下列关于该化合物的说法错误的是
A. 所有碳原子可能在同一平面B. 能使酸性高锰酸钾溶液褪色
C. 二氯代物有9种D. 生成1mol C8H18至少需要3mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POC13是重要的化工原料,某兴趣小组准备用三氯化磷、氯气、二氧化硫制备POC13,产物中还有一种遇水强烈水解的物质SOC12。

已知:PC13熔点-93.6℃、沸点76.1℃,遇水强烈水解,易与氧气反应;POC13遇水强烈水解,能溶于PC13.
(1)仪器甲的名称是________________。
(2)已知装置B制备POC13,以上仪器接口连接的顺序为a____d,装置B中发生反应的化学方程式为_________________________。
(3)B中反应温度控制在60~65℃,其原因是__________________________。
(4)用佛尔哈德法测定POC13含量:准确称取20.20g POC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;加入10.00mL 3.200mol·L-1AgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;加入指示剂,用0.2000mol·L-1KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mL KSCN溶液。
(已知:KSP(AgC1)=3.2×10-10,KSP(AgSCN)=2×10-12)
①POC13水解的化学反应方程式为______________________________。
②滴定选用的指示剂是__________(选填字母),滴定终点的现象为__________。
a.FeC12 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
③用硝基苯覆盖沉淀的目的是___________________________________。
④产品中POC13的百分含量为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCO3可用作选矿剂、催化剂及伪装涂料的颜料。以含钴废渣(主要成份CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3和ZnSO4溶液的一种工艺流程如下:
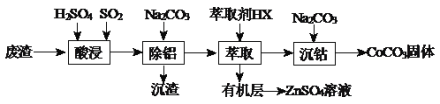
下表是相关金属离子生成氢氧化物沉淀的pH(按金属离子浓度为1.0mol·L-1计算):
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
(1)写出“酸浸”时发生氧化还原反应的化学方程式________________________。
(2)“除铝”过程中需要调节溶液pH的范围为_________,形成沉渣时发生反应的离子方程式为______________________。
(3)在实验室里,萃取操作用到的玻璃仪器主要有_________________;上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层)![]() ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______________。
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______________。
(4)“沉钴”时,Na2CO3溶液滴加过快会导致产品不纯,请解释原因___________________。
(5)在空气中煅烧CoCO3生成某种钴氧化物和CO2,若充分煅烧一定量CoCO3后测定所得固体质量为2.41g,CO2的体积为0.672L(标准状况),假设固体为纯净物,其化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是( )
A. CaCO3的电离方程式:CaCO3 ![]() Ca2++CO32-
Ca2++CO32-
B. H2SO3的电离方程式H2SO3![]() 2H++SO32-
2H++SO32-
C. CO32-的水解方程式:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. HCO3-在水溶液中的电离方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。

图中①为氯气发生装置,②的试管中盛有![]() 的
的![]() 溶液,并置于热水浴中,③的试管中盛有
溶液,并置于热水浴中,③的试管中盛有![]() 的
的![]() 溶液,并置于冰水浴中,④的试管中加有紫色石蕊试液,⑤为尾气吸收装置。
溶液,并置于冰水浴中,④的试管中加有紫色石蕊试液,⑤为尾气吸收装置。
(1)制取氯气时,在烧瓶中先加入一定量的二氧化锰固体,再通过_________(填写仪器名称)向烧瓶中加入适量的____________(填写试剂名称)。
(2)为除去氯气中混有的氯化氢气体,可在①和②之间安装盛有__________(选填字母编号)的净化装置。
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液
(3)本实验制取次氯酸钠的离子方程式是____________________。
(4)比较制取氯酸钾和次氯酸钠的条件,可以初步得到的结论是__。
(5)反应完毕经冷却后,②的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是___________(选填字母);从②的试管中分离该晶体的操作是___________(填写实验操作名称)。

(6)实验中可观察到④的试管中溶液颜色会发生变化:最初溶液由紫色变为_________,随后溶液逐渐变为无色,是因为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A2![]() 可将B2-氧化为B单质,
可将B2-氧化为B单质,![]() 则被还原为A3+,又知100 mL的0.3 mol·L-1的
则被还原为A3+,又知100 mL的0.3 mol·L-1的![]() 与150 mL的0.6 mol·L-1B2-恰好完全反应,则
与150 mL的0.6 mol·L-1B2-恰好完全反应,则![]() 中的n值为( )
中的n值为( )
A.4B.5C.6D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入0.1 mol·L-1的一元
酸HA,溶液pH的变化曲线如图所示。下列说法正确的是

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com