
【题目】高聚物M广泛用于各种刹车片。实验室以烃A为原料制备M的一种合成路线如下:

已知:

回答下列问题:
(1)A的结构简式为____。H的化学名称为_____。
(2)B的分子式为____。C中官能团的名称为____。
(3)由D生成E、由F生成G的反应类型分别为____、_____。
(4)由G和I生成M的化学方程式为____。
(5)Q为I的同分异构体,同时满足下列条件的Q的结构简式为____。
①1 moi Q最多消耗4 mol NaOH ②核磁共振氢谱有4组吸收峰
(6)参照上述合成路线和信息,以甲苯为原料(无机试剂任选),设计制备![]() 的合成路线_____________________。
的合成路线_____________________。
【答案】![]() 对二甲苯(或1,4-二甲苯) C6H5Cl 醚键 取代反应 取代反应
对二甲苯(或1,4-二甲苯) C6H5Cl 醚键 取代反应 取代反应  +(2n-1)H2O
+(2n-1)H2O 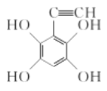 、
、

![]()
【解析】
结合给定的已知信息①,采用逆合成分析法可推出A为苯,与一氯甲烷和氯化铝反应生成H,则为对二甲苯,最终被高锰酸钾氧化为对二苯甲酸;因此B为氯苯,再结合给定信息②推知C为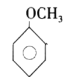 ,根据合成路线可知E为
,根据合成路线可知E为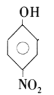 ,结合高聚物的结构简式可知,G为
,结合高聚物的结构简式可知,G为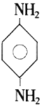 ,据此分析作答。
,据此分析作答。
(1)根据上述分析可知,A为苯,其结构简式为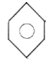 ,H的化学名称为对二甲苯(或1,4-二甲苯),
,H的化学名称为对二甲苯(或1,4-二甲苯),
故答案为: ;对二甲苯(或1,4-二甲苯);
;对二甲苯(或1,4-二甲苯);
(2)B为氯苯,其分子式为C6H5Cl,C为 ,其分子内所含官能团为醚键,
,其分子内所含官能团为醚键,
故答案为:C6H5Cl;醚键;
(3)由D生成E的过程为苯酚中苯环的硝化反应,即取代反应;由F生成G为羟基被氨基取代的过程,反应类型也为取代反应,
故答案为:取代反应;取代反应;
(4)由G和I生成M发生的是缩聚反应,其方程式为:
 +(2n-1)H2O,
+(2n-1)H2O,
故答案为:
 +(2n-1)H2O;
+(2n-1)H2O;
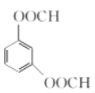
(5)I的分子式为C8H6O4,1 moi Q最多消耗4 mol NaOH,则分子内含4个酚羟基或4个甲酸酯结构;核磁共振氢谱有4组吸收峰,则分子内有4种不同化学环境的氢原子,据此可确定取代基的位置,其结构简式可能为: 或
或 ,
,
故答案为:  、
、 ;
;
(6)根据上述合成路线和已知信息,以甲苯为原料,先与氯气在氯化铁作用下发生取代反应生成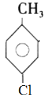 ,再根据已知信息①在氯化铝的条件下与甲苯合成的合成
,再根据已知信息①在氯化铝的条件下与甲苯合成的合成 ,最终被酸性高锰酸钾氧化为
,最终被酸性高锰酸钾氧化为![]() 。具体合成路线如下:
。具体合成路线如下:

![]() ,
,

![]() 。
。


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,用蒸馏水稀释1mol·L-1的醋酸溶液至0.01mol·L-1,随着溶液的稀释,下列各项中始终保持增大趋势的是( )
A. B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向物质X中逐渐加入(或通入)Y溶液,生成沉淀的量与加入Y的物质的量关系如图所示,下表中符合图示情况的是

A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,铝元素能损害人的脑细胞。适当地补充碘元素可预防甲状腺肿大,但摄入过多也会导致甲状腺肿大,因此补充人体所需的元素时也要适可而止。试回答下列问题:
(1)Fe也是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:________。
(2)与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系是________。
(3)氯化铝的熔点是194℃,氧化铝的熔点是2054℃,但是工业上不能用电解熔融氯化铝的方法获取铝单质,这是因为________________________________________。
(4)F与I是同一主族的元素,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别为________、________,BeF2分子的立体构型是________,H2O分子的立体构型是________。
(5)I2晶体的晶胞结构如图所示,该晶胞中含有________个I2分子,设该晶胞的晶胞参数为acm,则I2的密度是________________g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牛通过吃草从草中获得化合物和元素。那么,牛和草体内的各种化学元素( )
A.种类差异很大,含量大体相同B.种类和含量差异都很大
C.种类和含量都是大体相同的D.种类大体相同,含量差异很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组查阅资料可知高温下,FeCl2与O2反应一定生成Fe2O3,可能生成FeC13或Cl2。该小组同学利用如下装置对该反应进行探究。回答下列问题:
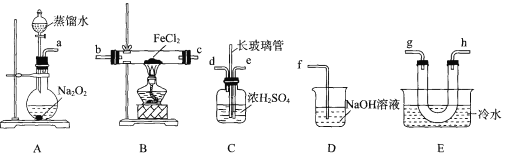
查阅资料:FeCl2固体呈绿色,熔点为674℃,沸点为1023℃;FeC13在100℃左右升华。
(l)装置A中盛放蒸馏水的仪器名称为____。
(2)按气流从左到右的顺序,上述装置合理的连接顺序为____(填仪器接口的小写字母)。
(3)装置C中浓硫酸的作用为 ___,长玻璃管的作用为 ___ 。
(4)实验结束后,用D中所得溶液设计实验证明此反应无Cl2生成 ___。
(5)实验过程中,B处硬质玻璃管中的现象为 ___;装置E中冷水的作用为 ____。
(6)由上述实验可知:高温下,FeCl2与O2反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL 18mol/L的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量
A. 小于0.45mo1B. 等于0.45molC. 在0.45mol和0.9mol之间D. 大于0.9mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图回答问题:

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:__________________
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是_________________作用是________________________.
B中加入的试剂是_________________作用是________________________.
C中加入的试剂是 _________________ ,作用是除尽 ____________气体.
D中加入的试剂是_________________作用是________________________.
(3)实验时,C中应观察到的现象是_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要0.5mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______________。
(3)在配制过程中,其他操作都准确,下列操作中错误的是________(填代号,下同),能引起误差偏高的有________。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
⑦定容时,俯视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com