
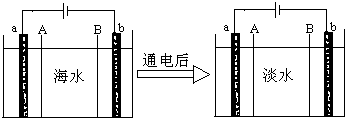
 电渗析法将海水进行淡化,其原理如图.已知海水中含Na+、Cl-、Ca2+、Ba2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )
电渗析法将海水进行淡化,其原理如图.已知海水中含Na+、Cl-、Ca2+、Ba2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )| A、通电后,海水中阳离子往a电极处运动 |
| B、B膜是阴离子交换膜 |
| C、通电后,电子由b极经过溶液到达a极 |
| D、通电后,b电极上产生无色气体,溶液中少量白色沉淀 |


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
| A、用碱式滴定管向锥形瓶内注入10mL氢氧化钠溶液,若开始时滴定管尖嘴有气泡,则测定结果偏高 |
| B、边滴边振荡,直到溶液由橙色变成黄色且半分钟内不褪色为止 |
| C、接近滴定终点时,往锥形瓶加入少量蒸馏水,则测定结果偏高 |
| D、用酸式滴定管时,起始读数俯视,结束读数仰视,则测定结果偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制标准溶液时,固NaOH体中混有NaCl 杂质 |
| B、滴定终点读数时,俯视滴定管的刻度 |
| C、盛放未知液的锥形瓶用蒸馏水洗过,未用未知液体润洗 |
| D、配制NaOH标准溶液时,定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.25×10-13mol?L-1 |
| B、0.02mol?L-1 |
| C、1×10-7mol?L-1 |
| D、1×10-12mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、平衡常数的表达式K=
| ||
| B、当v正(NH3):v正(NO)=1:1时,说明该反应已经达到平衡 | ||
| C、若平衡时两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=5:4 | ||
| D、反应达到平衡后,恒容条件下,同倍数改变NH3和NO的量,c(O2)=可能不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com