
【题目】用脱脂棉包住约0.2 g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加少量水,结果脱脂棉剧烈燃烧。
(1)由脱脂棉剧烈燃烧可得出过氧化钠与水反应的结论是:
a._______________________________________
b.______________________________________
(2)写出过氧化钠与水反应的离子方程式:________________________________________
(3)某研究性学习小组,拟用如图所示的装置进行实验,以证明上述2个结论。实验的操作方法及现象是:____________________

【答案】 有氧气生成 有大量的热放出 2Na2O2+2H2O=4Na++4OH-+O2↑ ①打开分液漏斗上口塞,打开旋塞K,使水由漏斗流下;②将带火星木条放在导管口A处,木条复燃;③导管口B处有气泡冒出。
【解析】(1)脱脂棉剧烈燃烧,说明该反应是放热反应,且反应中有助燃性气体生成,则实验结论为过氧化钠与水反应放出热量并氧气生成,故答案为:有氧气生成;有大量的热放出;
(2)过氧化钠与水反应生成氢氧化钠和氧气,反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(3)氧气具有使带火星的木条复燃的性质,所以可用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成;气体具有热胀冷缩的性质,如果该反应放热,放出的热量能使集气瓶内空气的压强增大;如果q导管插入盛水的小烧杯中,有气泡冒出,证明此反应放热,故答案为:打开分液漏斗上口塞,打开旋塞K,使水由漏斗流下,将带火星木条放在导管口A处,木条复燃,导管口B处有气泡冒出。


科目:高中化学 来源: 题型:
【题目】已知1molH—H、Br—Br和H—Br键断裂时需要吸收的能量分别是436kJ、200kJ和369kJ,氢气与溴蒸汽化合生成1mol溴化氢时放出的能量akJ,则a为
A. -102 B. -51 C. 102 D. 51
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下:

已知:![]()
请回答下列问题:
(1)F的名称是 _______________,⑤的反应类型是________。 .
(2)E中的含氧官能团是________ (写名称),W的结构简式为 _________________。
(3)反应③的化学方程式是________。
(4) D发生聚合反应的化学方程式为________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为________________。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(其他试剂任选)。
![]()
__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的叙述,正确的是
A. 离子化合物中一定含有离子键 B. 单质分子中一定不存在化学键
C. 含有非极性键的分子一定是单质分子 D. 含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示。钛铁矿主要成分为钛酸亚铁(FeTiO3),其中一部分Fe2+在风化过程中会转化为+3价。

已知:TiO(OH)2(即H2TiO3)为两性氢氧化物
(1)步骤②中,发生反应的主要离子方程式为______________________。
(2)步骤③中,实现混合物的分离是利用物质的____________(填字母序号)。
A.熔沸点差异 B.溶解性差异 C.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是____________(填操作名称)。
(4)请结合化学用语用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理:________________________________。
(5)上述工艺流程中可以循环利用的物质是____________。
(6)在酸性环境中,利用电化学原理可生成的羟基自由基(·OH) 其反应为Fe2++H2O2=Fe3++OH-+·OH-,成的羟基自由基对有机物有极强的氧化能力,可用于水体里有机污染物降解的高级氧化技术。电解原理如图:

①写出阳极所发生反应的电极反应式__________________________。
②电解过程中,假设电极上每1molFe3+转变为Fe2+ 的同时也 消耗1molO2,则 每消耗1molO2电解液中可以产生______mol ·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是
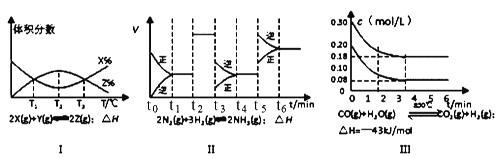
A. 由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
B. 由图Ⅱ知,反应在t6时,NH3体积分数最大
C. 由图Ⅱ知,t3时采取的措施是降低反应体系温度
D. Ⅲ在10L容器、850℃时反应,由图知,到4min时,反应放出51.6kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
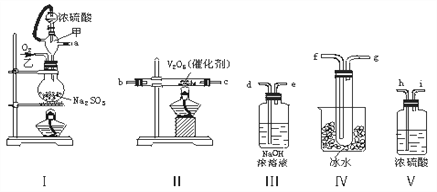
(1)装置的连接顺序(按气体左右的方向)是________________________________________________________(填各接口的编号)。
(2)实验时甲仪器的作用与原理是__________________________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序___________________________________________________。
(4)Ⅳ处观察到的现象是____________________________________________。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会________(填“增大”“不变”或“减小”)。
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为_______________________。(用n、m表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢吡格雷是一种血小板聚集抑制剂,该药物以2—氯苯甲醛为原料的合成路线如下

(1)A中含有的官能团名称为_________________________。其中1mol有机物A的含氧官能团含有的共用电子对数目为______NA。
(2)C→D的反应类型为_________________ ,有机反应物X的名称为______________。
(3)分子C在一定条件下生成一种含有3个六元环的产物的结构简式为_____________。
(4)写出Y在NaOH醇溶液加热条件下发生反应的化学反应方程式______________。
(5)同时满足下列两个条件的B的同分异构体共有_____种(不包括B,不考虑立体异构)
①与B含有相同的官能团;②苯环上的取代基不超过2个。
(6)已知:![]() ,则仅以甲醇、乙醇为有机原料制备
,则仅以甲醇、乙醇为有机原料制备
![]() 的合成路线流程图为______________________________________。
的合成路线流程图为______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com