
【题目】某化学兴趣小组想利用高岭土(其主要成分是Al2O3·2SiO2·2H2O)实验新型的净水剂。实验程序如下:

其中滤液C就是欲求的净水剂,试回答下列问题:
(1)写出混合物A、B,滤液C、D的主要成分:
A:___________;B:___________;C:___________;D:___________。
(2)写出高岭土与烧碱熔融的两个化学方程式___________。
(3)该实验中,熔融高岭土可以选用的坩埚是______。
A.玻璃坩埚 B.瓷坩埚 C.氧化铝坩埚 D.铁坩埚
【答案】 偏铝酸钠和硅酸钠的混合物 硅酸和氯化铝的混合物 氯化铝 硅酸 SiO2+Na2CO3![]() Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3![]() 2NaAlO2+CO2↑ D
2NaAlO2+CO2↑ D
【解析】
(1)氧化铝和二氧化硅在高温熔融状态下与纯碱反应生成硅酸钠和偏铝酸钠,A中加水溶解并过滤后得到的主要是硅酸钠与偏铝酸钠的混合液,滴加过量盐酸会生成硅酸沉淀和氯化铝溶液,过滤后的不溶物为硅酸,所以A、B、C、D的主要成分是偏铝酸钠和硅酸钠、硅酸和氯化铝、氯化铝、硅酸;
(2)髙岭土与纯碱加热熔融的两个化学方程式分别是SiO2+Na2CO3![]() Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
(3)瓷坩埚、玻璃坩埚的成分中含有二氧化硅,能和纯碱发生反应,氧化铝坩埚也能和纯碱发生反应,在加热时反应易使坩埚炸裂,应选择铁坩埚。
答案选D。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。回答下列问题:

(1)溶液中一定含有的溶质是______________(填化学式)。
(2)溶液中一定不含有的溶质是____________(填化学式)。
(3)溶液中可能含有的溶质是__________(填名称),判断该物质是否存在的实验方法是________,现象是_____________。
(4)分别写出AB段、BC段发生的离子方程式:
①AB段为________________________________;
②BC段为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。

实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
(1)配制混酸的方法是_______________________。反应中需不断搅拌,目的是__________________________________________。
(2)仪器A的名称是______,使用该仪器前必须进行的操作是____。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_____。
(4)分离反应后产物的方案如下:

其中,操作1的名称为______,操作2中需要使用下列仪器中的____(填序号)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(5)该实验中一硝基甲苯的产率为______(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法正确的是( )
A.用加热、蒸发的方法除去粗盐中的CaCl2、MgCl2等杂质
B.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D.用丁达尔现象区分溶液与胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有KOH和Ca(OH)2的混合溶液,c(OH﹣)=0.1 molL﹣1。取此溶液500 mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示。图中(V1)为112 mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )
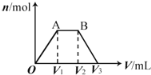
A. 560、672 B. 1008、1120 C. 2240、2352 D. 392、504
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位。请回答下列问题:

(1)图中X是________,Ⅰ在小麦种子中主要是指__________。
(2)在病毒中,携带遗传信息的物质是________________。(填序号)
(3)图中B是______,P的结构通式为________________________。
(4)导致地球上生物多种多样的直接原因是[ ] _________(填序号和名称)结构的多样性。
(5) 若P的平均相对分子质量为100,通过脱水合形成2条肽链,其中肽键的数目为10个,则这2条肽链的相对分子质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)不同温度下的平衡转化率与压强的关系如图所示。

①该反应△H 0,△S 0(填“>”或“<”),则该反 自发进行(填“一定能”、“一定不能”、“不一定”)实际生产条件控制在250℃、l.3×l04kPa左右,选择此压强的理由是 。
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.l mol·L -1。
①该反应的平衡常数K= :
②在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是 (填序号)。
A.氢气的浓度减少
B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加
D.重新平衡时n(H2)/n(CH3OH)增大
③若保持同一反应温度将起始物质改为a mol CO、b mol H2、c mol CH30H,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为 ,且欲使开始时该反应向逆反应方向进行,c的取值范围是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水是用氯气来消毒杀菌的,一些不法商贩用自来水冒充纯净水销售,为辨别纯净水的真伪,可用下列哪种试剂鉴别( )
A.酚酞溶液B.氯化铁溶液C.硝酸银溶液D.氢氧化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com