
A.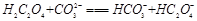 |
B.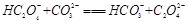 |
C.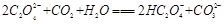 |
D.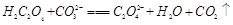 |


科目:高中化学 来源:不详 题型:单选题
| A.取等体积的醋酸和盐酸,分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n |
| B.取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸 |
| C.取等体积的两种酸,分别用完全一样的NaOH溶液进行中和,醋酸消耗NaOH的物质的量比盐酸消耗的多 |
| D.两种酸中c (CH3COO-) > c (Cl-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D. ×100% ×100% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ②
② ③c(H+)和c(OH-)的乘积 ④OH-的物质的量
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol/L氢氰酸溶液的pH约为3 |
| B.HCN易溶于水 |
| C.10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D.HCN溶液的导电性比HCl溶液的弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同浓度的两溶液中c(H+)相同 |
| B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D.两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH4+)/c(OH-) | B.c(OH-)/c(NH3·H2O) |
| C.c(NH3·H2O)/c(NH4+) | D.OH-物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 温度(℃) | 10 | 20 | 30 | 50 | 70 | 80 | 100 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 | 9.6 | 10.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com