
【题目】现有H、N、O、Na、Cl、Fe、Cu七种常见元素,回答下列问题:
(1)Cl位于周期表第____周期____族。
(2)Na+离子的结构示意图为____。
(3)能说明非金属性Cl比N强的事实是____(用方程式表示)。
(4)A~L是由上述七种元素中的一种、二种或三种组成,A的摩尔质量为166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E属同类物质,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如下图所示的关系(部分反应条件及产物已略去):
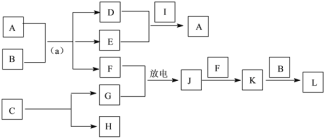
①C的化学式为____。
②D的电子式为____。
③L的稀溶液与H反应的离子方程式为____。
④反应(a)的化学方程式为____。
【答案】 三 ⅦA ![]() 3Cl2+2NH3 =N2+6HCl (或3Cl2+8NH3 =N2+6NH4Cl) Cu3N
3Cl2+2NH3 =N2+6HCl (或3Cl2+8NH3 =N2+6NH4Cl) Cu3N ![]() 3Cu + 8H++2NO3-=3Cu2++2NO↑+4H2O 4Na2FeO4 +10 H2O = 4Fe(OH)3↓+8NaOH + 3O2↑
3Cu + 8H++2NO3-=3Cu2++2NO↑+4H2O 4Na2FeO4 +10 H2O = 4Fe(OH)3↓+8NaOH + 3O2↑
【解析】(1)Cl的原子序数为17,原子结构中有3个电子层,最外层电子数为7,Cl元素位于元素周期表第三周期,第ⅦA族;(2)Na+核外存在10个电子核内有11个质子,其微粒结构示意图为:![]() ;(3)能说明非金属性Cl比N强的事实是3Cl2+2NH3 =N2+6HCl或3Cl2+8NH3 =N2+6NH4Cl;(4)A的摩尔质量为166g·mol-1,其焰色反应呈黄色,则含有钠元素;B是最常见的液体则为水; E呈红褐色则为氢氧化铁,D、E属同类物质,且D应该也含有钠元素故为氢氧化钠。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体即为铜单质,C中两元素的质量比为96∶7;可知生成铜和氮气,故C为,G为氮气,氮气与氧气放电产生NO,故F为氧气,J为一氧化氮,与氧气反应生成K为二氧化氮,二氧化氮与水反应生成L是常见的强酸硝酸,I是黄绿色气体则为氯气;A的摩尔质量为166g·mol-1,其焰色反应呈黄色,则含有钠元素,结合D、E、F可推知A为Na2FeO4。①C的化学式为Cu3N;②D为NaOH,电子式为
;(3)能说明非金属性Cl比N强的事实是3Cl2+2NH3 =N2+6HCl或3Cl2+8NH3 =N2+6NH4Cl;(4)A的摩尔质量为166g·mol-1,其焰色反应呈黄色,则含有钠元素;B是最常见的液体则为水; E呈红褐色则为氢氧化铁,D、E属同类物质,且D应该也含有钠元素故为氢氧化钠。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体即为铜单质,C中两元素的质量比为96∶7;可知生成铜和氮气,故C为,G为氮气,氮气与氧气放电产生NO,故F为氧气,J为一氧化氮,与氧气反应生成K为二氧化氮,二氧化氮与水反应生成L是常见的强酸硝酸,I是黄绿色气体则为氯气;A的摩尔质量为166g·mol-1,其焰色反应呈黄色,则含有钠元素,结合D、E、F可推知A为Na2FeO4。①C的化学式为Cu3N;②D为NaOH,电子式为![]() ;③L的稀溶液与H反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu + 8H++2NO3-=3Cu2++2NO↑+4H2O;④反应(a)的化学方程式为4Na2FeO4 +10 H2O = 4Fe(OH)3↓+8NaOH + 3O2↑。
;③L的稀溶液与H反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu + 8H++2NO3-=3Cu2++2NO↑+4H2O;④反应(a)的化学方程式为4Na2FeO4 +10 H2O = 4Fe(OH)3↓+8NaOH + 3O2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】甲胺(CH3NH2)是一种应用广泛的一元弱碱。常温下,向200mL0.10mol/L的甲胺溶液中滴加V mL.0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是
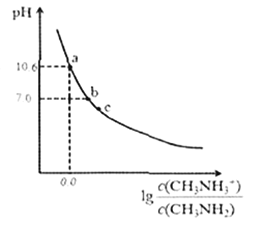
A. b点对应加入盐酸的体积V< 20.00mL
B. 甲胺在水中的电离方程式为:CH3NH2+H2O![]() CH3NH3++OH-
CH3NH3++OH-
C. 常温下,甲胺的电离常数为Kb,则pKb=-1gKb=4.3
D. c点可能存在关系: 2c(H+)+ c(CH3NH3+)=c(CH3NH2) +2c(OH- )+ c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)、碲(Te)为VIA族元素,是当今高新技术新材料的主要成分之一,电解精炼铜的阳极泥主要成分为Cu2Te、Ag2Se和少量金属单质及其他化合物,工业上从其中回收碲、硒的一种工艺流程如下:

已知:
I.Se 单质难溶于水。TeO2微溶于水,易溶于较浓的强酸和强碱;
II.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
III.25℃时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
(1)Se的氢化物的电子式是_______________。0.1mol/L的H2TeO3电离度(当弱电解质在溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来总分子数的百分数叫做电离度) 约为_____________________。
(2) 加入浓硫酸焙烧前常将阳极泥中大块颗粒先粉碎,其目的是_______________________。
(3) SeO2 与SO2在冷却后通入水中反应的化学方程式_________________________________。反应后分离出Se单质的操作①为_________________(填操作名称)。
(4)焙砂中碲以TeO2形式存在,与足量NaOH溶液反应后得到的溶液①,其溶质的主要成分为_______(填化学式,过量的NaOH除外)。工业上也可以通过电解溶液①得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为__________________________________。
(5)向溶液①中加入硫酸时控制溶液的pH 为4.5~5.0,生成TeO2沉淀,如果H2SO4过量,将导致碲的回收率__________(填“偏高”、“偏低”或“无影响”)。
(6)将纯净的TeO2先溶于盐酸得到四氯化碲,然后再将SO2通入到溶液中得到Te单质,请写出由四氯化碲得到Te单质的离子方程式________________________________。
(7)上述流程中可循环利用的物质_______________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
水的离子积常数 | 1×10﹣14 | α | 1×10﹣12 |
试回答下列问题:
(1)若25<t1<t2 , 则α1×10﹣14(填“>”“<”或“=”),作出此判断的理由是 .
(2)25℃下,某Na2SO4溶液中c(SO42﹣)=5×10﹣4 molL﹣1 , 取该溶液1mL,加水稀释至10mL,则稀释后溶液中c (Na+):c (OH﹣)= .
(3)t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2= . 此溶液中各种离子的浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3H2O的电离常数相等,现向10mL浓度为0.1molL﹣1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.![]() 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO﹣)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是
A.最高化合价为+2B.原子半径比钠的大
C.单质与水的反应比钠更剧烈D.最高价氧化物对应的水化物碱性比钠的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构简式如图所示,下列说法错误的是( ) 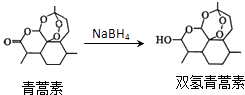
A.青蒿素易溶于苯,难溶于水
B.由青蒿素制备双氢青蒿素的反应属于 还原反应
C.青蒿素可与NaOH溶液在一定条件下发生水解反应
D.双氢青蒿素的同分异构体不可能有芳香族化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10mol/LKOH溶液滴定10.00mL0.10mol/LH2C2O4(二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).请回答: 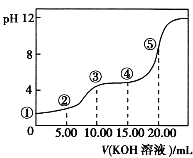
(1)点①所示溶液中,Kw= .
(2)点②所示溶液中的电荷守恒式为 .
(3)点③所示溶液中所有离子的浓度由大到小的顺序为 .
(4)点④所示溶液中的物料守恒式为0.10mol/L= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com