
����Ŀ����һ��������ܱ������н������»�ѧ��Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��_________________________��
(2)�÷�ӦΪ____________(����ȡ����ȡ�)��Ӧ��
(3)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������________��
A��������ѹǿ���� B�����������c(CO)����
C������(H2)������(H2O) D��c(CO2)��c(CO)
(4)ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)��c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ________�档
(5)��800 ��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)Ϊ2 mol��L��1��c(H2)Ϊ1.5 mol��L��1��c(CO)Ϊ1 mol��L��1��c(H2O)Ϊ3 mol��L��1������һʱ�̣���Ӧ��________(���������)���С�
���𰸡�c(CO)c(H2O)/[c(CO2)c(H2)] ���� BC 830 ����
��������
����ƽ�ⳣ���ĺ����Ϸ���ʽ��д����ʽ�������¶ȶԻ�ѧƽ���Ӱ���ж�ƽ�ⳣ�����¶ȵĹ�ϵ�����ݻ�ѧƽ��ı��ʣ����淴Ӧ������ȣ��������������ʵ����ʵ�����Ũ�ȱ��ֲ��䣩�ж�ƽ���־��������ͬ�¶���Ũ������ƽ�ⳣ���Ĺ�ϵ�жϿ��淴Ӧ���еķ���
��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ����ӦCO2(g)��H2(g)![]() CO(g)��H2O(g)�Ļ�ѧƽ�ⳣ������ʽK��c(CO)��c(H2O)/[c(CO2)��c(H2)]��
CO(g)��H2O(g)�Ļ�ѧƽ�ⳣ������ʽK��c(CO)��c(H2O)/[c(CO2)��c(H2)]��
��2�����б������ݱ����������¶����ߣ��÷�Ӧƽ�ⳣ��K����ƽ���ƶ�ԭ��������ƽ�����ƣ�����Ӧ���ȡ�
��3��A�����з�Ӧ��������������䣬��PV��nRT�����º���ʱ������ѹǿ��Ȼ���䣬����������ѹǿ���䡱��һ���ǻ�ѧƽ��״̬��A��ѡ��
B���������������c(CO)���䡱ʱ���������ֳɷֵ�Ũ��Ҳ���䣬��Ϊ��ѧƽ��״̬��Bѡ��
C�������Ƿ�ƽ�⣬����(H2)������(H2O)��������(H2)������(H2O)��ʱ������(H2O)������(H2O)����Ϊ��ѧƽ��״̬��Cѡ��
D����c(CO2)��c(CO)����һ���ǻ�ѧƽ��״̬��D��ѡ��
�ʴ�ѡBC��
��4��ij�¶��£�ƽ��Ũ�ȷ���c(CO2)��c(H2)��c(CO)��c(H2O)����K��1�����ж�Ӧ�¶�Ϊ830�档
��5����800 ��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)Ϊ2 mol��L��1��c(H2)Ϊ1.5 mol��L��1��c(CO)Ϊ1 mol��L��1��c(H2O)Ϊ3 mol��L��1�����ʱ��Ũ����Qc����1mol/L��3mol/L��/��2mol/L��1.5mol/L����1��K��0.9�������һʱ�̣���Ӧ��������С�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ü����Ӧ����ʱ�����ܴﵽĿ���ǣ� ��
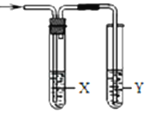
����װ�� ����װ��
���ɵ����� | �Լ� | �Լ� | |
| ��ʯ��ˮ��Ӧ��ȡ����Ȳ |
|
|
| ľ̿��Ũ | ���� | ����ʯ��ˮ |
|
| ˮ |
|
|
|
|
|
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����V1 mL1.00mol��L-1HCl��Һ��V2mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ(ʵ����ʼ�ձ���V1+V2=50mL������������ȷ����(����)
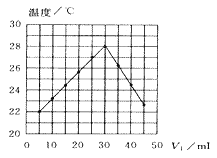
A.����ʵ��ʱ�����¶�Ϊ22��
B.��ʵ�������ѧ�ܿ���ת��Ϊ����
C.NaOH��Һ��Ũ��ԼΪ1.00mol��L-1
D.��ʵ�������ˮ���ɵķ�Ӧ���Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL��������Һ�У���������ʵ���Ũ��Ϊ0.4mol/L����������ʵ���Ũ��Ϊ0.2mol/L�������м���6.4gͭ�ۣ��ȣ�ʹ���ַ�Ӧ������NO�����ʵ���( )
A.0.1molB.0.02molC.0.03molD.0.04mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���淴ӦmA(g)��nB(g)![]() pC(g)���ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��tʱ���¶�T��ѹǿp�뷴Ӧ��B�ڻ�������е��������B%�Ĺ�ϵ���ߣ������߷����������ж���ȷ����
pC(g)���ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��tʱ���¶�T��ѹǿp�뷴Ӧ��B�ڻ�������е��������B%�Ĺ�ϵ���ߣ������߷����������ж���ȷ����
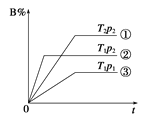
A��T1<T2 p1>p2 m��n>p ���ȷ�Ӧ
B��T1>T2 p1<p2 m��n>p ���ȷ�Ӧ
C��T1<T2 p1>p2 m��n<p ���ȷ�Ӧ
D��T1>T2 p1<p2 m��n<p ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У���ʹ�õ�װ��(�г�װ����)���Լ��Ͳ�����������ȷ����( )
A.�۲�Fe��OH��2������
B.����һ�����ʵ���Ũ�ȵ�NaCO3��Һ
C.��ȥCO�е�CO2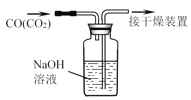
D.ʵ����ģ���Ʊ�NaHCO3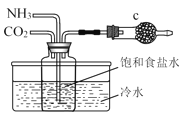
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��Ũ���Ṳ�Ȳ���������X��ͭ��Ũ���ᷴӦ����������Yͬʱͨ��ʢ�������Ȼ�����Һ��ϴ��ƿ��(��ͼװ��)�������й�˵����ȷ����(����)
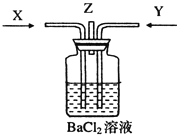
A. ϴ��ƿ�в����ij�������̼�ᱵ B. ��Z���ܳ�����������������̼
C. ϴ��ƿ�в����ij��������ᱵ D. ϴ��ƿ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaNO2��һ��ʳƷ���Ӽ��������°������� KMnO4��Һ�� NaNO2���ķ�Ӧ����ʽ��MnO4-+NO2-+����Mn2++NO3-+H2O��������������ȷ����( )
A. �÷�Ӧ�� NO2-����ԭ B. ��Ӧ��������Һ��pH ��С
C. ����1 mol NaNO3������ 0.4mol KMnO4 D. ��������� OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ի���������������������Ⱦ��кܴ��Ӱ�졣�밴Ҫ��ش���������
(1)����ij����ɸ��������NH3���ѳ����������е�NO��NO2����Ӧ��������ͼ��ʾ��A��������ΪH2O��___________(�ѧʽ)

(2)��֪��4NH3(g)+6NO(g) =5N2(g)+6H2O(g) ��H1=��a kJ/mol
4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) ��H2=��b kJ/mol
H2O(l)=H2O(g) ��H3=+c kJ/mol
��Ӧ4NH3(g)+3O2(g)=2N2(g)+6H2O(l)����H=___________ kJ/mol
(3)��ҵ�����ð�������������(HCN�ķ�ӦΪ��CH4(g)+NH3(g)![]() HCN(g)+3H2(g ) ��H>0
HCN(g)+3H2(g ) ��H>0
����������һ�����ﵽƽ��ʱNH3ת�������������X�仯�Ĺ�ϵ��ͼ����ʾ����X������___________(����ĸ���)

a���¶� b��ѹǿ c������ d��![]()
����һ���¶��£���2L�ܱ������м��� n mol CH4��2 moI NH3��ƽ��ʱNH3���������n�仯�Ĺ�ϵ��ͼ����ʾ��

a��ʱ��CH4��ת����Ϊ___________%��ƽ�ⳣ����K(a)_____K(b)(����>����=������<��)��
(4)�����еļ��쵰��(Mb)��O2�������MbO2���䷴Ӧԭ���ɱ�ʾΪ�� Mb(ag)+O2(g)![]() MbO2(aq)���÷�Ӧ��ƽ�ⳣ���ɱ�ʾΪ��
MbO2(aq)���÷�Ӧ��ƽ�ⳣ���ɱ�ʾΪ��![]() ����37�������´ﵽƽ��ʱ����ü��쵰�Ľ�϶�(a)��P(O2)�Ĺ�ϵ��ͼ����ʾ[
����37�������´ﵽƽ��ʱ����ü��쵰�Ľ�϶�(a)��P(O2)�Ĺ�ϵ��ͼ����ʾ[![]() ]���о���������Ӧ��������=k����c(Mb) �� P(O2)���淴Ӧ��������=k����c(MbO2)(����k����k���ֱ��ʾ����Ӧ���淴Ӧ�����ʳ���)��
]���о���������Ӧ��������=k����c(Mb) �� P(O2)���淴Ӧ��������=k����c(MbO2)(����k����k���ֱ��ʾ����Ӧ���淴Ӧ�����ʳ���)��

����д��ƽ�ⳣ��K�����ʳ���k����k��֮��Ĺ�ϵʽΪK=___________(�ú���k����k����ʽ�ӱ�ʾ)��
�������ͼ����c��ʱ��������Ӧ��ƽ�ⳣ��K=___________kPa��1����֪k��=60s��1�������ʳ���k��=___________s��1��kPa��1��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com