
����Ŀ��800��ʱ����2L���ܱ������з�����Ӧ��2NO��g��+O2��g��2NO2 �� n��NO����ʱ��ı仯�����ʾ��
ʱ��Ms | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO���Mmol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����0��3s�ڣ���NO��ʾ��ƽ����Ӧ����v��NO��= ��
��2��ͼ�б�ʾNOŨ�ȱ仯��������������ĸ���ţ��� 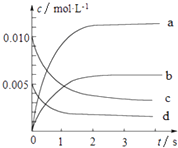
��3����ƽ��ʱNO��ת����Ϊ ��
��4����˵���÷�Ӧ�Ѵﵽƽ��״̬����������ţ��� A������������ɫ���ֲ���
B�����������ܶȱ��ֲ���
C��v�� ��NO2��=2v�� ��O2��
D����������ƽ����Է����������ֲ���
��5�������µ�850�棬��ƽ���n��NO��=n��NO2������Ӧ���������Ӧ�����淴Ӧ�����ƶ���
��6������һ��������0.2molNO������������Ӧ����ƽ��ʱ��÷ų�������ΪakJ����ʱNOת����Ϊ80%����2molNO������ȫ��Ӧ�ų�������Ϊ ��
���𰸡�
��1��2.17��10��3mol?L��1?s��1
��2��c
��3��65%
��4��A��C��D
��5���淴Ӧ����
��6��12.5akJ
���������⣺��1���ɱ��������ݿ�֪��0��3s�ڣ���n��NO��=��0.020��0.007��mol=0.013mol��v��NO��= ![]() =2.17��10��3molL��1s��1 �� ���Դ��ǣ�2.17��10��3molL��1s��1����2����2��NO��O2Ϊ��Ӧ�����ʱ������ƣ�NO��O2�����ʵ�����С����c��NO������c��O2��=2��1�����c��ʾNOŨ�ȱ仯�����ߣ�d��ʾO2Ũ�ȱ仯�����ߣ����Դ��ǣ�c����3��3sʱ����ƽ��״̬��ƽ��ʱNOΪ0.007mol��NOת����=
=2.17��10��3molL��1s��1 �� ���Դ��ǣ�2.17��10��3molL��1s��1����2����2��NO��O2Ϊ��Ӧ�����ʱ������ƣ�NO��O2�����ʵ�����С����c��NO������c��O2��=2��1�����c��ʾNOŨ�ȱ仯�����ߣ�d��ʾO2Ũ�ȱ仯�����ߣ����Դ��ǣ�c����3��3sʱ����ƽ��״̬��ƽ��ʱNOΪ0.007mol��NOת����= ![]() ��100%=
��100%= ![]() ��100%=65%�����Դ��ǣ�65%����4��A������������ɫ���ֲ��䣬˵��NO2��Ũ�ȱ��ֺ㶨��˵���÷�Ӧ�Ѵﵽƽ��״̬��B����
��100%=65%�����Դ��ǣ�65%����4��A������������ɫ���ֲ��䣬˵��NO2��Ũ�ȱ��ֺ㶨��˵���÷�Ӧ�Ѵﵽƽ��״̬��B���� ![]() ��֪���������ܶ�ʼ�ձ��ֲ��䣬����˵���÷�Ӧ�Ѵﵽƽ��״̬��C����Ϊ
��֪���������ܶ�ʼ�ձ��ֲ��䣬����˵���÷�Ӧ�Ѵﵽƽ��״̬��C����Ϊ ![]() ������v�� ��NO2��=2v�� ��O2��=v�� ��NO2����˵���÷�Ӧ�Ѵﵽƽ��״̬��D������M=
������v�� ��NO2��=2v�� ��O2��=v�� ��NO2����˵���÷�Ӧ�Ѵﵽƽ��״̬��D������M= ![]() ��m�Ƕ�ֵ��n�DZ���������MΪ��������˻�������ƽ����Է����������ֲ��䣬˵���÷�Ӧ�Ѵﵽƽ��״̬�����Դ��ǣ�ACD����5�����µ�850�棬ƽ���n��NO��=n��NO2��������Nԭ���غ��֪n��NO��=n��NO2��=0.1mol��ƽ�����淴Ӧ���У����Դ��ǣ��淴Ӧ����6��ת����NO�����ʵ���Ϊ2mol��80%=0.16mol���ų�������ΪakJ������2molNO��Ӧ�ų�������Ϊ
��m�Ƕ�ֵ��n�DZ���������MΪ��������˻�������ƽ����Է����������ֲ��䣬˵���÷�Ӧ�Ѵﵽƽ��״̬�����Դ��ǣ�ACD����5�����µ�850�棬ƽ���n��NO��=n��NO2��������Nԭ���غ��֪n��NO��=n��NO2��=0.1mol��ƽ�����淴Ӧ���У����Դ��ǣ��淴Ӧ����6��ת����NO�����ʵ���Ϊ2mol��80%=0.16mol���ų�������ΪakJ������2molNO��Ӧ�ų�������Ϊ ![]() ��akJ=12.5aKJ�����Դ��ǣ�12.5akJ��
��akJ=12.5aKJ�����Դ��ǣ�12.5akJ��
�����㾫�������÷�Ӧ���ʵĶ�����ʾ�����ͻ�ѧƽ��״̬���ж϶���Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��Ӧ���ʵĵ�λ��mol/(L��min)��mol/(L��s) v=��c-��t��״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���ȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�м�����Ƭ�����������������Һ��һ���ܴ���������������ǣ� ��
A.Cl����Fe3+
B.HCO3����Al3+
C.Ba2+��SO42��
D.Na+��SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ܿ������ܡ����ܵ��ת�������б�������ȷ���ǣ� �� 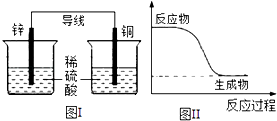
A.��ѧ��Ӧ�������仯����Ҫԭ���ǻ�ѧ���Ķ������γ�
B.�кͷ�Ӧ�У���Ӧ��������������������������
C.ͼI��ʾ��װ���ܽ���ѧ��ת��Ϊ����
D.ͼII��ʾ�ķ�ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���穁Fenton��������ˮ�����л���Ⱦ�オ��ĸ������������䷴Ӧԭ����ͼ��ʾ�����е�������H2O2��Fe2+����Fenton��Ӧ��Fe2++H2O2=Fe3++OH��+OH�����ɵ��������ɻ���OH�������������л���Ⱦ�����˵������ȷ���ǣ� �� 
A.��Դ��A���Ǹ���
B.������ֻ��O2��Fe3+������ԭ��Ӧ
C.�����Ϸ����缫��Ӧ��H2O��e��=OH+H+ ��
D.����1molO2 �� ���Բ���4molOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��D��E��F��G���ֶ����ڵ�����Ԫ�أ�A��ԭ�Ӱ뾶��С��B����������������������������2����B��D�г��ȼ����������ۻ�����BD2 �� E+��D2��������ͬ�ĵ��Ӳ�ṹ��G��Dͬ���壬A������F������ȼ�յIJ�������ˮ�õ�һ��ǿ��X����ش��������⣺
��1��BD2�ĽṹʽΪ ��
��2��GԪ����Ԫ�����ڱ��е�λ��Ϊ �� ��GD2���������Ƶ�F���ʵ�ˮ��Һ�����ӷ���ʽΪ ��
��3�������Ԫ���к�AԪ�صĶ�Ԫ���ӻ�����ĵ���ʽΪ �� D��E�γɵĻ��������DZˮ����еĹ���������û�������ˮ��Ӧ�����ӷ���ʽΪ ��
��4��A��B��D��Ԫ������ɵ�ijһԪ��Y���ճ������г�����һ�ֵ�ζ�����ڵ������Ũ�ȵ�X��Y��Һ�м�����״��ͬ��������п�������ߵ�ƽ����Ӧ���ʵĴ�С��ϵ��XY�������������=������
��5����A��D��E��G��Ԫ�ؿ��γ�������ʽ�Σ�����������ʽ����ˮ��Һ�з�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��N2(g)��3H2(g) ![]() 2NH3(g)(����ӦΪ���ȷ�Ӧ)��2SO2(g)��O2(g)
2NH3(g)(����ӦΪ���ȷ�Ӧ)��2SO2(g)��O2(g)![]() 2SO3(g)(����ӦΪ���ȷ�Ӧ)��
2SO3(g)(����ӦΪ���ȷ�Ӧ)��
��ش��������⣺
��1����Ӱ�컯ѧ��Ӧ���ʺͻ�ѧƽ������ط�����Ҫ������NH3��SO3�����ɣ�������Ӧ��ȡ�Ĵ�ʩ����ʵ�������в�ȡ�Ĵ�ʩ���� ��
��2���ںϳɰ��Ĺ�ҵ�����У�Ҫ���������Ŀ���������ϳ�SO3�Ĺ����У�����Ҫ�����SO3 �� ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��Ӧ����C���ٶ���Ӧ��A��B��ʼ�����ǵ���ʼŨ�Ⱦ�Ϊ1mol/L����Ӧ����2min��A��Ũ��Ϊ0.8mol/L��B��Ũ��Ϊ0.6mol/L��C��Ũ��Ϊ0.6mol/L����2min�ڷ�Ӧ��ƽ������VB= �� �÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ���������е����ʣ������Լ��ͷ�������ȷ���� �� ��
���� | ���� | �����������Լ��ͷ��� | |
A | KCl��Һ | I2 | CCl4����ȡ |
B | KNO3 | K2SO4 | Ba��NO3��2��Һ������ |
C | Cu | CuO | ���ᣬ���� |
D | CaCO3 | CaO | ���ᣬ���� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭƬ��пƬ��200mL ϡH2SO4��ɵ�ԭ����У���пƬֻ�����绯ѧ��Ӧ����ͭƬ�Ϲ��ų�3.36L����״��������ʱ��H2SO4ǡ����ȫ���ģ���
��1����Ӧ�����ĵ�п�������Ƕ��٣���Zn��65��
��2���ж��ٸ�����ͨ���˵��ߣ�
��3��ԭϡH2SO4�����ʵ���Ũ���Ƕ��٣�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com