
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���д���пհף�
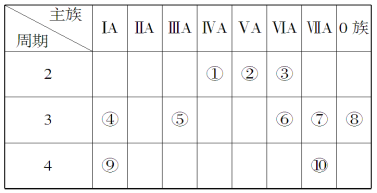
(1)Ԫ�آߵ�����Ϊ______�������ڱ��е�λ��______________��
(2)������������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ��_______��������ǿ�Ļ�����ĵ���ʽ��__________��
(3)�õ���ʽ��ʾԪ�آܺ͢Ļ�������γɹ��̣�____________���û���������______(��������������������)�����
(4)д��һ��������Ԫ����ɵļ������Ӽ����й��ۼ������ʵĻ�ѧʽ______��
(5)�ޡ��ߡ�������Ԫ���γɵ����ӣ����Ӱ뾶�ɴ�С��˳����_________(�����ӷ��ű�ʾ)
���𰸡��� �������ڵ���A�� HClO4 ![]()
![]() ���� KOH��NaOH��Na2SO4��NaClO��Na2O2��K2O2�� S2����Cl����K+
���� KOH��NaOH��Na2SO4��NaClO��Na2O2��K2O2�� S2����Cl����K+
��������
��Ԫ�������ڱ��е�λ�ÿ�֪����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK����ΪBr��
(1)Ԫ�آ�Ϊ��Ԫ�أ�λ��Ԫ�����ڱ��������ڵ���A�壻
(2)�ǽ�����Խǿ����������������Խǿ��ͬһ��������Ԫ���������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ�������Oû�к����ᣬ��������������ˮ����������ǿ��Ԫ��ΪCl����Ӧ����ΪHClO4��������Խǿ������������ˮ�������Խǿ��ͬ��������Ԫ���������ҽ����Լ�����ͬ�������϶��½�������ǿ������ͼʾԪ���н�������ǿ����K����Ӧ�ļ�ΪKOH������ʽΪ![]() ��
��
(3)��ΪNa����ΪS�������γɿ��γ����������������ӹ��ɵ����ӻ�����Na2S�����γɹ���Ϊ��![]() ��
��
(4)����Ԫ����ɵļ������Ӽ����й��ۼ��������ж��֣���KOH��NaOH�ȼNa2SO4��NaClO�Ⱥ������Σ�����Na2O2��K2O2�ȣ�
(5)��ΪS����ΪCl����ΪK������Ԫ���γɵ����ӵ��Ӳ�����Ϊ3�㣬���Ӳ�����ͬ�˵����ԽС�뾶Խ���������Ӱ뾶�ɴ�СΪS2����Cl����K+��


 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д� ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����nAΪ����٤����������ֵ������˵����ȷ����
A. 23g Na ������H2O��Ӧ��ȫ�������nA��H2����
B. 1 molCu��������Ũ���ᷴӦ������nA��SO3����
C. ��״���£�22.4L N2��H2������к�nA��ԭ��
D. 3mol����Fe��ȫת��ΪFe3O4��ʧȥ8nA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������漰���ӷ���ʽ��д�����ۺ������ǣ��� ����
ѡ�� | ��ѧ��Ӧ�����ӷ���ʽ | ���� |
A | ���������Һ��ͨ������SO2��Ca2+��ClO����SO2��H2O===CaSO4����Cl����2H�� | ��ȷ |
B | ʵ������Ũ������MnO2��Ӧ��Cl2��MnO2��4H����2Cl�� | ����H����Cl���Ļ�ѧ������Ӧ��� |
C | ��������Һ�мӹ�����ˮ��Fe3����3NH3��H2O===Fe��OH��3�����壩��3NH4+ | ����Fe��OH��3Ӧ���dz��� |
D | ������̼���У�2Al��3H2CO3===2Al3����3H2����3CO32- | ��ȷ |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����24.4 g NaOH��������ˮ���100 mL��Һ�����ܶ�Ϊ1.219 g/mL��
��1������Һ��NaOH�����ʵ���Ũ��Ϊ________mol/L��
��2������Һ��NaOH����������Ϊ________��
��3���Ӹ���Һ��ȡ��10 mL������NaOH�����ʵ���Ũ��Ϊ________ mol/L����NaOH�����ʵ���Ϊ________��
��4����ȡ����10 mL��Һ��ˮϡ�͵�100 mL��ϡ�ͺ���Һ��NaOH�����ʵ���Ũ��Ϊ________mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ�Ķ��ֻ����������������ж��й㷺��;����ش��������⣺
��1��Cu2O��CuO��ͭ������������ɻ���ת������֪��
i.2Cu2O(s)��O2(g)=4CuO(s) ��H=-292.0kJ��mol-1
ii.C(s)��2CuO(s)=Cu2O(s)��CO(g) ��H=��35.5kJ��mol-1
��CO��ȼ����Ϊ283.0kJ��mol-1����C(s)��ȼ����Ϊ___��
��2��Cu2O��CuO������������
�����ӽ���Ĥȼ�ϵ��(PEMFC)��ȼ�����г�����H2�����������CO��CO2������CO��PEMFC���������ض�����������CuO/CeO2���������������ѳ�CO��160�桢��CuO/CeO2������ʱ������CO�Ļ�ѧ����ʽΪ___���ֱ���HIO3��H3PO4��CuO/CeO2���д�������һ�������£����ò�ͬ��������CO�����ĶԱ�ʵ�飬����ͼ���ߣ����д���___ (����b������c��)��������ã�120��ʹ�ô���b������������ȼ������CO���������Ϊ0.71%����������Ϊ2000mL��h-1����1h��CO���Ϊ___mL��

����Cu2O�������ºϳ�CH3OH����Ӧ���£�CO(g)��2H2(g)![]() CH3OH(g) ��H=-90.0kJ��mol-1����������߸÷�ӦCO��ƽ��ת���ʵ�������___(����)��
CH3OH(g) ��H=-90.0kJ��mol-1����������߸÷�ӦCO��ƽ��ת���ʵ�������___(����)��
A.���µ�ѹ B.���¸�ѹ C.���¸�ѹ D.���µ�ѹ
T��ʱ����CO��H2��һ��������Ϻ�Ͷ���ݻ�Ϊ2L�ĺ����ܱ������У�CO����ʼŨ��Ϊ1.0mol��L-1��ƽ��ʱ�������ϵ�У�n(H2)=1.4mol��n(CH3OH)=1.7mol����Ӧ�ﵽƽ��ʱCO��ת����Ϊ___������Ӧ�ﵽƽ��״̬���������������䣬�ٳ���0.2molCO��0.2molCH3OH��ƽ����___(����������������)��Ӧ�����ƶ���������___��
��3��CuS�ʺ�ɫ���������ܵ�����֮һ����������������ʹ��һЩ���Ʋ����ܵķ�Ӧ���Է�������0.01mol��L-1CuSO4��Һ�У�����ͨ��H2Sά�ֱ���(H2S����Ũ��Ϊ0.1mol��L-1)��������Ӧ��H2S(aq)��Cu2��(aq)![]() CuS(s)��2H��(aq)���÷�Ӧ�Ļ�ѧƽ�ⳣ��KΪ___(����2λ��Ч����)����֪��Ka1(H2S)=1.1��10-7��Ka2(H2S)=1.3��10-13��Ksp(CuS)=6.3��10-36��
CuS(s)��2H��(aq)���÷�Ӧ�Ļ�ѧƽ�ⳣ��KΪ___(����2λ��Ч����)����֪��Ka1(H2S)=1.1��10-7��Ka2(H2S)=1.3��10-13��Ksp(CuS)=6.3��10-36��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���F���������㾫������������·�ߺϳɡ�
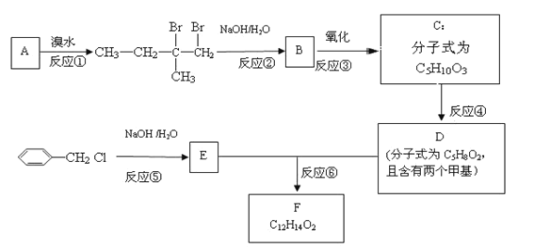
�ش��������⣺
��1��A�Ļ�ѧ������______________��
��2��B�Ľṹ��ʽ��______________��D�й����ŵ�������_____________��
��3���١���������ȡ����Ӧ����________________(�����)��
��4����Ӧ�Ļ�ѧ����ʽΪ_________________________________________________��
��5��C�ж���ͬ���칹�壬��C������ͬ�����ŵ���_________��(������C)�����к˴Ź�������Ϊ�����Ľṹ��ʽΪ_________(��дһ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦC(s)��H2O(g) ![]() CO(g)��H2(g)��һ�ɱ��ݻ����ܱ������н��У����������ĸı��ʹ��Ӧ���ʼӿ����(����)
CO(g)��H2(g)��һ�ɱ��ݻ����ܱ������н��У����������ĸı��ʹ��Ӧ���ʼӿ����(����)
A. ����C����
B. �������������Сһ��
C. ����������䣬���뵪��ʹ��ϵ��ѹǿ����
D. ����ѹǿ���䣬���뵪��ʹ��ϵ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H3PO4)��һ����ǿ�ᣬ�����£�H3PO4ˮ��Һ�к������ķֲ�����(ƽ��ʱij����Ũ��ռ����������Ũ�ȵķ���)��pH�Ĺ�ϵ����ͼ������˵����ȷ����
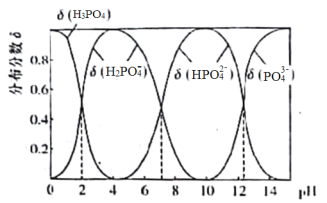

A.�μ�NaOH��Һ��pH=7����Һ��c(Na+)��c(H2PO4-)+c(HPO42��)+c(PO43��)
B.���¶��£�H3PO4���������볣��Ka3��10-12
C.H3PO4�ĵ��뷽��ʽΪ��H3PO4 3H+ + PO43��
D.�μ�����Na2CO3��Һ����ѧ��Ӧ����ʽΪ3 Na2CO3 + 2H3PO4=2Na2PO4+3H2O+3CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ�������������
I.�������������
��14C ��16O ��14N ��18O ��O2 ��O3
��CH3-CH3 ��C2H6 ��CH3- CH2-OH �� CH3-O-CH3
(1)��Ϊͬλ�ص���______��(����ţ���ͬ)��������ͬ��������ͬ����______________
(2)��Ϊͬ�����������_________, ��Ϊͬ���칹�����_____________________
II.��25 C��101 kPa�������£�

���ڷ�ӦH2(g)+Cl2(g)= 2HCl(g), �������2 mol HCI(g)ʱ,��Ӧ�����зų�183 kJ����������Ͽ�1 mol H- Cl�������������____ kJ.

III.��ͼ��ʾ��ԭ���װ���У������ĵ缫��Ӧ����ʽ��________________________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com