
【题目】下列涉及离子方程式书写的评价合理的是( )
选项 | 化学反应及离子方程式 | 评价 |
A | 次氯酸钙溶液中通入足量SO2:Ca2++ClO-+SO2+H2O===CaSO4↓+Cl-+2H+ | 正确 |
B | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4H++2Cl- | 错误,H+、Cl-的化学计量数应相等 |
C | 硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O===Fe(OH)3(胶体)+3NH4+ | 错误,Fe(OH)3应该是沉淀 |
D | 铝溶于碳酸中:2Al+3H2CO3===2Al3++3H2↑+3CO32- | 正确 |
A. AB. BC. CD. D
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用糖类物质制备乙酸乙酯的合成路线之一如下图所示:
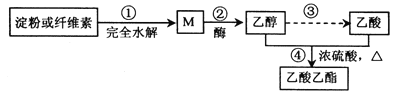
下列说法正确的是( )
A. 淀粉和纤维素互为同分异构体
B. 反应②:1 mol M 在酒化酶作用下可生成3 molCH3CH2OH
C. 反应③:乙醇变乙酸所需反应条件可为酸性重铬酸钾溶液
D. 反应④:产物通入滴有酚酞的饱和碳酸钠溶液中振荡,无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车发动机稀燃控制系统主要工作原理是发动机在稀燃和富燃条件下交替进行,尾气中的NOx在催化剂上反应脱除。其工作原理示意图如下:

下列说法不正确的是
A. 稀燃过程中,NO发生的主要反应为:2NO + O2 === 2NO2
B. 稀燃过程中,NO2被吸收的反应为:BaO + 2NO2 === Ba(NO3)2
C. 富燃过程中,NO2被CO还原的反应为:2NO2 + 4CO === N2 + 4CO2
D. 富燃过程中,CxHy被O2氧化的反应为:CxHy + (x+y/4)O2 == xCO2 + y/2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3X(g)+Y(g)2Z(g)+2W(g)在 2L密闭容器中进行,10 min后 Y减少了1.0 mol,则此反应的平均速率v为
A.v(X)=0.05mol·L-1·min-1B.v(Z)=0.10mol·L-1·min-1
C.v(Y)=0.10mol·L-1·min-1D.v(W)=0.05mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铁离子,氯气、溴均为常见的氧化剂,某化学兴趣小组设计了如下实验探究其强弱:
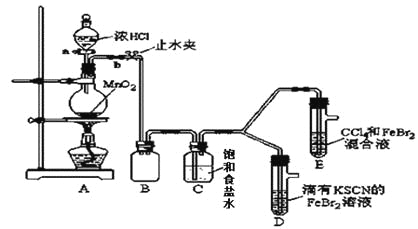
(1)①装置A中发生反应的离子方程式是_________________。
②整套实验装置存在一处明显的不足,请指出________。
(2)用改正后的装置进行实验,实验过程如下:
实验操作 | 实验现象 | 结论 |
打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后_______________。(填具体实验操作) | D装置中:溶液变红 E装置中:水层溶液变黄, 振荡后,下层CCl4层无明显变化。一段时间后______。(填实验现象) | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为:Cl2>Br2>Fe3+ |
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化。
D装置中:红色慢慢褪去。
E装置中:CCl4层颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
ⅰ.Fe3+ +3SCN-![]() Fe(SCN)3是一个可逆反应。
Fe(SCN)3是一个可逆反应。
ⅱ.(SCN)2性质与卤素单质类似。氧化性:Cl2 > (SCN)2。
①请用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因____。现设计简单实验证明上述解释:取少量褪色后的溶液,滴加________溶液,若溶液颜色______________。则上述解释是合理的。
小组同学另查得资料如下:
ⅲ.Cl2和Br2反应生成BrCl,BrCl呈红色(略带黄色),沸点约5℃,它与水能发生水解反应,且该反应为非氧化还原反应。
ⅳ.AgClO、AgBrO均可溶于水。
②欲探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步离子方程式解释仅产生白色沉淀原因___________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )
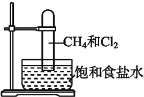
A. 此反应无光照也可发生
B. 盛放饱和食盐水的水槽底部会有少量晶体析出
C. 甲烷和Cl2反应后的产物只有CH3Cl和HCl
D. CH4和Cl2完全反应后液面上升,液体充满试管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气和氯气混合光照即可发生爆炸而释放出大量的热量。在反应过程中,断裂1 mol H2中的化学键消耗的能量为Q1 kJ,断裂1 molCl2中的化学键消耗的能量为Q2 kJ,形成1 mol HCl中的化学键释放的能量为Q3 kJ。下列关系式中正确的是
A.Q1+ Q2<2Q3B.Q1+ Q2>2Q3C.Q1+ Q2<Q3D.Q1+ Q2>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
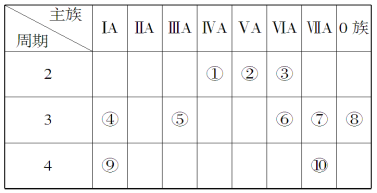
(1)元素⑦的名称为______,在周期表中的位置______________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______,碱性最强的化合物的电子式是__________。
(3)用电子式表示元素④和⑥的化合物的形成过程:____________,该化合物属于______(填“共价”或“离子”)化合物。
(4)写出一种由上述元素组成的既有离子键又有共价键的物质的化学式______。
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是_________(用离子符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用氟化钙固体和浓硫酸混合加热制HF:CaF2+H2SO4(浓)![]() CaSO4+2HF↑。下列关于该反应的说法错误的是
CaSO4+2HF↑。下列关于该反应的说法错误的是
A.该反应利用了浓硫酸的酸性和难挥发性
B.CaF2晶体中Ca2+和F-的配位数之比为1:2
C.影响H2SO4和CaSO4熔点的作用力不同
D.HF是极性分子且分子极性强于HC1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com