
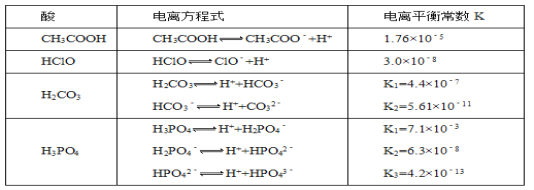
【题目】化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示)。下表是某温度下几种常见弱酸的电离平衡常数:
回答下列问题:
(1)若把CH3COOH、HClO、H2CO3、HCO3-、H3PO4、H2PO4-、HPO42-都看作是酸,则它们酸性最强的是___________(填化学式,下同),最弱的是_________________
(2)向NaClO溶液中通入少量的二氧化碳,发生的离子方程式为__________________________,1.2molL﹣1的NaClO溶液pH=__________________________(已知:lg2=0.3)。
(3)求出该温度下,0.10molL﹣1的CH3COOH溶液中的c(H+)=____________molL﹣1。
【答案】H3PO4 HPO42 CO2+ClO+H2O═HClO+HCO3 10.8 1.33×103
【解析】
(1)同一温度下,酸的电离常数越大其酸性越强,根据酸的电离常数知,则它们酸性强弱顺序是:![]() ,所以酸性最强的是
,所以酸性最强的是![]() ,最弱的是
,最弱的是![]() ;
;
(2)因为酸性:![]() ,碳酸的酸性强于次氯酸,所以反应的离子方程式为:
,碳酸的酸性强于次氯酸,所以反应的离子方程式为:![]() ═
═![]() ;
;
1.2mol/L的NaClO溶液中水解离子方程式为:![]()
![]() ,Kh=
,Kh=![]() =
=![]() =
=![]() =
=![]() ×10-6,由于ClO-的水解程度较小,所以c(HClO)≈c(OH-),c(HClO)≈1.2mol/L,则c(OH-)=
×10-6,由于ClO-的水解程度较小,所以c(HClO)≈c(OH-),c(HClO)≈1.2mol/L,则c(OH-)=![]() =2×10-3.5mol/L,
=2×10-3.5mol/L,![]() mol/L,pH=-lg(5×10-11.5)=10.8;
mol/L,pH=-lg(5×10-11.5)=10.8;
(3)该温度下,0.1mol/L的CH3COOH溶液中存在电离平衡CH3COOH![]() ,平衡常数
,平衡常数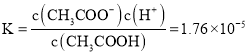 ,由于电离程度较小,c(CH3COO-)≈c(H+),c(CH3COOH)≈0.1mol/L,
,由于电离程度较小,c(CH3COO-)≈c(H+),c(CH3COOH)≈0.1mol/L,![]() ,c(H+)=1.33×10-3mol/L。
,c(H+)=1.33×10-3mol/L。


科目:高中化学 来源: 题型:
【题目】化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
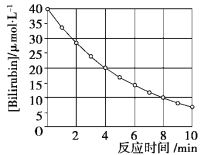
A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
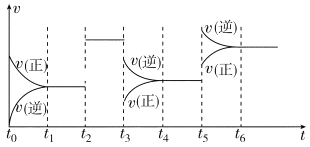
A.t2时加入了催化剂B.t3时降低了温度
C.t5时增大了压强D.t4~t5时间内X转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)![]() CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
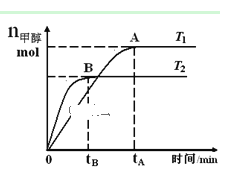
A.平衡常数K =![]()
B.该反应在T1时的平衡常数比T2时的小
C.任意时刻,T2温度下的反应速率均大于T1温度下的速率
D.处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)X元素在周期表中的位置为__。
(2)NH3的电子式为__。
(3)下列事实能说明Y 元素的非金属性比S 元素的非金属性强的是__。
a.Y 单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y 单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)常温下,碳与镁形成的 1 mol 化合物Q 与水反应,生成2 mol Mg(OH)2和 1 mol 气态烃,该烃中碳氢质量比为 9:1。写出化合物Q 与水反应的化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是一种重要的金属元素,具有多种价态,单质铬是硬度最大的金属,熔点为![]() 。回答下列问题:
。回答下列问题:
![]() 工业上以铬铁矿
工业上以铬铁矿![]() 主要成分是
主要成分是![]() 为原料冶炼铬的流程如图所示:
为原料冶炼铬的流程如图所示:
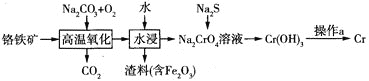
![]() 中铬元素的化合价为_________。
中铬元素的化合价为_________。
![]() 高温氧化时发生反应的化学方程式为________________。
高温氧化时发生反应的化学方程式为________________。
![]() 操作a由两种均发生了化学反应的过程构成,其分别是_________、铝热反应。
操作a由两种均发生了化学反应的过程构成,其分别是_________、铝热反应。
![]() 是两性氢氧化物,请写出其电离方程式_________________。
是两性氢氧化物,请写出其电离方程式_________________。
![]() 铬元素能形成含氧酸及含氧酸盐,若测得浓度为
铬元素能形成含氧酸及含氧酸盐,若测得浓度为![]() 的铬酸
的铬酸![]() 溶液中含铬元素的微粒浓度分别为
溶液中含铬元素的微粒浓度分别为![]() 、
、![]() 、
、![]() ,试推测
,试推测![]() 溶液呈________
溶液呈________![]() 填“酸”“碱”或“中”
填“酸”“碱”或“中”![]() 性,原因是______________。
性,原因是______________。
![]() 水中的铬元素对水质及环境均有严重的损害作用,工业上用下述方法来进行无害化处理并获得有价值的产品。
水中的铬元素对水质及环境均有严重的损害作用,工业上用下述方法来进行无害化处理并获得有价值的产品。
![]() 电解处理含有
电解处理含有![]() 的污水:用铁作电极电解污水,
的污水:用铁作电极电解污水,![]() 被阳极区生成的离子还原成
被阳极区生成的离子还原成![]() ,生成的
,生成的![]() 与阴极区生成的
与阴极区生成的![]() 结合生成
结合生成![]() 沉淀而除去。则阴极上的电极反应式为_______,若要处理
沉淀而除去。则阴极上的电极反应式为_______,若要处理![]() 浓度为
浓度为![]() 的污水,理论上需要消耗_______kg的铁。
的污水,理论上需要消耗_______kg的铁。
![]() 转化为有价值的产品磁性铁铬氧体
转化为有价值的产品磁性铁铬氧体![]() :先向含
:先向含![]() 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气![]() 氧化部分
氧化部分![]() 并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。写出
并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。写出![]() 在酸性条件下被
在酸性条件下被![]() 还原为
还原为![]() 的离子方程式__________,若处理含
的离子方程式__________,若处理含![]() 不考虑其他含铬微粒
不考虑其他含铬微粒![]() 的污水时恰好消耗
的污水时恰好消耗![]() ,则当铁铬氧体中
,则当铁铬氧体中![]() 时,铁铬氧体的化学式为_______________。
时,铁铬氧体的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一真空密闭容器中盛有1 mol PCl5,加热到200 ℃,发生反应:PCl5(g) ![]() PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2 mol PCl5,反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m和n的关系正确是( )
PCl3(g)+Cl2(g),反应达到平衡时,PCl5在混合气体中的体积分数为m%,若在相同的温度和相同的容器中,起始时加入2 mol PCl5,反应达到平衡时,PCl5在混合气体中的体积分数为n%,则m和n的关系正确是( )
A.m>nB.m<nC.m=nD.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电解技术,以氯化氢为原料回收氯气的过程如图所示,下列说法不正确的是

A.H+由阳极区向阴极区迁移
B.阳极电极反应:2HCl + 2e- == Cl2 + 2H+
C.阴极电极反应:Fe3+ + e- == Fe2+
D.阴极区发生的反应有:4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+要使溶液中
CH3COO-+H+要使溶液中![]() 值增大,可以采取的措施是( )
值增大,可以采取的措施是( )
A.加少量烧碱溶液B.降低温度
C.加少量冰醋酸D.加水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com