
【题目】在恒容密闭容器中,由CO合成甲醇:CO(g) + 2H2(g)![]() CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
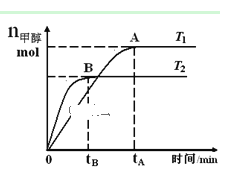
A.平衡常数K =![]()
B.该反应在T1时的平衡常数比T2时的小
C.任意时刻,T2温度下的反应速率均大于T1温度下的速率
D.处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
科目:高中化学 来源: 题型:
【题目】室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。下列说法正确的是
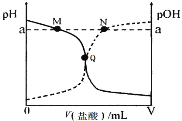
A.M点所示溶液c(![]() )+c(NH3·H2O)= c(Cl-)
)+c(NH3·H2O)= c(Cl-)
B.N点所示溶液中:c(![]() )>c(Cl-)
)>c(Cl-)
C.Q点所示消耗盐酸的体积等于氨水的体积
D.M点和N点所示溶液中水的离子积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜锈的主要成分有 Cu2(OH)2CO3 和 Cu2(OH)3Cl,结构如图所示。考古学家将铜锈分为无害锈和有害锈, 下列说法不正确的是( )

A.上述铜锈的形成过程中,铜均为负极
B.Cu2(OH)2CO3 结构致密,属于无害锈
C.在文物表面涂抹饱和食盐水,能够对文物起到保护作用
D.上述铜锈的形成过程中,正极电极反应式均为O2+4e+2H2O=4OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用标准0.1400molL-1NaOH溶液滴定未知浓度硫酸的实验操作如下。
A.用酸式滴定管取稀H2SO425.00mL,注入锥形瓶中,加入酚酞。
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度,用去NaOH溶液15.00mL。
(1)①滴定操作的正确顺序是(用序号填写)___;②在G操作中如何确定终点?___。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”)___。
(3)配制100mLNaOH标准溶液,必须使用到的玻璃仪器是___。
(4)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值___(选填“偏大”“偏小”或“无影响”)
(5)计算待测硫酸溶液的物质的量浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以明矾![]() 为原料制备Al、
为原料制备Al、![]() 和
和![]() 的工艺流程如下:
的工艺流程如下:
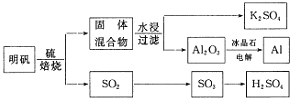
依据上述流程图回答下列问题:
![]() 写出明矾和硫单质混合焙烧发生反应的化学方程式______.
写出明矾和硫单质混合焙烧发生反应的化学方程式______.
![]() 从水浸后的滤液中得到
从水浸后的滤液中得到![]() 晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
![]() 电解
电解![]() 时加入冰晶石的作用是______.
时加入冰晶石的作用是______.
![]() 以Al和
以Al和![]() 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时![]() 转化为
转化为![]() ,该电池反应的化学方程式是______.
,该电池反应的化学方程式是______.
![]() 焙烧产生的
焙烧产生的![]() 可用于制硫酸.已知
可用于制硫酸.已知![]() ,101kPa时:
,101kPa时:
![]()
![]()
![]()
则![]() 和
和![]() 反应的热化学方程式是______.
反应的热化学方程式是______.
![]() 焙烧948吨明矾
焙烧948吨明矾![]() ,若
,若![]() 的利用率为
的利用率为![]() ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为![]() 的硫酸?
的硫酸?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2-硝基甲苯和4-硝基甲苯均可用于印染行业,实验室利用下列反应和装置制备这两种物质。
 (反应明显放热)
(反应明显放热)

实验中可能用到的数据:
相对分子质量 | 密度/gcm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 92 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
2-硝基甲苯 | 137 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
4-硝基甲苯 | 137 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比3:1配制浓硫酸与浓硝酸混合物40mL;
②在三颈瓶中加入20.0mL甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出2-硝基甲苯和4-硝基甲苯并称重,其总总质量为13.7g。
(1)在烧杯中配制该实验所需混酸的方法是___。
(2)步骤④的关键是控制温度,其措施有水浴加热、充分搅拌和___。
(3)分离产物的方案如下:

回答下列问题:
操作ii中会用到下列仪器中的___(填序号)。
a.温度计 b.蒸发皿 c.锥形瓶 d.分液漏斗
该实验中2-硝基甲苯和4-硝基甲苯的总产率为___。
(4)实验中的无机混合物可以回收再利用,回收前需要测定各成分的浓度,取10.00mL无机混合物,加水稀释至100.00mL待用,取稀释液10.00mL,用0.1000molL-1NaOH溶液滴定至溶液呈中性,消化NaOH溶液VmL,另取稀释液10.00mL,加入过量BaCl2溶液,充分反应后过滤并将滤渣洗涤、干燥后称重,质量为Wg。
①取10.00mL稀释液的过程中,酸式滴定管的初始液面为0.20mL,左手控制活塞向锥形瓶中加稀释液,此时眼睛应该___。
②设计简单实验证明滤渣已经洗涤干净:___。
③原无机混合物中HNO3的浓度为___molL-1(用含V和W的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示)。下表是某温度下几种常见弱酸的电离平衡常数:
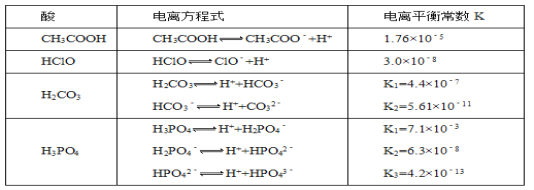
回答下列问题:
(1)若把CH3COOH、HClO、H2CO3、HCO3-、H3PO4、H2PO4-、HPO42-都看作是酸,则它们酸性最强的是___________(填化学式,下同),最弱的是_________________
(2)向NaClO溶液中通入少量的二氧化碳,发生的离子方程式为__________________________,1.2molL﹣1的NaClO溶液pH=__________________________(已知:lg2=0.3)。
(3)求出该温度下,0.10molL﹣1的CH3COOH溶液中的c(H+)=____________molL﹣1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,用蒸馏水稀释1 mol/L氨水至0.01 mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A.![]() B.c(H+)·c(OH-)
B.c(H+)·c(OH-)
C.![]() D.c(OH-)
D.c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电子排布式或轨道表示式正确的是( )
①C原子的轨道表示式:![]()
②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式:![]()
④Br原子的外层电子排布式:3d104s24p5
⑤B原子的轨道表示式:![]()
A.① ② ③B.② ③ ④C.① ② ④ ⑤D.只有③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com