
ОТ№ъКЗёцёЦМъґу№ъ,ёЦМъІъБїѕУКАЅзµЪТ»О»,ёЯВЇБ¶МъКЗЧоОЄЖХ±йµДБ¶Мъ·Ѕ·ЁЎЈДіЦЦїуКЇЦРМъФЄЛШТФСх»ЇОпFemOnµДРОКЅґжФЪ,ПЦЅшРРИзПВКµСй:Ѕ«ЙЩБїМъїуКЇСщЖ··ЫЛй,іЖИЎ25.0 gСщЖ·УЪЙХ±ЦР,јУИлПЎБтЛбід·ЦИЬЅв,ІўІ»¶ПјУИИЎўЅБ°и,ВЛИҐІ»ИЬОпЎЈПтЛщµГВЛТєЦРјУИл10.0 gН·Ыід·Ц·ґУ¦єу№эВЛЎўПґµУЎўёЙФпµГКЈУа№ММе3.6 gЎЈКЈПВВЛТєУГ2 molЎ¤L-1µДЛбРФKMnO4µО¶Ё,ЦБЦХµгК±ПыєДKMnO4ИЬТєМе»э25.0 mLЎЈ
(1)јЖЛгёГМъїуКЇЦРМъФЄЛШµДЦКБї·ЦКэЎЈ
(2)јЖЛгСх»ЇОпFemOnµД»ЇС§КЅ(mЎўnОЄХэХыКэ)ЎЈ
(1)56%ЎЎ(2)Fe5O7
ЎѕЅвОцЎї(1)ТАѕЭ8H++Mn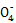 +5Fe2+
+5Fe2+ Mn2++5Fe3++4H2OїЙЦЄn(Fe2+)=5n(Mn
Mn2++5Fe3++4H2OїЙЦЄn(Fe2+)=5n(Mn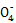 )=5ЎБ0. 025 LЎБ2 molЎ¤L-1=0.25 mol,m(Fe)=14 g,МъїуКЇЦРМъФЄЛШµДЦКБї·ЦКэ=
)=5ЎБ0. 025 LЎБ2 molЎ¤L-1=0.25 mol,m(Fe)=14 g,МъїуКЇЦРМъФЄЛШµДЦКБї·ЦКэ=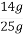 ЎБ100%=56%;(2)ІОјУ·ґУ¦n(Cu)=
ЎБ100%=56%;(2)ІОјУ·ґУ¦n(Cu)=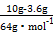 =0.1 mol,ТАѕЭ2Fe3++Cu
=0.1 mol,ТАѕЭ2Fe3++Cu 2Fe2++Cu2+їЙЦЄМъїуКЇЦРn(Fe3+)=0.2 molЎўn(Fe2+)=0.25 mol-0.2 mol=0.05 mol,1ёцёГСх»ЇОп·ЦЧУє¬УРТ»ёц+2јЫМъФЧУ,є¬УР4ёц+3јЫМъФЧУ,ТАѕЭ»ЇєПјЫїЙЦЄOФЧУОЄ7ёц
2Fe2++Cu2+їЙЦЄМъїуКЇЦРn(Fe3+)=0.2 molЎўn(Fe2+)=0.25 mol-0.2 mol=0.05 mol,1ёцёГСх»ЇОп·ЦЧУє¬УРТ»ёц+2јЫМъФЧУ,є¬УР4ёц+3јЫМъФЧУ,ТАѕЭ»ЇєПјЫїЙЦЄOФЧУОЄ7ёц



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦёґП° ЧЁМв11УР»ъ»ЇС§»щґЎБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
ўсКЗЦШТЄµД»Ї№¤ФБПЈ¬їЙ·ўЙъПВБР·ґУ¦ЙъіЙўуєНўфЎЈ

»ЇєПОпўсїЙУГКЇУНБСЅвЖшЦРµД2-ОмП©АґєПіЙЈ¬БчіМИзПВЈє
CH3ЎЄCH==CHЎЄCH2ЎЄCH3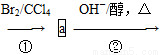 CH2==CHЎЄCH==CHЎЄCH3
CH2==CHЎЄCH==CHЎЄCH3
(1)aµДЅб№№јтКЅКЗ________________Ј»ўЪµД·ґУ¦АаРНКЗ____________ЎЈ
(2)Рґіц·ґУ¦ўЩµД»ЇС§·ЅіМКЅ________________Ј¬ёГ·ґУ¦АаРНКЗ________ЎЈ
(3)ўЩУГјЧґјУлДіУР»ъОп·ўЙъхҐ»Ї·ґУ¦їЙєПіЙ»ЇєПОпўтЈ¬РґіцёГ·ґУ¦µД»ЇС§·ЅіМКЅ________________________________________________________ЎЈ
ўЪ»ЇєПОпўтУлРВЦЖµДЗвСх»ЇНРьЧЗТє·ґУ¦µД»ЇС§·ґУ¦·ЅіМКЅОЄ___________ЎЈ
(4)»ЇєПОпўфКЗўуµДН¬·ЦТм№№МеЈ¬ТІУРН¬СщµДБщФЄ»·Ј¬ўфµДЅб№№јтКЅОЄ______ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦіеґМ·ЗСЎФсМвФц·ЦЧЁБ· »щ±ѕёЕДоЎў»щ±ѕАнВЫБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
ГєЦ±ЅУИјЙХµДДЬБїАыУГВКЅПµНЈ¬ОЄМбёЯЖдАыУГВКЈ¬№¤ТµЙПЅ«ГєЖш»Ї(ЧЄ±діЙCOєНH2)єуФЩєПіЙТТґјЎў¶юјЧГСµИ¶аЦЦДЬФґЎЈ
(1)ИзНјЛщКѕКЗТ»ЦЦЛбРФИјБПµзіШѕЖѕ«јмІвТЗЈ¬ѕЯУРЧФ¶ЇґµЖшБчБїХмІвУлїШЦЖµД№¦ДЬЈ¬·ЗіЈККєПЅшРРПЦіЎѕЖѕ«јмІвЎЈёГµзіШµДёєј«·ґУ¦КЅОЄ______________________ЎЈ

(2)ГєЖш»ЇЛщµГЖшМеїЙУГУЪ№¤ТµєПіЙ¶юјЧГСЈ¬Жд·ґУ¦ИзПВЈє
2CO(g)Ј«4H2(g) CH3OCH3(g)Ј«H2O(g)ЎЈ
CH3OCH3(g)Ј«H2O(g)ЎЈ
Н¬К±·ўЙъё±·ґУ¦ЈєCO(g)Ј«2H2(g) CH3OH(g)Ј»CO(g)Ј«H2O(g)??CO2(g)Ј«H2(g)ЎЈ
CH3OH(g)Ј»CO(g)Ј«H2O(g)??CO2(g)Ј«H2(g)ЎЈ
ФЪОВ¶ИОЄ250 ЎжЎўС№ЗїОЄ3.0 MPaК±Ј¬Ді№¤і§°ґН¶БП±ИV(H2)ЎГV(CO) ЈЅaЅшРРЙъІъЈ¬ЖЅєвК±·ґУ¦МеПµЦРёчЧй·ЦµДМе»э·ЦКэИзПВ±нЈє
ОпЦК | H2 | CO | CO2 | (CH3)2O | CH3OH(g) | H2O(g) |
Ме»э·ЦКэ | 0.54 | 0.045 | 0.18 | 0.18 | 0.015 | 0.03 |
ўЩН¶БП±ИaЈЅ________Ј»
ўЪ250ЎжК±·ґУ¦CO(g)Ј«H2O(g) CO2(g)Ј«H2(g)µДЖЅєвіЈКэKЈЅ________ЎЈ
CO2(g)Ј«H2(g)µДЖЅєвіЈКэKЈЅ________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦіеґМСЎФсМвПЮК±МбЛЩЧЁБ· ¶ЁБї·ЦОцБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ДіЗ¦ЛбРоµзіШµД№¤ЧчФАнИзНјЛщКѕЈ¬ЖдЧЬ·ґУ¦КЅОЄPbЈ«PbO2Ј«2H2SO4=2PbSO4Ј«2H2OЎЈПВБРЕР¶ПІ»ХэИ·µДКЗ(ЎЎЎЎ)
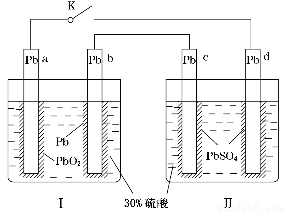
AЈ®±ХєПKК±Ј¬dµзј«µД·ґУ¦КЅОЄPbSO4Ј«2H2OЈ2eЈ=PbO2Ј«4HЈ«Ј«SO42ЎЄ
BЈ®µ±µзВ·ЦРЧЄТЖ0.2 molµзЧУК±Ј¬ўсЦРПыєДµДH2SO4ОЄ0.2 mol
CЈ®±ХєПKК±Ј¬ўтЦРSO42ЎЄПтcµзј«ЗЁТЖ
DЈ®±ХєПKТ»¶ОК±јдєуЈ¬ўтїЙµҐ¶АЧчОЄФµзіШЈ¬dµзј«ОЄХэј«
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦіеґМСЎФсМвПЮК±МбЛЩЧЁБ· ¶ЁБї·ЦОцБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
25ЎжК±Ј¬ДіДСИЬРФјоMOHФЪЛ®ЦРµДіБµнИЬЅвЖЅєвЗъПЯИзНјЛщКѕ(µҐО»ЈєmolЎ¤LЈ1)ЎЈПВБРЛµ·ЁХэИ·µДКЗ(ЎЎЎЎ)

AЈ®ёГјоФЪ25ЎжК±µДKspОЄ2ЎБ10Ј10
BЈ®aµгµДKspґуУЪbµгµДKsp
CЈ®НЁ№эХф·ўїЙК№ИЬТєУЙbµг±дОЄcµг
DЈ®25ЎжК±Ј¬ТЄК№c(MЈ«)ОЄ0.1 molЎ¤LЈ1µДИЬТєРОіЙіБµнЈ¬ИЬТєµДpHЦБЙЩТЄЙэёЯµЅ5
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦЧЁМвёґП°ОпЦКµДЧйіЙ·ЦАај°ДЬБї±д»ЇБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРУР№Ш»ЇС§КµСйµДГиКцЦРХэИ·µДКЗ(ЎЎЎЎ)
A.Ѕ«40 g NaOHИЬУЪ1 LХфБуЛ®ЦР,ёГИЬТєµДОпЦКµДБїЕЁ¶ИОЄ1 molЎ¤L-1
B.ЕдЦЖТ»¶ЁОпЦКµДБїЕЁ¶ИµДNaClИЬТє,Из№ыNaCl№ММеЦРє¬УРNa2CO3,ЛщЕдЦЖИЬТєЦРc(Na+)Ѕ«Ж«µН
C.Ѕ«2.5 g CuSO4Ў¤5H2OИЬЅвФЪ97.5 gЛ®ЦР,ЕдЦЖЦКБї·ЦКэОЄ2.5%µДCuSO4ИЬТє
D.°С200 mL 3 molЎ¤L-1µДBaCl2ИЬТєёъ100 mL 3 molЎ¤L-1µДKClИЬТє»мєПєу,ИЬТєЦРc(Cl-)=5 molЎ¤L-1
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦЧЁМвёґП° АлЧУ·ґУ¦ЎўСх»Ї»№Ф·ґУ¦Б·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
СЗПхЛб(HNO2)КЗТ»ЦЦУлґЧЛбЛбРФПаµ±µДИхЛб,єЬІ»ОИ¶Ё,НЁіЈФЪКТОВПВБўјґ·ЦЅвЎЈ
(1)РґіцСЗПхЛбµДµзАл·ЅіМКЅ:ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(2)ФЪЛбРФМхјюПВ,µ±NaNO2УлKI°ґОпЦКµДБїЦ®±И1ЎГ1ЗЎєГНкИ«·ґУ¦,ЗТI-±»Сх»ЇОЄI2К±,ІъОпЦРє¬µЄµДОпЦКОЄЎЎЎЎЎЎЎЎ(Мо»ЇС§КЅ)ЎЈ
(3)ТЄµГµЅОИ¶ЁµДHNO2ИЬТє,їЙТФПтАд¶іµДNaNO2ЕЁИЬТєЦРјУИл»тНЁИлДіЦЦОпЦК,ПВБРОпЦКІ»ККєПµДКЗЎЎЎЎЎЎЎЎ(МоЧЦДё)ЎЈ
a.ПЎБтЛбЎЎb.¶юСх»ЇМјЎЎc.¶юСх»ЇБтЎЎd.БЧЛб
(4)јоРФ№¤Тµ·ПЛ®ЦРµДN їЙУГВБ·ЫіэИҐЎЈТСЦЄґЛ·ґУ¦МеПµЦРє¬УРAlЎўNaAlO2ЎўNaNO2ЎўNaOHЎўNH3Ў¤H2OЎўH2OБщЦЦОпЦКЎЈ
їЙУГВБ·ЫіэИҐЎЈТСЦЄґЛ·ґУ¦МеПµЦРє¬УРAlЎўNaAlO2ЎўNaNO2ЎўNaOHЎўNH3Ў¤H2OЎўH2OБщЦЦОпЦКЎЈ
ўЩРґіцЙПКц·ґУ¦µДАлЧУ·ЅіМКЅ:ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ўЪ·ўЙъЙПКц·ґУ¦єу·ПЛ®µДpHЅ«ЎЎЎЎЎЎЎЎ(МоЎ°ФцґуЎ±Ў°јхРЎЎ±»тЎ°І»±дЎ±)ЎЈ
(5)ЛбРФ№¤Тµ·ПЛ®ЦРµДN їЙУГДтЛШіэИҐЎЈДтЛШ
їЙУГДтЛШіэИҐЎЈДтЛШ
( )УлN
)УлN ФЪЛбРФМхјюПВ·ґУ¦ЙъіЙБЅЦЦОЮ¶ѕЖшМеЎЈёГ·ґУ¦ЦРЙъіЙ16.8 L(ТСХЫЛгОЄ±кЧјЧґїц)»мєПЖшМеК±,ПыєДДтЛШµДЦКБїОЄЎЎЎЎЎЎЎЎ gЎЈ
ФЪЛбРФМхјюПВ·ґУ¦ЙъіЙБЅЦЦОЮ¶ѕЖшМеЎЈёГ·ґУ¦ЦРЙъіЙ16.8 L(ТСХЫЛгОЄ±кЧјЧґїц)»мєПЖшМеК±,ПыєДДтЛШµДЦКБїОЄЎЎЎЎЎЎЎЎ gЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2013-2014С§ДкёЯїј»ЇС§¶юВЦЧЁМвёґП° µзЅвЦКИЬТєУлµзАлЖЅєвБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
№¤ТµЙПіЈУГ»№ФіБµн·Ёґ¦Анє¬ёх·ПЛ®(Cr2 єНCr
єНCr ),ЖдБчіМОЄ:Cr
),ЖдБчіМОЄ:Cr
 Cr2
Cr2
 Cr3+
Cr3+ Cr(OH)3Ўэ
Cr(OH)3Ўэ
ТСЦЄ:
(1)ІЅЦиўЩЦРґжФЪЖЅєв:2Cr (»ЖЙ«)+2H+
(»ЖЙ«)+2H+ Cr2
Cr2 (іИЙ«)+H2O
(іИЙ«)+H2O
(2)ІЅЦиўЫЙъіЙµДCr(OH)3ФЪИЬТєЦРґжФЪТФПВіБµнИЬЅвЖЅєв:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)іЈОВПВ,Cr(OH)3µДИЬ¶И»эKsp=10-32;ЗТµ±ИЬТєЦРАлЧУЕЁ¶ИРЎУЪ10-5 molЎ¤L-1К±їЙКУЧчёГАлЧУІ»ґжФЪ
ПВБРУР№ШЛµ·ЁЦРХэИ·µДКЗ(ЎЎЎЎ)
A.ІЅЦиўЩЦРјУЛб,Ѕ«ИЬТєµДpHµчЅЪЦБ2,ИЬТєПФ»ЖЙ«,Cr ЕЁ¶ИФцґу
ЕЁ¶ИФцґу
B.ІЅЦиўЩЦРµ±2v(Cr )=v(Cr2
)=v(Cr2 )К±,ЛµГч·ґУ¦2Cr
)К±,ЛµГч·ґУ¦2Cr (»ЖЙ«)+2H+
(»ЖЙ«)+2H+ Cr2
Cr2 (іИЙ«)+H2OґпµЅЖЅєвЧґМ¬
(іИЙ«)+H2OґпµЅЖЅєвЧґМ¬
C.ІЅЦиўЪЦР,ИфТЄ»№Ф1 mol Cr2 ,РиТЄ12 mol (NH4)2Fe(SO4)2Ў¤6H2O
,РиТЄ12 mol (NH4)2Fe(SO4)2Ў¤6H2O
D.ІЅЦиўЫЦР,µ±Ѕ«ИЬТєµДpHµчЅЪЦБ6К±,ФтїЙИПОЄ·ПЛ®ЦРµДёхТСіэѕЎ
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com