
����Ŀ����1����ͬ���ʵ������ơ�þ�������������ᷴӦʱ�ų������������Ϊ__________����ͬ�������ơ�þ�������������ᷴӦʱ�ų��������������_________���ֱ�Ϊ0.3 mol���ơ�þ����Ͷ��100 mL 1 mol��L-1��������Һ�У����߲������������______________��
��2����һ�������Ƶ��������ڳ���CO2���壬Ȼ��������ע��������NaOH��Һ�������ý����ܷ�ڡ�����һ��ʱ��ޱ��ڰ������ٹ�һ��ʱ����˵Ĺޱ����¹�������
�ޱ��ڰ������ԭ����______________________�����ӷ���ʽ����Ϊ____________________________��
���ٹ����ԭ����___________________________�����ӷ���ʽ����Ϊ___________________________��
���𰸡�1��2��3 ![]() ��
��![]() ��
��![]() 3��2��2 CO2�����ն���������ѹѹ�� 2OH-+CO2=CO32-+H2O ��������Ӧ����H2��ѹǿ��������¹��� 2Al+2OH-+2H2O=2AlO2-+3H2��
3��2��2 CO2�����ն���������ѹѹ�� 2OH-+CO2=CO32-+H2O ��������Ӧ����H2��ѹǿ��������¹��� 2Al+2OH-+2H2O=2AlO2-+3H2��
��������
��1����ͬ���ʵ������ơ�þ�������������ᷴӦ��������ȫ��Ӧ�����ݵ���ת���غ����֪���������������֮�ȵ��ڽ����ṩ�������ʵ���֮�ȣ����������������֮��Ϊ1:2:3��
�������Ϊ1g����![]() ��
��![]() ��
��![]() ��������ȫ��Ӧ�������������֮�ȵ��ڽ����ṩ�������ʵ���֮�ȣ��������������֮��Ϊ
��������ȫ��Ӧ�������������֮�ȵ��ڽ����ṩ�������ʵ���֮�ȣ��������������֮��Ϊ![]() ��
��
![]() ������Һ��
������Һ��![]() �����ʵ���Ϊ
�����ʵ���Ϊ![]() ����:
����:![]()
![]()
![]()
![]()
![]()
![]() ��
��
��Al��Mg����������![]() ���㣬��Al��Ӧ��������Ϊ0.1mol����Mg��Ӧ��������Ϊ0.1mol�������ƻ��ã�����ˮ��Ӧ������������
���㣬��Al��Ӧ��������Ϊ0.1mol����Mg��Ӧ��������Ϊ0.1mol�������ƻ��ã�����ˮ��Ӧ������������![]() ����֪�����Ʒ�Ӧ��������Ϊ0.15mol�����ơ�����þ�������������֮��Ϊ
����֪�����Ʒ�Ӧ��������Ϊ0.15mol�����ơ�����þ�������������֮��Ϊ![]() ��
��
��2��
���������ڳ���CO2�����NaOH�ᷢ����Ӧ2NaOH+CO2=Na2CO3+H2O����ʹ��������ѹǿ��С��������������ѹ�������¶�����������NaOH���������ijɷ���������Ӧ������H2�������ķ�Ӧ��2Al+2NaOH+2H2O=2NaAlO2+3H2�������Թ�����ѹǿ���������������ֻ����¹�������


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧϰ���о���ѧ������Ҫ����ʵ�飬���������ʵ����ص����⡣
(1)ʵ�����Ʊ�����ʱ����ʵ��װ�ó�����ͼ��ʾ���ʱ����©������__________ ��
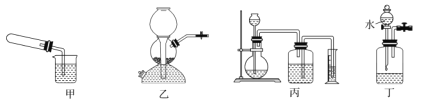
A.װ�ü��������Թ�һ��ʱ�䣬���ɿ���
B.װ���ҷ���CaCO3��ϡ���ᣬ���رճ����ڻ���
C.װ�ñ���ƿ�ڷ������Zn��ϡ����
D.װ�ö����ƿ��װ��MnO2��H2O2���رճ�����ֹˮ�У���Һ©������
(2)������ȡ��Һ�ķ����ڵ�ˮ����ȡ�⣬һ���ѡ��________Ϊ��ȡ������Һ©��ʹ��ǰ��________��ϴ�����á���ȡʱ���Ⱥ�������ȡҺ����ȡ��������ҡ��________����Һ©����������̨����Ȧ�Ͼ���Ƭ�̣��ֲ㡣�������²�Һ��ʱ��Ӧ��_____________��Ȼ������ų��²�Һ�壬�ϲ�Һ����Ͽڵ�����
(3)��Һ�������ᴿʱ����Ҫ�õ��IJ����������˾ƾ��ơ�������ƿ���¶ȼơ�ţ�ǹܡ���ƿ�⣬����___________��������ƿ����ʱ��ӵ�ʯ������ƿ��Һ����ӷ�ʯ�����ѿ�ʼ���ȣ��������Ǽӷ�ʯ��Ӧ���еIJ�����__________________������װ�����¶ȼ�λ����ȷ����_____________�����ܻᵼ���ռ����IJ�Ʒ�л��еͷе����ʵ�װ����________��
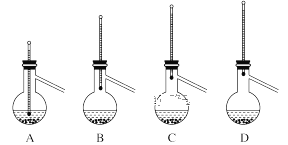
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ����Ǹ��л�ѧ���õ�������������������йؼ��㡣
(1)��0.3 mol Al3����Al2(SO4)3��������SO42�������ʵ�����___________��
(2)___________g H2O2����ԭ������0.2 mo lH3PO4����ԭ������ȡ�
(3)������ͬ��H2��NH3��SO2��O3���������У�����ԭ����Ŀ���ٵ���_____(��д��ѧʽ)��
(4)����涨��1mol���Ӽ�������������������0.024 kg 12C��������̼ԭ������ͬ����ô��36.5 g HCl����ˮ�������Һ500mL������Һ��Ũ��Ϊ_________mol/L��
(5)ͬ��ͬѹ�£�ij��������������116g��������������̼��122g���ֳ���ij������114g����������Ħ������Ϊ___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ���������PFS����ˮ��������Ҫ������������ͼ���Ի��շ���мΪԭ���Ʊ�PFS��һ�ֹ������̣�
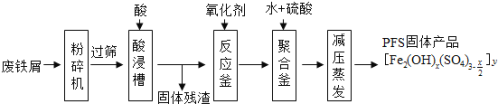
�ش���������
��1������м��ҪΪ���渽�д�������������������Ҫ�ɷ�Ϊ_______�������ɸ��Ŀ����________��
��2�����ʱ����ʵ�����______��д���������ᷴӦ�����ӷ���ʽ_________��
��3����Ӧ���м���������������������������ʵ���______�����ţ���
A��KMnO4 B��Cl2C��H2O2D��HNO3
��4������ڳ�ѹ��������ѹ�������ŵ���____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��������л��ϳ��м��壬��ɺϳ�J��߾���ȣ���ϳ�J����·ͼ��ͼ��
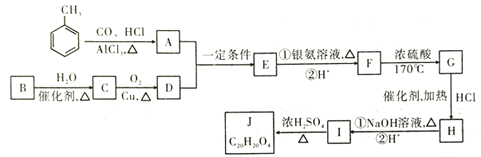
��֪����![]() ��A�����ϵ�һ�ȴ���ֻ��2��
��A�����ϵ�һ�ȴ���ֻ��2��
���л���B����ĵ�ϩ����JΪ����3����Ԫ��������
��![]()
![]() ��
��![]() ��
��![]() Ϊ������Hԭ�ӣ�
Ϊ������Hԭ�ӣ�
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ_____��E�Ļ�ѧʽΪ_____��
��2��![]() �ķ�Ӧ���ͣ�____��H�����й����ŵ�������____��
�ķ�Ӧ���ͣ�____��H�����й����ŵ�������____��
��3��J�Ľṹ��ʽΪ____��
��4��д��I��һ�����������ɸ߾���Ļ�ѧ��Ӧ����ʽ____��
��5���л���K��G��һ��ͬϵ���Է���������G��14�����������������K��ͬ���칹����___�֣������������칹����
a��������ֻ������ȡ����
b�����ܷ���������ӦҲ����![]() ��Һ��Ӧ
��Һ��Ӧ
д�����к˴Ź���������6���壬�����֮��Ϊ2:2:1:1:1:1�Ľṹ��ʽ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���������;�������в���ȷ����
A.�������ƿ����ں������DZˮͧ����Ϊ��������Դ
B.�ڳ����¿�������������������Ũ����
C.Al(OH)3��������θ������һ��ҩ��
D.Al2O3 ��MgO�ǽϺõ��ͻ���ϣ����߾�����NaOH��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ�������й�˵����ȷ����( )
A.38g3H2O2�к���3NA���ۼ�
B.��״���£�2.24L F2ͨ����������ʳ��ˮ�п��û���0.1NA��Cl2
C.�����£���5.6g����Ͷ������Ũ�����У�ת��0.3NA����
D.1L 0.5mol��L1 pH=7��CH3COONH4��Һ��NH4+��ĿΪ0.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��������γ�ʾ��ͼ������ͼʾ�ش��������⡣
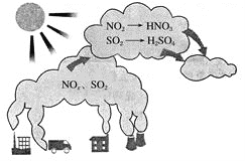
��1����������������������_____��
A��CO2 B��SO2 C��N2 D��NO2
��2��������ˮ��Ʒ1�ݣ�ÿ��һ��ʱ��ⶨ����ˮ��Ʒ��pH�������������£�
����ʱ��/h | 0 | 1 | 2 | 3 | 4 |
��ˮ��pH | 4.73 | 4.63 | 4.56 | 4.55 | 4.55 |
�������ݣ��ش��������⣺
����ˮ��Ʒ��pH�仯��ԭ����____(�û�ѧ����ʽ��ʾ)��
���������ȡ����������ˮ������ˮ���ϣ�pH����____��ԭ����_____(�û�ѧ����ʽ��ʾ)��
��3�����д�ʩ�У��ɼ������������;������____(����ĸ)��
������ú��ȼ�� �ڰѹ����̴���� ��ȼ������ �������ữ�������м�ʯ�� �ݿ�������Դ
A���٢ڢ� B���ڢۢܢ� C���٢ۢ� D���٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�������ƻ���������Ӧ�����ӷ���ʽ��ȷ����
A. ��FeCl3��Һ��ʴͭ��·�壺Cu + 2Fe3+ �� Cu2+ + 2Fe2+
B. ����������ˮ�Ʊ������Cl2 + H2O �� 2H+ + Cl�� + ClO��
C. ���������Ũ�ȵ�Ca(HCO3)2��Һ��NaOH��Һ���Ca2+ + 2HCO3- +2OH-=CaCO3��+CO32-+2H2O
D. ��Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO![]() + 6H+ + 5H2O2 �� 2Mn2+ + 5O2�� + 8H2O
+ 6H+ + 5H2O2 �� 2Mn2+ + 5O2�� + 8H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com