
����Ŀ��ijС��ͬѧΪ̽�� H2O2�� H2SO3�� Br2 ������ǿ�����������ʵ�飨�г���������ȥ��װ�õ��������Ѽ��飩��

ʵ���¼���£�
ʵ����� | ʵ������ | |
�� | ���� a���μ���ˮ���رջ��� a | _____________________________________________ |
�� | �����ȿ���һ��ʱ���ֹͣ | A����Һ��ɫ���Ա�dz��B�������ݣ�����������ɫ�������������ϲ���ҺΪ��ɫ |
�� | ����b����μ���H2O2��Һ | ��ʼʱ��Һ��ɫ�����Ա仯�������μ�H2O2��Һ��һ��ʱ����Һ��ɳȺ�ɫ�� |
���������գ�
��1���ڽ��в�����ʱ��A�е�ʵ��������___________���йط�Ӧ�����ӷ���ʽ��___________��
��2�������ڴ����ȿ�����Ŀ����____________��B �в�����ɫ�����Ļ�ѧʽ��___________��
��3��װ��C��������____________________��
��4��������ʵ���֪���ڴ�ʵ�������£�H2O2��H2SO3��Br2������ǿ��˳��Ϊ________________��
��5�������ۿ�ʼʱ��ɫ�����Ա仯����ԭ���ǣ�д��һ�����ɣ���___________________��
���𰸡� A ����Һ��Ϊ�Ⱥ�ɫ Cl2+2Br-=Br2+2Cl- �������� Br2 BaSO4 ����β�� H2O2��Br2��H2SO3 H2SO3 ��ʣ�ࣨH2O2Ũ��С�� Br-�� H2O2 ��Ӧ�������أ��������ɣ�
��������װ�÷������������á��������������Դ������������һԭ�����Ƚ�H2O2��H2SO3��Br2������ǿ������NaBr��Һ�еμ���ˮ����ˮ�û����嵥�ʣ�Ȼ��Ĵ��ȿ�������Br2(g)����Bװ�ã�H2SO3��BaCl2����Ӧ����Br2(g)���룬�����˰�ɫ��������Br2��H2SO3������H2SO4��Br2����ԭΪBr-��˵��Br2������ǿ��H2SO3���ð�ɫ����ΪBaSO4������Bװ���м���H2O2��Һ��һ��ʱ�����Һ��Ⱥ�ɫ����Br-������ΪBr2��˵��H2O2�����Ա�Br2ǿ��
��1������ a����NaBr��Һ�еμ���ˮ����ˮ����������Ϊ�嵥�ʣ���Ӧ����ʽΪCl2+2Br-=Br2+2Cl-��A����Ϊ���嵥�ʵ���A����Һ��Ⱥ�ɫ��
�ʴ�Ϊ��A����Һ��Ϊ�Ⱥ�ɫ��Cl2+2Br-=Br2+2Cl-��
��2��Br2���лӷ��ԣ��ȿ����ܴٽ�Br2�ӷ�����Br2(g)����Bװ�ã�Br2��H2SO3����ΪH2SO4������ɫ����ΪBaSO4��
�ʴ�Ϊ����������Br2��BaSO4��
��3��װ��C��ΪNaOH��Һ����Ӧ������������������������Ⱦ�����岻���ŷŵ�������,������NaOH��Һ���գ�����װ��C������������β����
�ʴ�Ϊ������β����
��4������������������֪��������H2O2��Br2��H2SO3��
��5���������У���Bװ������μ���H2O2����Һ��ʼʱ��ɫ�����Ա仯��������Ϊ��Bװ���л���H2SO3ʣ�࣬H2O2����H2SO3��Ӧ������Br-��Ӧ��Ҳ��������ΪH2O2Ũ��С�� Br-��H2O2 ��Ӧ�������ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A.��������Һ���Ȼ�����Һ��Ӧ��Ba2++SO ![]() �TBaSO4��
�TBaSO4��
B.ͭ����������Һ��Ӧ��Cu+Ag+�TCu2++Ag
C.����ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2��
D.̼�����ϡ���ᷴӦ��CO ![]() +2H+�TCO2��+H2O
+2H+�TCO2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ������˵������ȷ���ǣ�������
A.������Ӧ�ͻ�ԭ��Ӧͬʱ����
B.һ�������ŵ���ת��
C.һ��������Ԫ�ػ��ϼ۱仯
D.һ���е��ʲμӷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X��Y��Z��Ϊ����Ԫ�أ������������ݣ��ж�����˵����ȷ���ǣ� ��
Ԫ�� | X | Y | Z |
���������� | a | b | a |
ԭ�Ӱ뾶/nm | 0.152 | 0.143 | 0.256 |
A.X��Yλ��ͬһ���壬��X��Y����һ����
B.X��Zλ��ͬһ���壬��X��Z����һ����
C.X��Zλ��ͬһ���ڣ���X��ԭ������С��Z��ԭ������
D.X��Zλ��ͬһ���壬��X��ԭ������С��Z��ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� �� 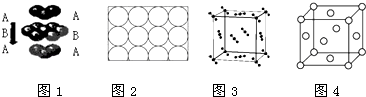
A.�Ѻͼض���ȡͼ1�Ķѻ���ʽ
B.ͼ2Ϊ����ԭ���ڶ�ά�ռ���ķ����ò���ã��˷�ʽ����ά�ռ���ѻ������ü������ѻ�
C.ͼ3�Ǹɱ�����ľ����������ⳤΪa cm������ÿ��CO2��Χ���������Ϊ ![]() acm��CO2��8��
acm��CO2��8��
D.ͼ4���ֽ�������ľ������ǽ���ԭ������ά�ռ��������ò��ȡABCABC���ѻ��Ľ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ���ܴ���������������ǣ�������
A.H+��OH����Na+
B.K+��NO3����Cu2+
C.Ba2+��SO42����Na+
D.Fe3+��OH����NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�������ȡ�ⵥ�ʣ�����Ĺ����������£��ɺ��� ![]() ������
������ ![]() ����Һ
����Һ ![]() ��Һ
��Һ ![]() ��ˮ
��ˮ ![]() I2��CCl4��Һ
I2��CCl4��Һ ![]() I2���й��ں�ˮ�Ƶ��˵��������ȷ���ǣ� ��
I2���й��ں�ˮ�Ƶ��˵��������ȷ���ǣ� ��
A.ʵ�����������������ոɺ����������ò���������
B.��I������Һ�м���ϡ�����˫��ˮ��Ԫ�ط���������Ӧ
C.�ڵ�ˮ�м��뼸�ε�����Һ����Һ����ɫ
D.��ˮ����CCl4�õ�I2��CCl4��Һ���ò���Ϊ����ȡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ���������֪C2H4��C3H6�Ļ���������Ϊa g����û���� ��
A.�������е��Ӷ���ĿΪ ![]() NA
NA
B.����̼�����ĿΪ ![]()
C.��ȫȼ��ʱ���ĵ�O2һ����33.6a/14 L
D.����ԭ������Ϊ ![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com