
【题目】一定条件下,有机化合物 Y 可发生重排反应:
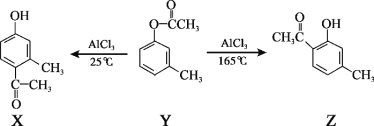
下列说法不正确的是( )
A.X、Y、Z互为同分异构体
B.1 mol X最多能与3 mol H2发生加成反应
C.可以用FeCl3溶液区分Y和Z
D.通过调控温度可以得到不同的目标产物
科目:高中化学 来源: 题型:
【题目】某有机物M结构简式为![]() ,其合成线路如下:
,其合成线路如下:
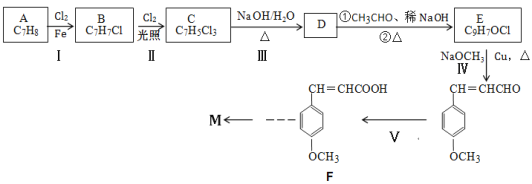
已知①通常在同一个碳原子上连有两个羟基不稳定,易脱水成羰基,即 +H2O
+H2O
②R1CHO+R2CH2CHO![]() +H2O
+H2O
试回答下列问题:
(1)A的1H-NMR谱(核磁共振氢谱)中显示吸收峰的数目为___,有机物M中含氧官能团的名称是___,C的结构简式____。
(2)D→E的转化过程中第①步反应的化学方程式为___。
(3)Ⅳ的反应类型为___,“Ⅴ”包含两步反应,其中第一步反应的试剂、条件是___。
(4)A也是合成阿斯匹林(![]() )的原料,
)的原料,![]() 有多种同分异构体,写出符合下列条件的同分异构体的结构简式___(任写一种)。
有多种同分异构体,写出符合下列条件的同分异构体的结构简式___(任写一种)。
①苯环上有3个取代基;
②仅属于酯类,能发生银镜反应,且1mol该物质反应时最多能生成4molAg;
③苯环上的一氯代物有2种。
(5)若以F和乙醛为原料来合成化合物M(![]() ),试写出合成路线____。
),试写出合成路线____。
(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.某温度下纯水的pH=6,该温度下5LpH=11的NaOH溶液中含OH-的数目为0.5NA
B.1molAlCl3在熔融状态时含有的离子总数为4NA
C.8.7g二氧化锰与含有0.4molHCl的浓盐酸加热充分反应,转移电子的数目为0.2NA
D.12g金刚石中C-C键的数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中,只含有下表中所示的四种离子,试推测X离子及其个数b可能为:( )
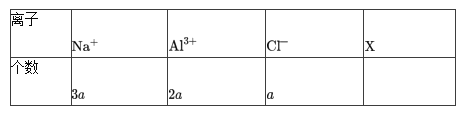
A.SO42- 8aB.OH- 8aC.NO3- 4aD.SO42- 4a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以芳香族化合物A为起始原料,按下列路线合成高血压药物阿替洛尔。
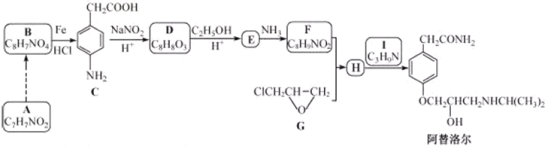
已知:化合物H中除了苯环还有其它环
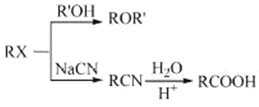 :
:![]()
请回答:
(1)下列说法正确的是________。
A.化合物D能发生加成,取代,氧化反应,不发生还原反应
B.化合物E能与![]() 溶液发生显色反应
溶液发生显色反应
C.化合物1具有弱碱性
D.阿替洛尔的分子式是![]()
(2)写出化合物E的结构简式________。
(3)写出![]() 的化学方程式________。
的化学方程式________。
(4)设计从A到B的合成路线(用流程图表示,无机试剂任选)________。
(5)写出化合物C同时符合下列条件的同分异构体的结构简式________。
①![]() 谱和IR谱检测表明:分子中共有4种氢原子,无氮氧键和碳氮双键;
谱和IR谱检测表明:分子中共有4种氢原子,无氮氧键和碳氮双键;
②除了苯环外无其他环。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置图的叙述中,正确的是

① ②
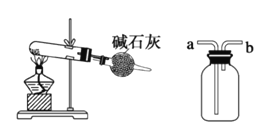
③ ④
A. 装置①:常用于分离互不相溶的液体混合物
B. 装置②:可用于吸收氯化氢、氨气等气体尾气,防止倒吸
C. 装置③:可用于实验室以氯化铵为原料制备少量NH3的实验
D. 装置④:先装满水,再从b口进NO气体,可收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到实验目的的是( )
实验目的 | 实验操作 | |
A | 比较S和Si的非金属性强弱 | 向Na2SiO3溶液中通入SO2产生白色沉淀 |
B | 除去NaHCO3溶液中的杂质Na2CO3 | 向混合液中通入足量的CO2气体 |
C | 检验某盐是否为铵盐 | 试样 |
D | 验证H2O2和Fe3+的氧化性 强弱 | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
B.500℃、30M Pa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH = -38.6 kJ/mol
2NH3(g) ΔH = -38.6 kJ/mol
C.已知热化学方程式:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH = -Q kJ/mol ,若将一定量的SO2(g)和O2(g)置于密闭容器中充分反应后放出热量Q kJ,则此过程中有2 mol SO2(g)被氧化
2SO3(g) ΔH = -Q kJ/mol ,若将一定量的SO2(g)和O2(g)置于密闭容器中充分反应后放出热量Q kJ,则此过程中有2 mol SO2(g)被氧化
D.X(g)+Y(g)![]() Z(g) ΔH >0,恒温恒容条件下达到平衡后加入X,上述反应ΔH增大
Z(g) ΔH >0,恒温恒容条件下达到平衡后加入X,上述反应ΔH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛铁矿是铁和钛的氧化物矿物,成分可表示为FeTiO3(Ti为+4价)。钛白粉(TiO2)涂料、塑料、油墨、造纸行业具有广泛的用途,制备流程如图:
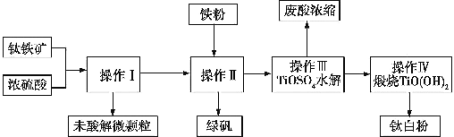
(1)钛铁矿与硫酸反应时可表示为FeTiO3+H2SO4→TiOSO4+X+H2O,其中X的化学式为 ______,该反应为______ (填“氧化还原反应”或“非氧化还原反应”)。
(2)某钛铁矿中FeTiO3的含量为76%,该钛铁矿与硫酸反应时Ti转化率为92%,操作I到操作IV的过程中Ti的转化率为96%,则1t该钛铁矿可生产钛白粉 ______ t(所有计算结果保留两位有效数字),能否计算绿矾的产量______?(若能则计算数值,否则说明理由)。
(3)操作I的名称是 ______,操作II包括搅拌、结晶、______,操作II中加入铁粉的目的是______(用离子方程式表示)。
(4)写出操作III中TiOSO4水解的化学方程式: ______ 。
(5)该生产过程中产生的尾气SO2、SO3的处理方法是 ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com