
【题目】质子交换膜燃料电池(简称:PEMFC),又称固体高分子电解质燃料电池,是一种以含氢燃料与空气作用产生电力与热力的燃料电池,膜极组和集电板串联组合成一个燃料电池堆。目前,尤以氢燃料电池倍受电源研究开发人员的注目。它的结构紧凑,工作温度低(只有80℃),启动迅速,功率密度高,工作寿命长。工作原理如图,下列说法正确的是
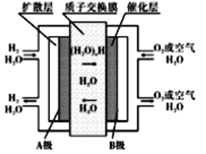
A. 可用一氧化碳代替图中氢气形成质子交换膜燃料电池
B. B极的电极反应式为O2+4H++4e-=2H2O
C. 用该电池作为精炼铜的电源时,A极与粗铜电极相连
D. 当外电路中转移0.1mole-时,通过质子交换膜的H+数目为0.2NA
科目:高中化学 来源: 题型:
【题目】以黄铜矿(主要成分二硫化亚铁铜CuFeS2)为原料,用Fe2(SO4)3溶液作浸取剂提取铜,总反应的离子方程式是CuFeS2 + 4Fe3+ ![]() Cu2+ + 5Fe2+ + 2S。
Cu2+ + 5Fe2+ + 2S。
(1)该反应中,Fe3+体现________性。
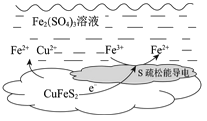
(2)上述总反应的原理如图所示。
负极的电极反应式是________。
(3)一定温度下,控制浸取剂pH = 1,取三份相同质量黄铜矿粉末分别进行如下实验:
实验 | 操作 | 2小时后Cu2+浸出率/% |
I | 加入足量0.10 mol·L-1 Fe2(SO4)3溶液 | 78.2 |
II | 加入足量0.10 mol·L-1 Fe2(SO4)3溶液,通入空气 | 90.8 |
III | 加入足量0.10 mol·L-1 Fe2(SO4)3溶液,再加入少量0.0005 mol·L-1 Ag2SO4溶液 | 98.0 |
①对比实验I、II,通入空气,Cu2+浸出率提高的原因是________。
②由实验III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+==Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+==2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005 mol·L-1 Ag2SO4溶液,充分混合后静置。取上层清液,加入稀盐酸,观察到溶液中________,证明发生反应i。
b.取少量Ag2S粉末,加入________溶液,充分混合后静置。取上层清液,加入稀盐酸,有白色沉淀,证明发生反应ii。
(4)用实验II的浸取液电解提取铜的原理如图所示:
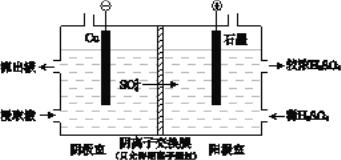
① 电解初期,阴极没有铜析出。用电极反应式解释原因是_______________。
② 将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是 _____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染.下列做法不符合绿色化学理念的是( )
A.研制水溶剂涂料替代有机溶剂涂料
B.用可降解塑料生产包装盒或快餐盒
C.用反应:Cu+2H2SO4(浓) ![]() ?CuSO4+SO2↑+2H2O? 制备硫酸铜
?CuSO4+SO2↑+2H2O? 制备硫酸铜
D.用反应:2CH2=CH2+O2 ![]()
![]() 制备环氧乙烷
制备环氧乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某些植物树叶提取的挥发油中含有下列主要成分: 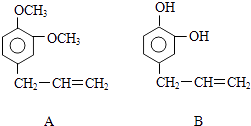
(1)写出A的分子式 .
(2)1molB与溴水充分反应,需消耗mol单质溴 .
(3)写出A与B在一定条件下相互反应,生成高分子化合物的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定
B.已知C(s)+O2(g)═CO2(g)△H1 C(s)+ ![]() O2(g)═CO(g)△H2 , 则△H2>△H1
O2(g)═CO(g)△H2 , 则△H2>△H1
C.已知2H2(g)+O2(g)═2H2O(g)△H=﹣483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol
D.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=﹣57.3 kJ/mol,则含20 g NaOH的稀溶液与稀盐酸完全中和,中和热为28.65 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中A、C、D、E为短周期元素,最外层电子数之和为23,下列说法正确的是
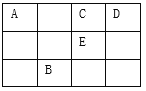
A. 元素A对应的氢化物,常温下一定是气态
B. 元素B、E的原子序数相差19
C. 与金属钠的反应中,1molC原子和1molE原子得电子数目一定相等
D. A、C、D均可形成18e-分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是:
A. 标准状况下,VL气态烯烃(CnH2n)含中子的数目为![]()
B. 1LFe2(SO4)3溶液中,若c(Fe3+)=2 molL-1,则SO42-的数目为3NA
C. 一定量的硝酸和铁粉反应放出0.5mol气体,则转移的电子数一定是1.5NA
D. 46g甲酸含H-O键的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的原理为N2(g)+3H2(g)![]() 2NH3(g),请回答下列问题:
2NH3(g),请回答下列问题:
(1)已知拆开1mol H﹣H键、1mol N≡N、1mol N﹣H键分别需要吸收的能量为436kJ、946kJ、391kJ。则由N2和H2反应生成1mol NH3需要放出_________的热量。
(2)若N2、H2、NH3的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),则各物质的浓度有可能的是___________。
A.c=0.5mol/L B.b=0.5mol/L
C.c=0.4mol/L D.a=0.3mol/L
(3)若在2L密闭容器中,充入1 mol N2和3mol H2,2min时达到平衡。测得平衡时N2的浓度为0.3 mol/L。
①2min内v(NH3)=___________。
②平衡时容器的压强与起始时压强之比___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质与条件己略去)。已知A、C由两种相同元素組成的物质,其A摩尓质量为65g/mol,C是白色粉末且焰色反应呈黄色,I是最常见的液体,E是一种红棕色气体,B、F都是无色气体单质。
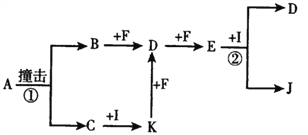
(1)E的化学式为________。
(2)C的电子式为_________。
(3)用电子式表示I的形成辻程________。
(4)写出反应①的化学方程式________。
(5)写出反应②的离子方程式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com