
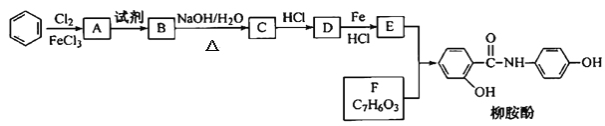
����Ŀ��ij�������Ա�Ϊ��Ҫԭ�ϣ���ȡ����·�ߺϳ�����ҩ���������ӡ�
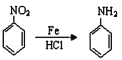
��֪����
��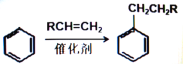 ��RΪ������Hԭ�ӣ�
��RΪ������Hԭ�ӣ�
�ش��������⣺
��1�����������ӣ�����˵����ȷ����___������ţ���
A.1mol�����������Ժ�2molNaOH��Ӧ
B.���ܷ���������Ӧ
C.�ɷ���ˮ�ⷴӦ
D.�����巢��ȡ����Ӧ
��2��д��A��B��Ӧ������Լ�___��
��3��д��B��C�Ļ�ѧ����ʽ___��
��4��д��������F�Ľṹ��ʽ____��
��5��д��ͬʱ��������������F��ͬ���칹��Ľṹ��ʽ___��д��1�֣���
�����������ұ����������ֲ�ͬ��ѧ��������ԭ�ӣ����ܷ���������Ӧ
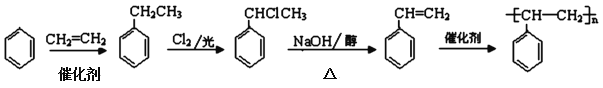
��6���Ա�����ϩΪԭ�Ͽɺϳɾ۱���ϩ������ƺϳ�·��___�����Լ����ܼ���ѡ����
ע���ϳ�·�ߵ���д��ʽ��������ʾ������ͼ��
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
���𰸡�C��D Ũ�����Ũ���� 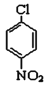 +2NaOH
+2NaOH +NaCl+H2O
+NaCl+H2O 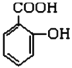
 ��
�� ��
�� ��
��
��������
����������̺���Ϣ���������ʵ����ʷ���AΪ�ȱ����������ӵĽṹ����֪��EΪ�������ӣ��ṹ��ʽΪ![]() ��FΪ���ǻ�������
��FΪ���ǻ�������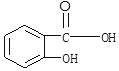 �����ƿ�֪��BΪ����������
�����ƿ�֪��BΪ����������![]() ��CΪ������������
��C������������![]() ��D����������
��D����������![]() ��
��
(1)A��1 mol�����Ӻ���2mol���ǻ���1mol�ļ��������Ժ�3 molNaOH��Ӧ��A����B���������к��б������ܷ���������Ӧ��B����
C���������к����ļ����ɷ���ˮ�ⷴӦ��C��ȷ��
D���������з��ǻ��ڡ���λ������ԭ�ӣ������巢��ȡ����Ӧ��D��ȷ��
��ѡCD��
(2)���Ϸ�����AΪ�ȱ���BΪ������������A![]() B����������Ӧ��������Լ�ΪŨ�����Ũ���ᡣ
B����������Ӧ��������Լ�ΪŨ�����Ũ���ᡣ
(3)BΪ������������CΪ�����������ƣ�B������������Һ������ԭ��ȡ����Ӧ���ɷ��ǻ������ǻ����������Ƽ�����Ӧ����C����ѧ����ʽΪ +2NaOH
+2NaOH +NaCl+H2O��
+NaCl+H2O��
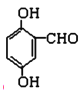
(4)���Ϸ���������FΪ���ǻ������ᣬ�ṹ��ʽΪ ��
��
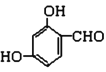
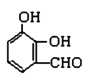
(5)F��ͬ���칹������������ұ����������ֲ�ͬ��ѧ��������ԭ�ӣ� ���ܷ���������Ӧ������ȩ���������������л���Ľṹ��ʽΪ ��
�� ��
�� ��
�� ��
��
(6)������֪�ڿ�֪��������ϩ�ڴ��������������ұ����ұ�����������ȡ����Ӧ���������������ԭ�ӵ���ȥ��Ӧ���ɱ���ϩ������ϩ�������������·������۷�Ӧ�ϳɾ۱���ϩ������ϳ�·��Ϊ��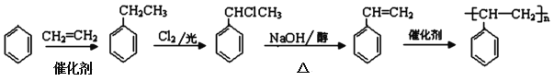 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǰ뵼���绯ѧ��ع��ˮ����ķ�Ӧԭ��ʾ��ͼ���ڹ����£������ɼ۴�ԾǨ��������Ȼ������Ե缫������˵������ȷ����

A. �Ե缫�ĵ缫��ӦʽΪ��2H++2e��=H2��
B. �뵼��缫������ԭ��Ӧ
C. �������Һ����������Ե缫�ƶ�
D. ����������ʵ����̫���ܡ����ܡ���ѧ�ܵ�ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��г���5��Ԫ�������ڱ��е�λ�á�
| ��A | 0 | ||||||
1 | ��A | ��A | ��A | ��A | ��A | ��A | ||
2 | �� | �� | ||||||
3 | �� | �� | �� |
(1)����Ԫ�ط�����________������ԭ�ṹʾ��ͼ��________________��
(2)����Ԫ���У���������ǿ����________________(��Ԫ�ط���)��
(3)��Ԫ�ص�����������Ӧ��ˮ�����________��(������������������������)��
(4)�ۢܢ�����Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳����__________(��Ԫ�ط���)��
(5)Ԫ������Ԫ�����γɵĻ������������________________��
(6)����Ԫ�����ĵ���ͨ��������________��(����ú��������ˮ��)��
(7)Ԫ������Ԫ�����ĵ��������Խ�ǿ����________(�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ú��ܷ���(��Ҫ�ɷ�ΪCoCO3������������NiCO3����м)�Ʊ�CoCl26H2O�Ĺ���������ͼ��
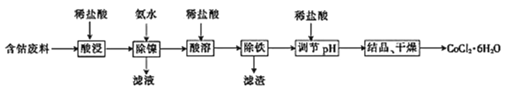
����֪������������ҺpH���ܵĻ����ʼ�Ni2+������Ӱ����ͼ��ʾ��
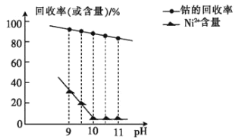
�ڲ��ֽ�����������ʵ�������¿�ʼ��������ȫ������pH�����ʾ��
���������� | ��ʼ����pH | ��ȫ����pH |
Fe3+ | 1.5 | 4.0 |
Fe2+ | 7.5 | 9.7 |
Co2+ | 6.6 | 9.4 |
Ni2+ | 7.7 | 9.5 |
�ش��������⣺
(1)�������Һ�е�������Ϊ��Co2+��Ni2+��__��
(2)����ʱ��Ӧ������ҺpH=__����ʱNi2+�Ƿ��γ�Ni(OH)2������___(�ǻ��)����pH��С�����Ʒ���Ȼ�___(���ߣ����ͣ���)��
(3)����ʱ��������pH=8ʱ����Һ��n(Fe3+)��n(Co2+)=__��
��֪Ksp[Co(OH)2]=2.0��10-16��Ksp[Fe(OH)3]=4.0��10-38��
(4)����ʱ������Һ�м���30%��H2O2���������ӷ�Ӧ����ʽ�ǣ�__����ַ�Ӧ��������Һ�м���CoCO3��������ҺpH��ΧΪ__��ʹFe3+��ȫת��ΪFe(OH)3�����������˵õ�CoCl2��Һ��
(5)��֪Ag++SCN-=AgSCN����Ϊ�ⶨ�ֲ�Ʒ��CoCl26H2O�ĺ�������ȡ11.9g�ֲ�Ʒ���100mL��Һ������ȡ��25mL�ȼ��뺬0.03mol��AgNO3��(���ʲ����䷴Ӧ)������0.5mol/L��KSCN��Һ�궨������AgNO3���ñ궨�������õ�ָʾ��Ϊ__(�ѧʽ)��������20.00mL��KSCN��Һ����ôֲ�Ʒ��CoCl26H2O����������Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����������ͽ��۾���ȷ���ǣ� ��
ѡ�� | ʵ����� | ʵ������ | ���� |
A | ��ij�л�����������Ȼ�̼��Һ��� | ��Һ��ɫ | ���л����бض�����̼̼˫�� |
B | ������������Һ�еμ����ᱵ��ϡ���� | ������ɫ���� | ����������Һ�ѱ��� |
C | �����Ը��������Һ�еμ�˫��ˮ | ��ɫ��ȥ���������� | H2O2���л�ԭ�� |
D | ���Ҵ���Һ�м�һС���� | �������� | �Ҵ������ǻ� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽�������ﵽ��ӦĿ�ĵ��ǣ� ��
Ŀ�� | A.��֤�������������������� | B.�о�Ũ�ȶ�FeCl3ˮ��ƽ���Ӱ�� |
ʵ�鷽�� |
|
|
Ŀ�� | C.�Ƚ�CH3COOH��H3BO3�����ᣩ���Ե�ǿ�� | D.�Ƚ�AgCl��AgI�ܽ�ȵĴ�С |
ʵ�鷽�� |
|
|
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е�ʳƷ���Ӽ��а�ɰ�ǡ�������̼������ɫ�����ᡢ������ȡ����ֵ�����ζ�����ᣨ��ѧʽΪH3PO4���е���ѻӷ�����һ����ϵ��
(1)�����£����0.1mol/LH3PO4��Һ��pH=1.5���õ��뷽��ʽ����ԭ��__��
(2)���ڹ������ÿ��ֻ��ƻ������ʣ�ʹ�����ƽ�����ѿ����ƶ������ȣ�ݡ����ƽ���ƶ�ԭ������ԭ��__��
Ca5(PO4)3OH(s)![]() 5Ca2+(aq) +3PO
5Ca2+(aq) +3PO![]() (aq)+OH-(aq)
(aq)+OH-(aq)
(3)��������Һ�еμ�NaOH��Һ������������Һ�е����ʵ���������pH�Ĺ�ϵ��ͼ��ʾ��
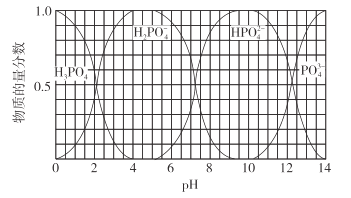
����������Һ�еμ�NaOH��Һ��pH=10ʱ��������Ҫ��Ӧ�����ӷ���ʽ��___��
�����й���0.1mol/LNa2HPO4��Һ��˵����ȷ����__������ţ���
a��Na2HPO4��Һ�Լ��ԣ�ԭ����HPO![]() ��ˮ��̶ȴ��������̶�
��ˮ��̶ȴ��������̶�
b��c(Na+)+c(H+)=c(H2PO![]() )+2c(HPO
)+2c(HPO![]() )+3c(PO
)+3c(PO![]() )+c(OH-)
)+c(OH-)
c��c(Na+)=c(H2PO![]() )+c(HPO
)+c(HPO![]() )+c(PO
)+c(PO![]() )+c(H3PO4)
)+c(H3PO4)
(4)С��ͬѧ��ʵ���Ҳⶨij����������ĺ����������ǰ�ɰ�ǡ��������Ӱ�죩��
i.��һƿ����ע��Բ����ƿ���������̿������ɫ�ء�
��.�����ֻ�������10min����ȴ�����£����ˡ�
��.ȡ50.00mL��Һ���ð������̪��ָʾ������0.100mol/LNaOH��Һ�ζ����յ�ʱ����Na2HPO4������NaOH��Һ5.00mL��
�����ȵ�Ŀ����__��
���ÿ�����Ʒ������ĺ���Ϊ__g/L��H3PO4Ħ������Ϊ98g/mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������Ҫ�Ļ���ԭ��֮һ���㷺Ӧ�����Ṥ�ջ������ġ�ʳƷ��ҵ����ҵ��
(1)����̼�����к����Ȼ������ʣ�ѡ�������Լ����ʵ�鷽�����м��飬�Լ���ϡH2 SO4��BaCl2��Һ��Ca(NO3)2��Һ��AgNO3��Һ
ʵ�鲽�� | �� �� |
��ȡ������Ʒ��������ˮ�ܽ� | �ڹ�����ȫ�ܽ�õ���ɫ������Һ |
��_____ | ���а�ɫ�������� |
�ݾ��ã�________ | �� ________ |
(2)��AgNO3����Һ�ζ�Cl-(��K2CrO4��ҺΪָʾ����Ag2CrO4Ϊש��ɫ����)�����ⶨ̼���ƵĴ��ȡ�
��������Ʒ��Һ����ȡij̼������Ʒmg��������ƿ����100 mL��Һ������ʱ����____������ˮ���̶��ߡ�
������AgNO3��Һ��Ũ�ȱ궨����ȡAgNO3����8.5 g���ձ��У���____ȡ500 mLˮ�������ձ��У�����ҡ�Ⱥ�ת��____ɫ�Լ�ƿ�����ڰ��������á���NaCl����Һ�궨����AgNO3��ҺŨ��Ϊb mol/L��
�۵ζ���Ʒ��ȡ��Ʒ��Һ20. 00 mL����ƿ�У��ӹ���ϡHNO3������2��3��K2 CrO4��Һ����AgNO3����Һ�ζ����ζ��յ������Ϊ_________��
�ظ������������Ρ��Ĵβⶨ�������±���
ʵ����� | 1 | 2 | 3 | 4 |
����AgNO3��Һ���/mL | 20.00 | 21. 55 | 20. 02 | 19. 98 |
���ڵζ��յ��ȡ�ζ��̶ܿ�ʱ���ӱ�ҺҺ�棬��ⶨ���____(����ƫ��������ƫ����������Ӱ����)����Ʒ�Ĵ���Ϊ____%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����������ȷ���ǣ���
A.![]() 1��3��4-���ױ�
1��3��4-���ױ�
B.![]() 3-����ϩ
3-����ϩ
C.![]() 2-��-1-����
2-��-1-����
D.![]() 1��3-�������
1��3-�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com