
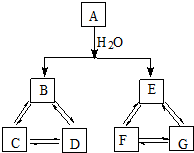
 有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:
有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,则该化合物的结构简式可能是(4种):
,则该化合物的结构简式可能是(4种):查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C是三种常见短周期元素的单质,常温下D为无色液体,E是一种常见的温室气体,F是化合物.其转化关系如图(反应条件和部分产物略去).
A、B、C是三种常见短周期元素的单质,常温下D为无色液体,E是一种常见的温室气体,F是化合物.其转化关系如图(反应条件和部分产物略去).查看答案和解析>>
科目:高中化学 来源: 题型:
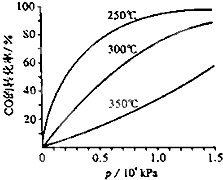 Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
| ||
| △ |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不慎将酸溅入眼中,立即用水冲洗,边洗边眨眼睛 |
| B、不慎将碱液沾到皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 |
| C、不慎碰翻酒精灯导致失火,马上用湿抹布扑灭 |
| D、稀释浓硫酸时,先把浓硫酸注入量筒,然后向其中加入水,边加边搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com